Ступінь окиснення. Визначення ступеня окиснення елемента за хімічною формулою сполуки. Складання формули сполуки презентация
Содержание
- 2. Мета уроку: закріпити знання про ступінь окиснення, розвивати навички визначення ступеня окиснення в сполуках за формулами,
- 3. Валентність ⎯це зв’язки (спільні електронні пари) між елементами Ступінь окиснення і валентність — родинні поняття. У
- 4. Основні правила визначення ступенів окиснення - Металічні елементи мають у сполу-ках лише позитивний ступінь окис-нення. -
- 5. Основні правила визначення ступенів окиснення Ступінь окиснення елементів у простих речовинах дорівнює нулю (H02, Na0, P0,
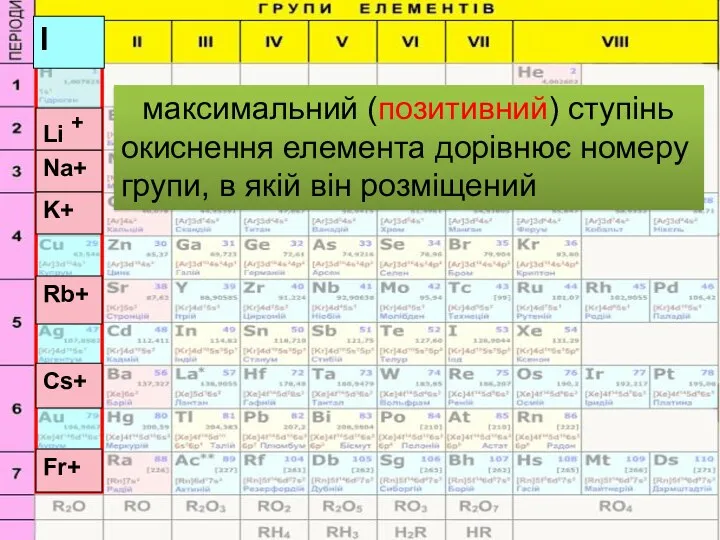
- 6. максимальний (позитивний) ступінь окиснення елемента дорівнює номеру групи, в якій він розміщений Na+ Li + K+
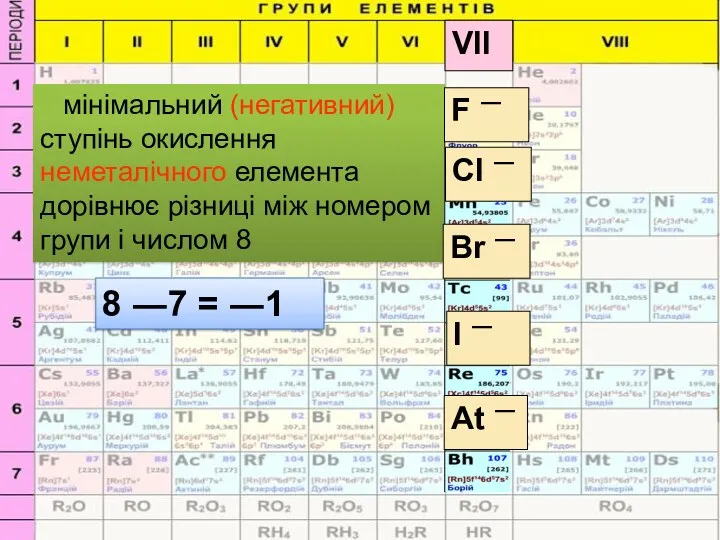
- 7. мінімальний (негативний) ступінь окислення неметалічного елемента дорівнює різниці між номером групи і числом 8 I ―
- 8. Варіант I: Na2O, CuO, H2S, Н3РO4. Варіант II: MgS, NH3, Fe2O3, HNO3. Визначити ступені окиснення у
- 9. Алгоритм складання формули бінарної сполуки за ступенями окиснення хімічних елементів 1. Записуємо символи хімічних елементів у
- 10. Завдання 1 Скласти формули сполук: Брому(+7) і Оксигену; Мангану(+2) і Брому; Кальцію і Хлору; Фосфору(-3) і
- 11. Завдання 2 Сульфур утворює хімічні зв'язки з Калієм, Гідрогеном (ступінь окиснення S --2), Оксигеном (ступінь окиснення
- 12. Завдання 3 «Лови помилку» Виправити помилки у формулах сполук +4 -1 +2 -1 +4 -1 +3
- 13. Завдання 4 Складіть формули бінарних сполук за ступенями окиснення елементів: сульфур флуорид (ступінь окиснення Сульфуру +6);
- 14. Завдання 5 «Чомучка» Чому ступінь окиснення простих речовин дорівнює нулю? Чому один і той же хімічний
- 15. Самостійна робота І варіант Визначити ступені окиснення у сполуках CrCl3, KClO3, BaCl2, Ca (NO3)2, H2CO3, Na2SO4.
- 17. Скачать презентацию












 Теория электролитической диссоциации (ТЭД)
Теория электролитической диссоциации (ТЭД) Катализ и катализаторы
Катализ и катализаторы Объёмная доля компонента смеси
Объёмная доля компонента смеси Задачи
Задачи Вугдеводи. Моносахариди
Вугдеводи. Моносахариди Химия в косметологии
Химия в косметологии Топливо. Виды топлива
Топливо. Виды топлива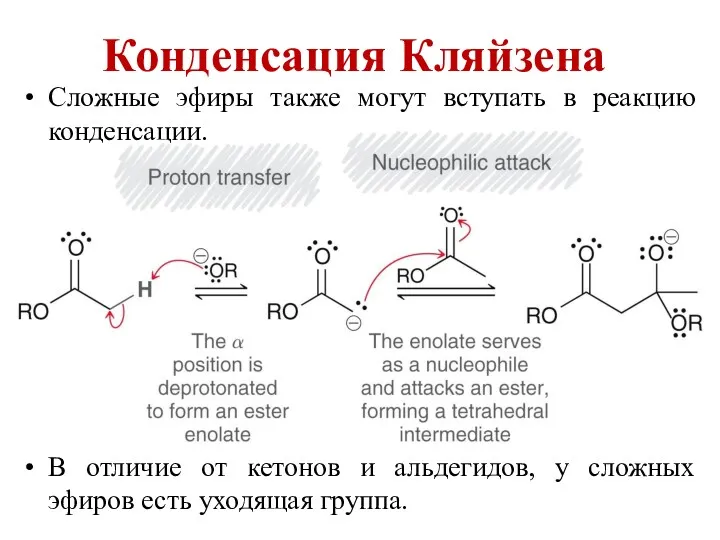 Конденсация Кляйзена
Конденсация Кляйзена Снег и лед. Тайны твердой воды
Снег и лед. Тайны твердой воды Природные источники углеводородов и их переработка
Природные источники углеводородов и их переработка Кислоты, их классификация и свойства
Кислоты, их классификация и свойства Химическая промышленность и химическая технология
Химическая промышленность и химическая технология Характеристика элементов VIIA-группы (галогены)
Характеристика элементов VIIA-группы (галогены) Магний (Mg)
Магний (Mg) Неметаллы
Неметаллы Степени окисления атомов и формулы веществ
Степени окисления атомов и формулы веществ Карбонові кислоти
Карбонові кислоти Алканы: физические и химические свойства, получение
Алканы: физические и химические свойства, получение Водород и щелочные металлы
Водород и щелочные металлы Жиры (триглицериды)
Жиры (триглицериды) Камень чароит
Камень чароит Ионоселективные электроды
Ионоселективные электроды Керамика на основе Al2O3
Керамика на основе Al2O3 Щелочные металлы
Щелочные металлы Строение атома. Периодичность свойств элементов и их соединений
Строение атома. Периодичность свойств элементов и их соединений Химические уравнения. Типы химических реакций. А что такое химическая реакция?
Химические уравнения. Типы химических реакций. А что такое химическая реакция? Химическая термодинамика
Химическая термодинамика Карбоновые кислоты
Карбоновые кислоты