Содержание
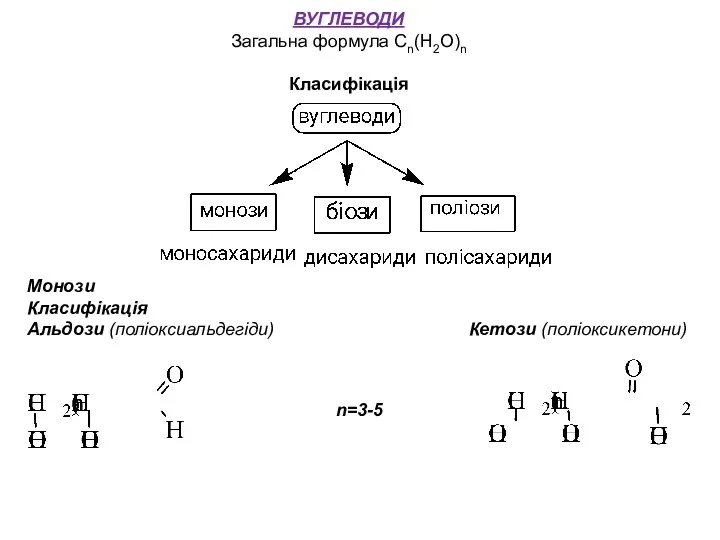
- 2. ВУГЛЕВОДИ Загальна формула Сn(H2O)n Класифікація Монози Класифікація Альдози (поліоксиальдегіди) Кетози (поліоксикетони) n=3-5
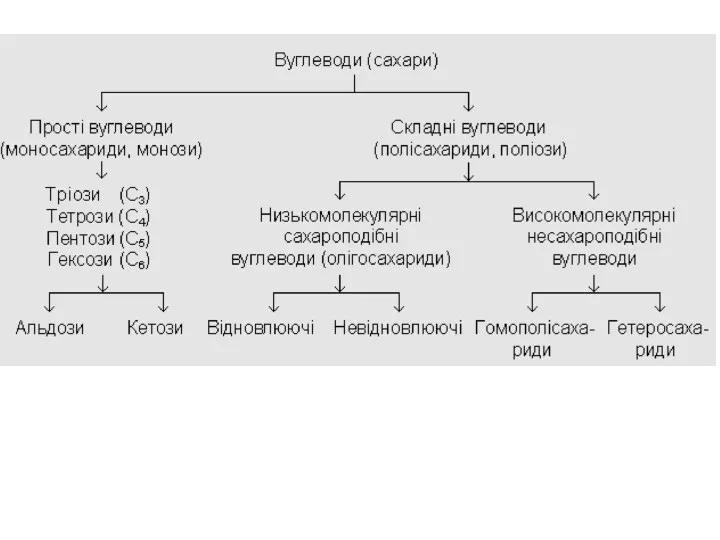
- 3. За числом атомів вуглецю альдози і кетози діляться на триози (три атоми вуглецю), тетрози (чотири атоми
- 4. Низькомолекулярні (сахароподібні) полісахариди містять в молекулі не-велике число залишків моноз (2-10). Вони добре розчиняються у воді,
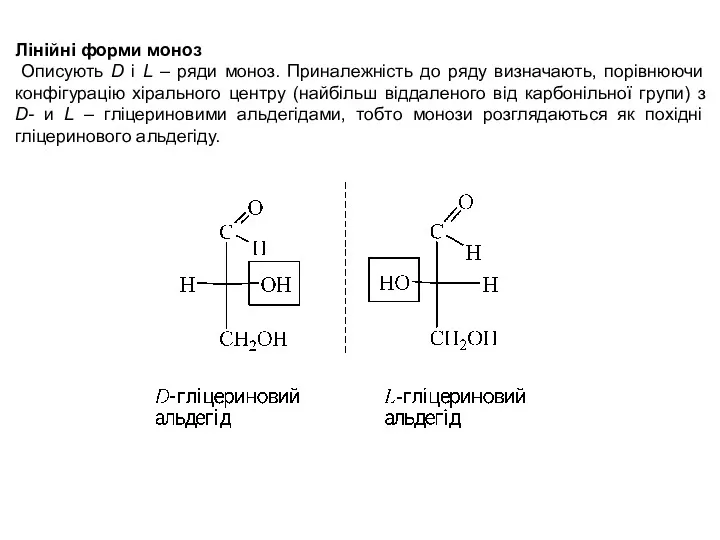
- 5. Лінійні форми моноз Описують D і L – ряди моноз. Приналежність до ряду визначають, порівнюючи конфігурацію
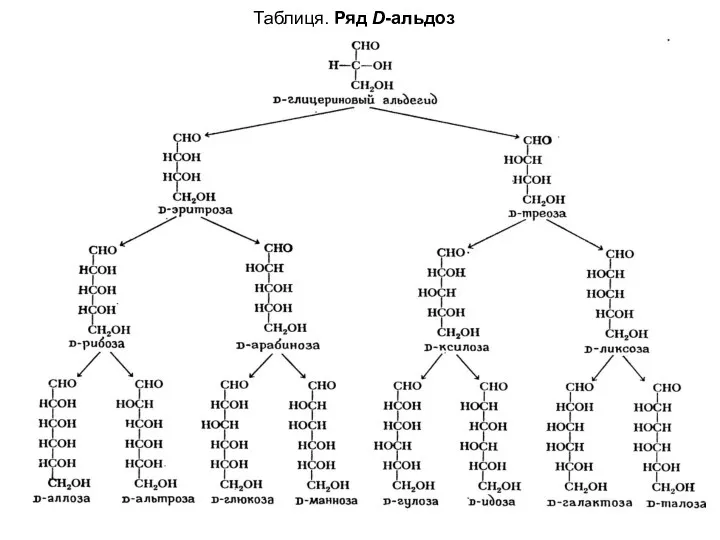
- 6. Таблиця. Ряд D-альдоз
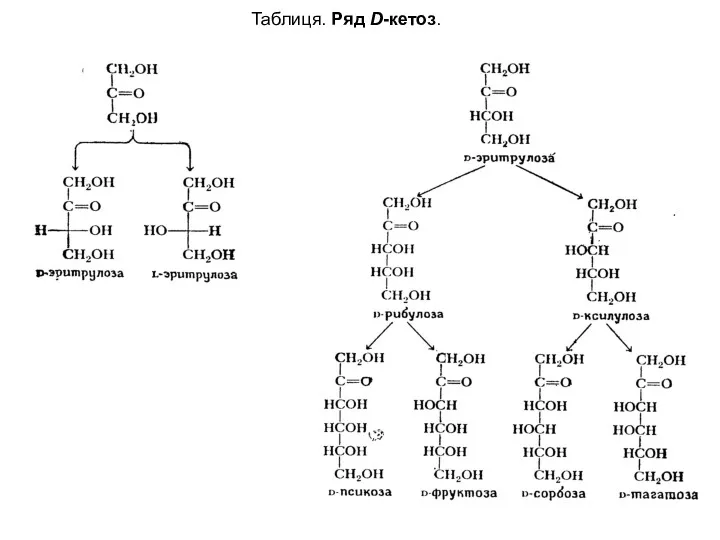
- 7. Таблиця. Ряд D-кетоз.
- 8. Окремі моносахариди звичайно мають тривіальні назви з суфіксом -оза, наприклад, глюкоза, маноза, фруктоза, рибоза. Відповідно до
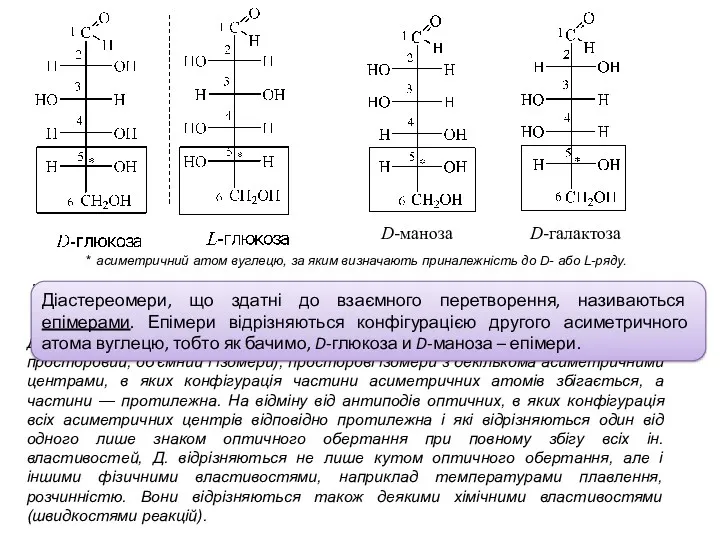
- 9. * асиметричний атом вуглецю, за яким визначають приналежність до D- або L-ряду. Крім D-глюкози, в природі
- 10. Циклічні форми альдогексоз Поліоксиальдегіди (поліоксикетони), що містять 5,6 і 7 атомів вуглецю здатні до внутрішньомолекулярної циклізації.
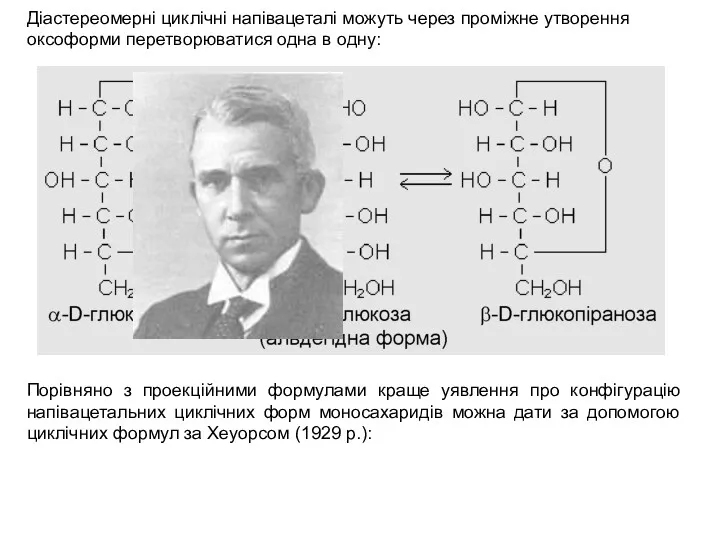
- 12. Діастереомерні циклічні напівацеталі можуть через проміжне утворення оксоформи перетворюватися одна в одну: Порівняно з проекційними формулами
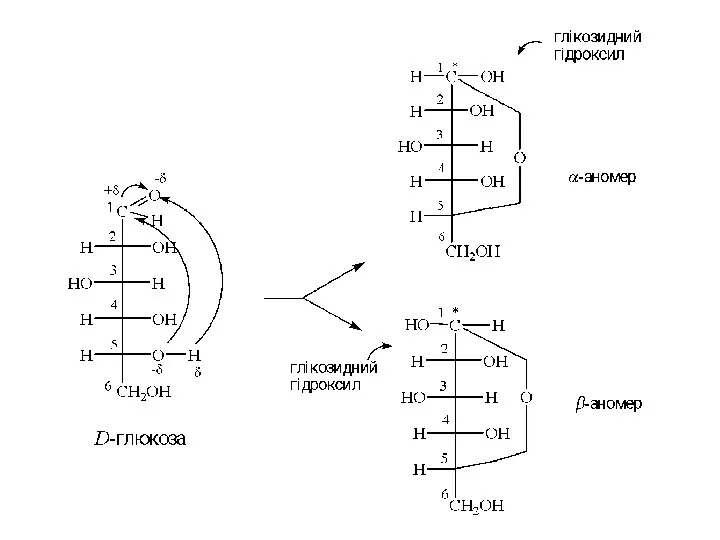
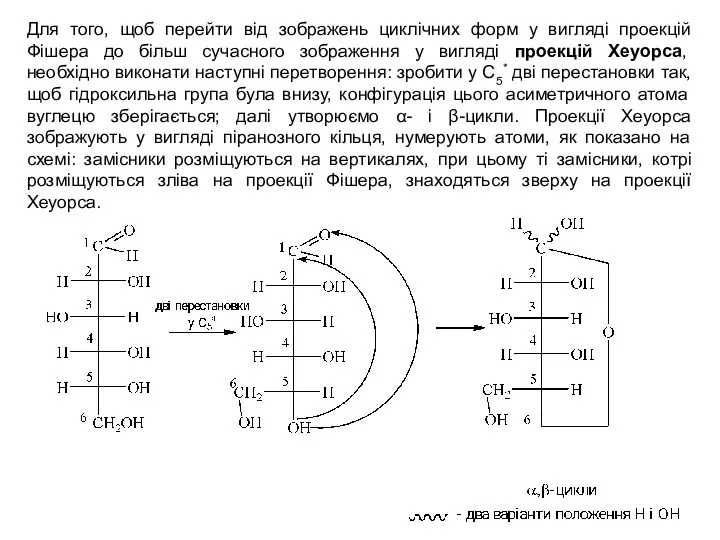
- 13. Для того, щоб перейти від зображень циклічних форм у вигляді проекцій Фішера до більш сучасного зображення
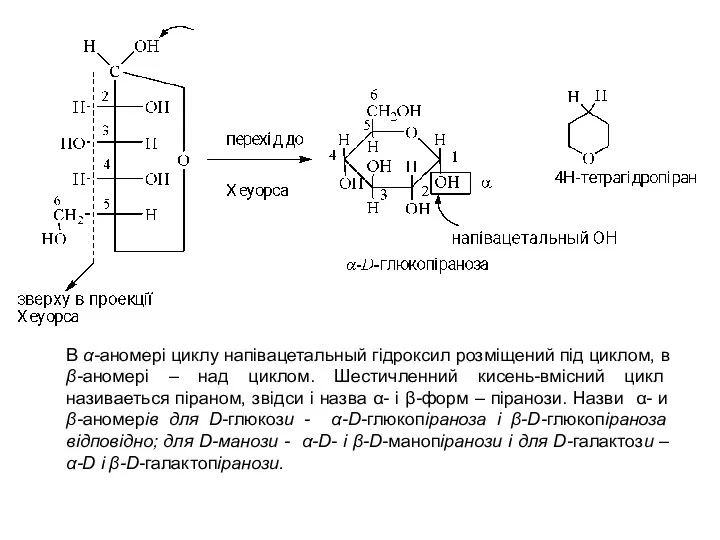
- 14. В α-аномері циклу напівацетальный гідроксил розміщений під циклом, в β-аномері – над циклом. Шестичленний кисень-вмісний цикл
- 15. В α-аномері циклу напівацетальный гідроксил розміщений під циклом, в β-аномері – над циклом. Шестичленний кисень-вмісний цикл
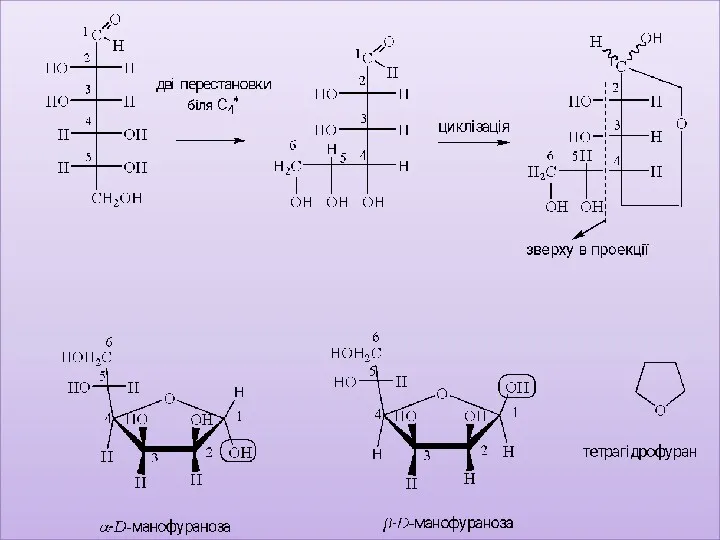
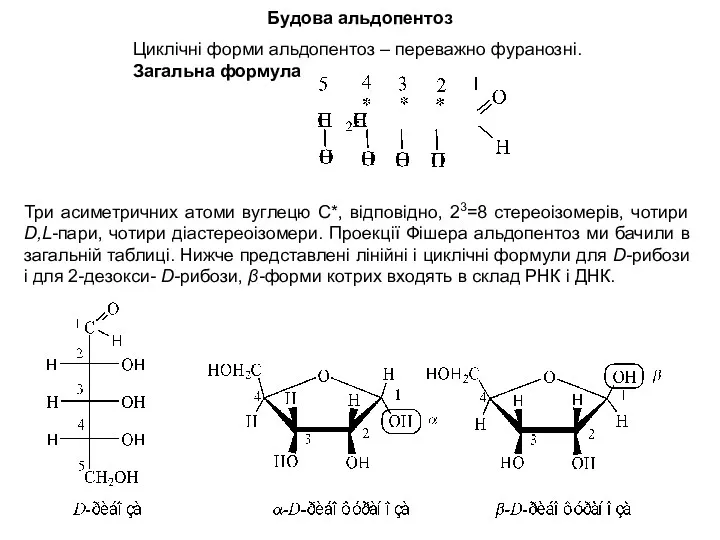
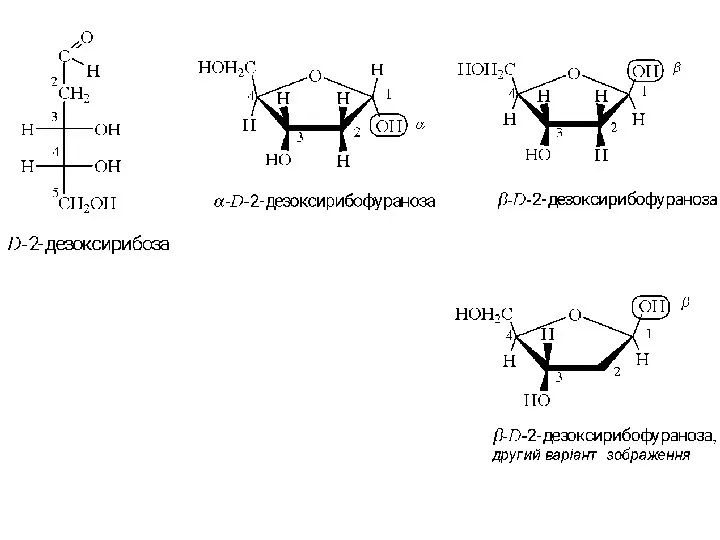
- 16. Три асиметричних атоми вуглецю С*, відповідно, 23=8 стереоізомерів, чотири D,L-пари, чотири діастереоізомери. Проекції Фішера альдопентоз ми
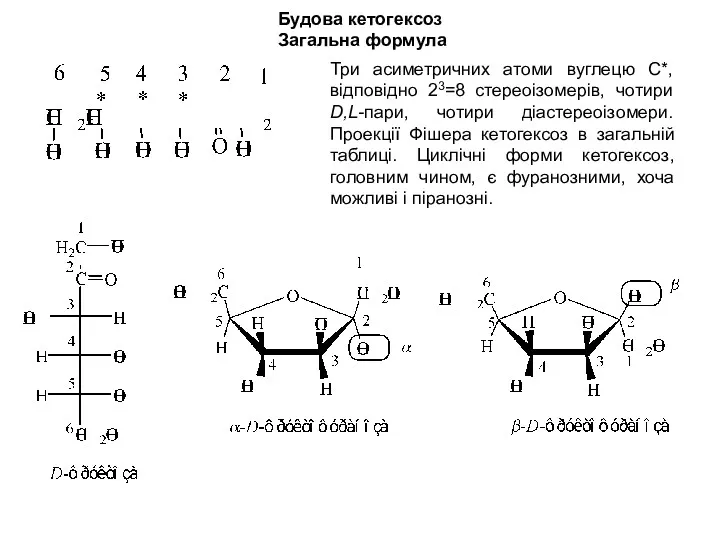
- 18. Будова кетогексоз Загальна формула Три асиметричних атоми вуглецю С*, відповідно 23=8 стереоізомерів, чотири D,L-пари, чотири діастереоізомери.
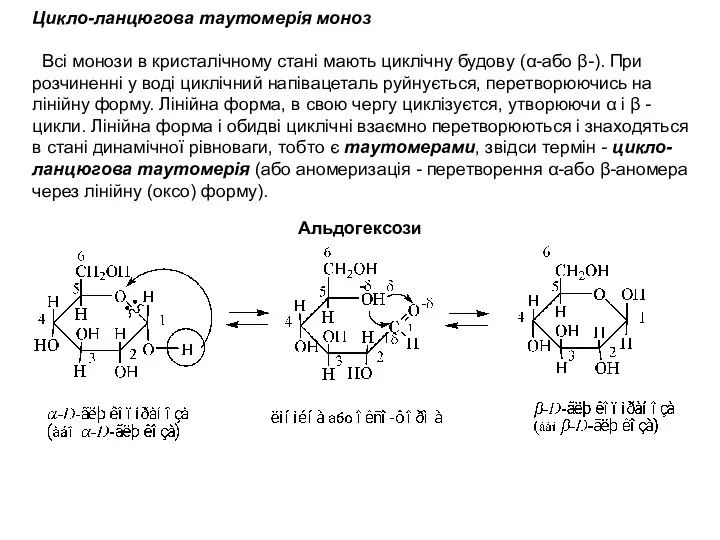
- 19. Цикло-ланцюгова таутомерія моноз Всі монози в кристалічному стані мають циклічну будову (α-або β-). При розчиненні у
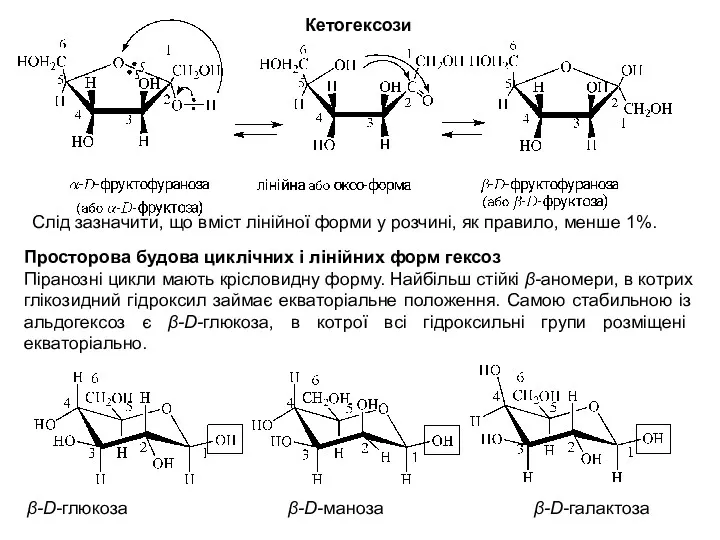
- 20. Кетогексози Слід зазначити, що вміст лінійної форми у розчині, як правило, менше 1%. Просторова будова циклічних
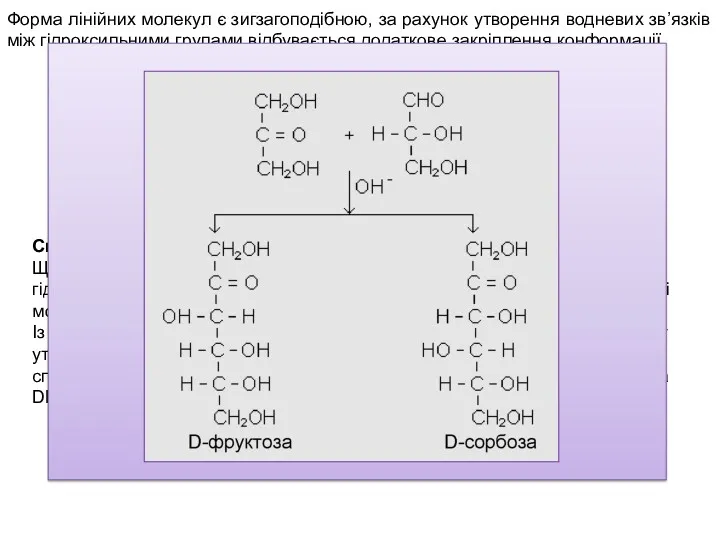
- 21. Форма лінійних молекул є зигзагоподібною, за рахунок утворення водневих зв’язків між гідроксильними групами відбувається додаткове закріплення
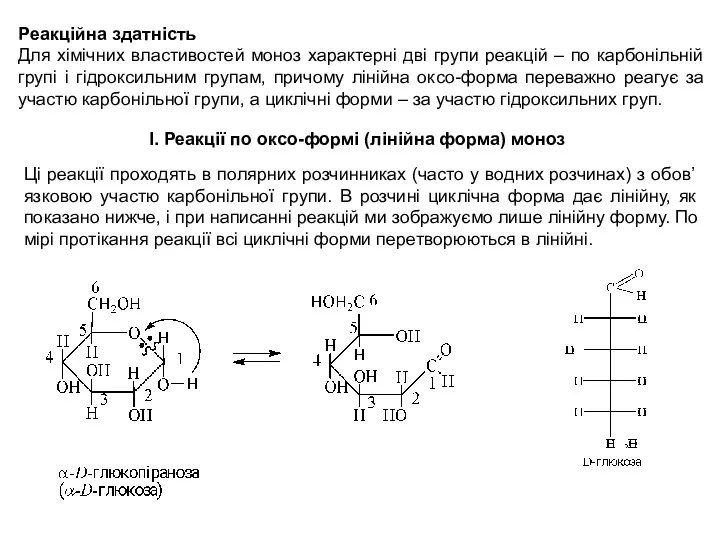
- 22. Реакційна здатність Для хімічних властивостей моноз характерні дві групи реакцій – по карбонільній групі і гідроксильним
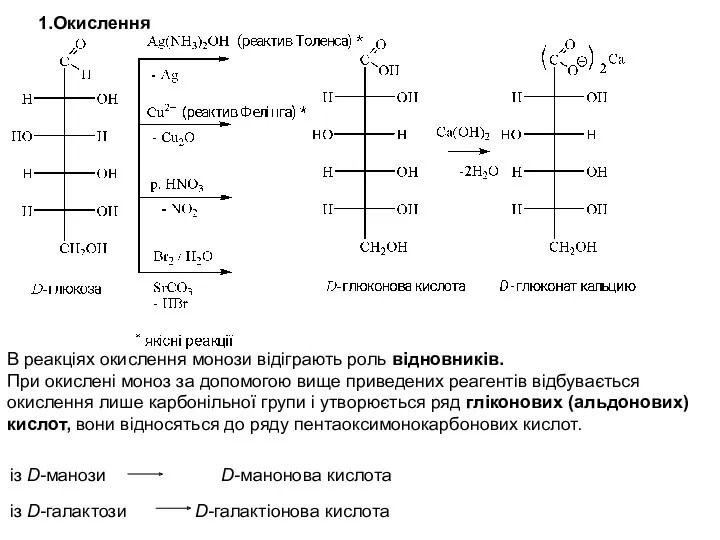
- 23. 1.Окислення В реакціях окислення монози відіграють роль відновників. При окислені моноз за допомогою вище приведених реагентів
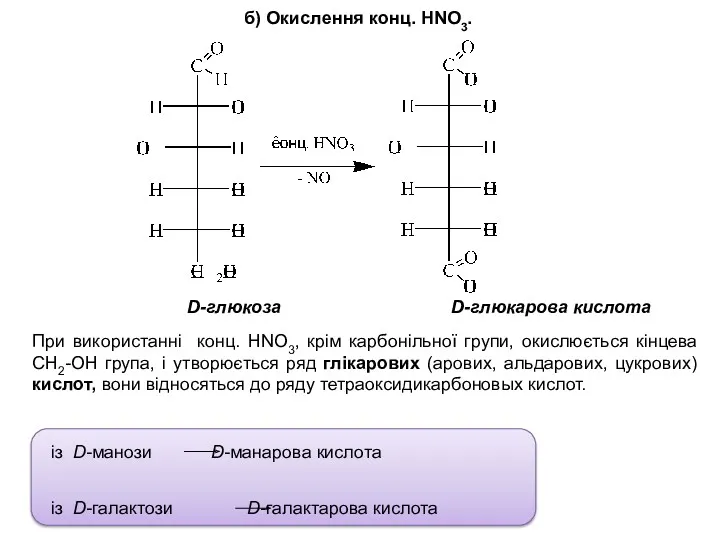
- 24. б) Окислення конц. HNO3. D-глюкоза D-глюкарова кислота При використанні конц. HNO3, крім карбонільної групи, окислюється кінцева
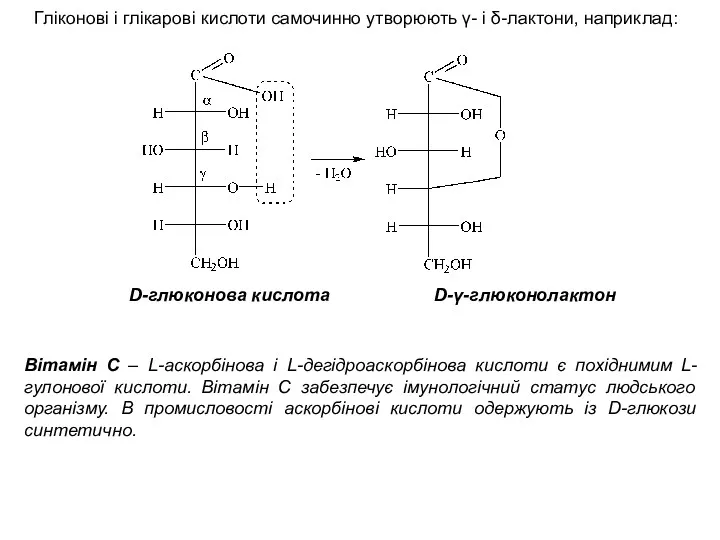
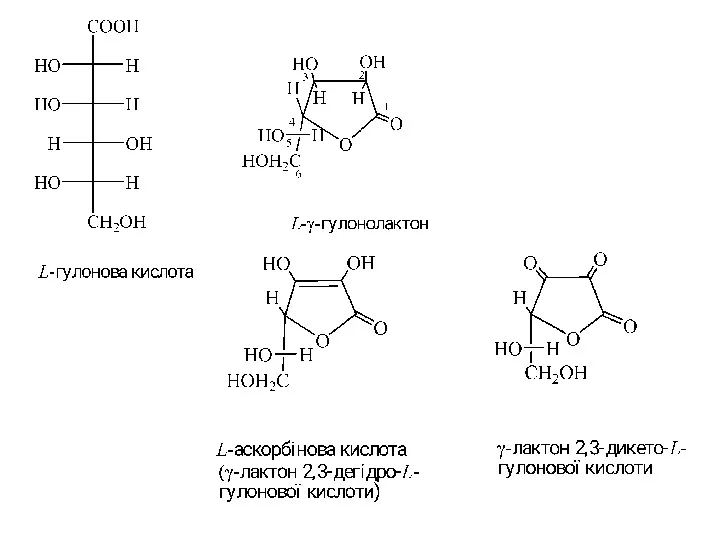
- 25. Гліконові і глікарові кислоти самочинно утворюють γ- і δ-лактони, наприклад: D-глюконова кислота D-γ-глюконолактон Вітамін С –
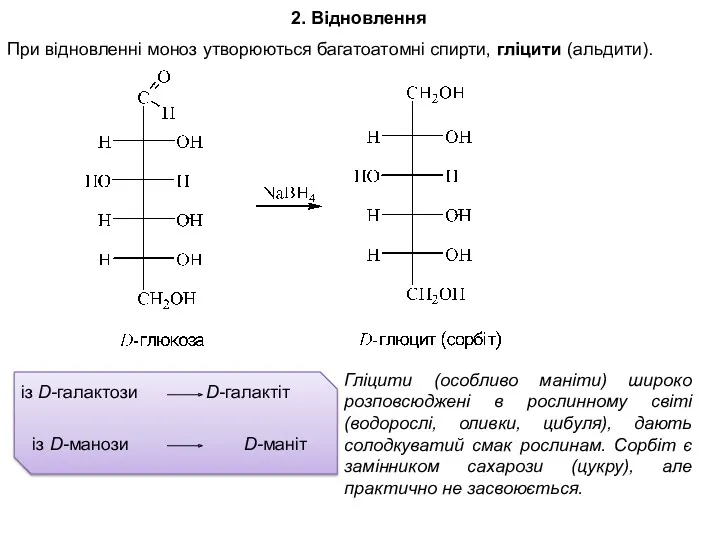
- 27. 2. Відновлення При відновленні моноз утворюються багатоатомні спирти, гліцити (альдити). із D-манози D-маніт із D-галактози D-галактіт
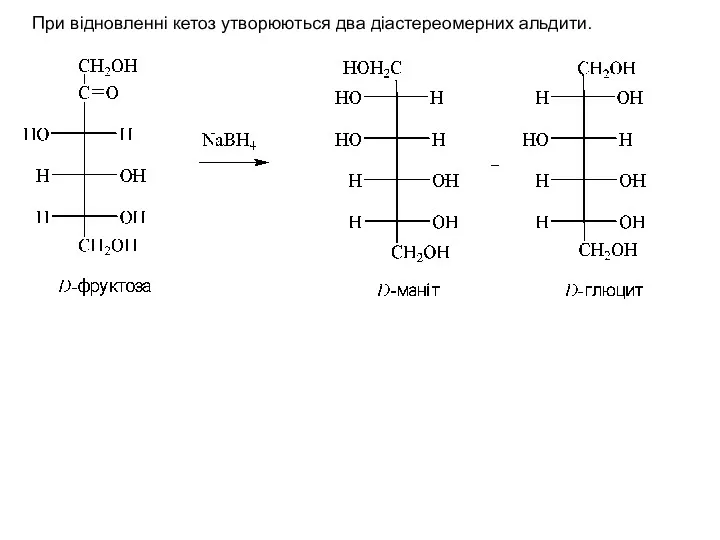
- 28. При відновленні кетоз утворюються два діастереомерних альдити.
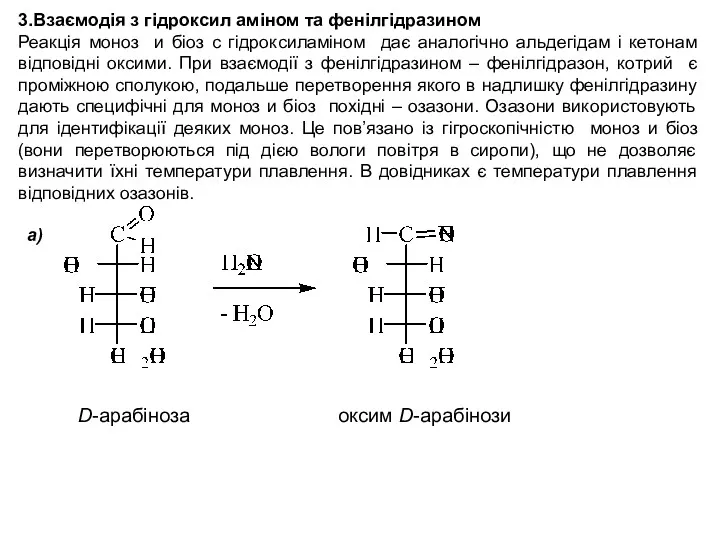
- 29. 3.Взаємодія з гідроксил аміном та фенілгідразином Реакція моноз и біоз с гідроксиламіном дає аналогічно альдегідам і
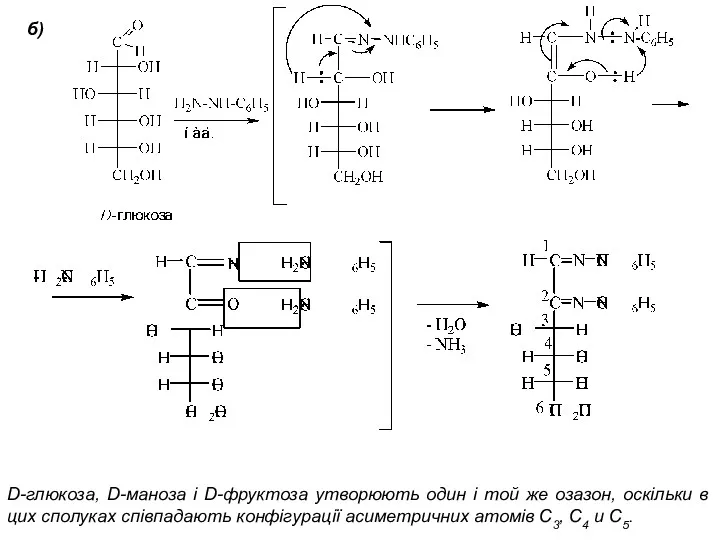
- 30. б) D-глюкоза, D-маноза і D-фруктоза утворюють один і той же озазон, оскільки в цих сполуках співпадають
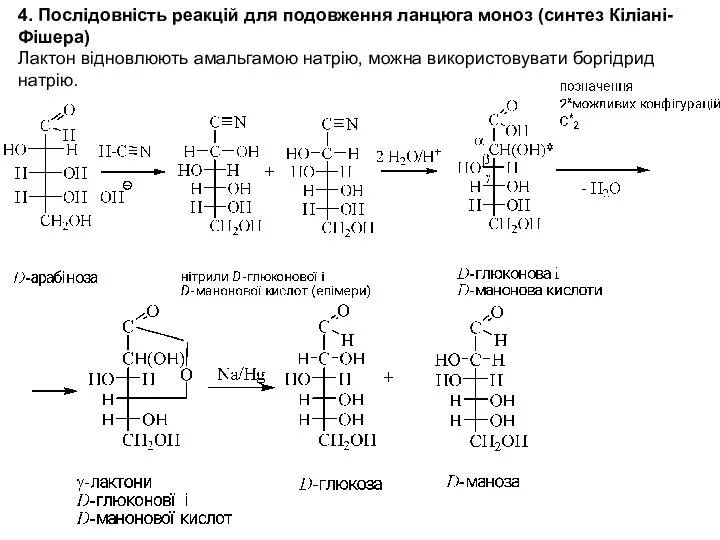
- 31. 4. Послідовність реакцій для подовження ланцюга моноз (синтез Кіліані-Фішера) Лактон відновлюють амальгамою натрію, можна використовувати боргідрид
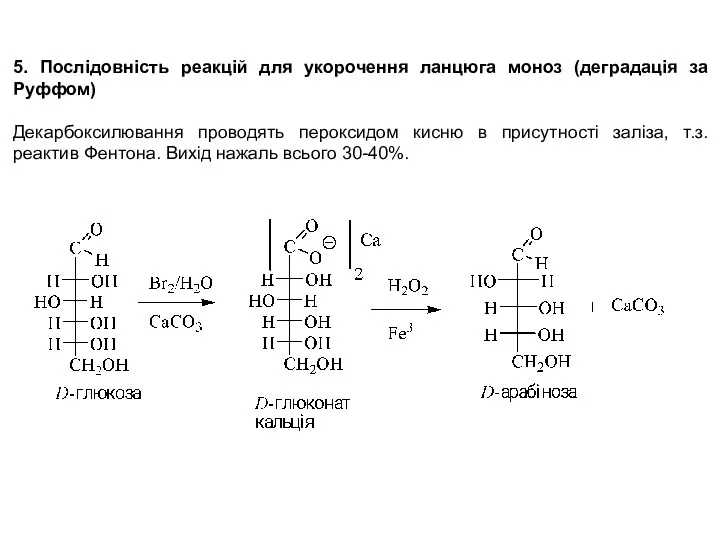
- 32. 5. Послідовність реакцій для укорочення ланцюга моноз (деградація за Руффом) Декарбоксилювання проводять пероксидом кисню в присутності
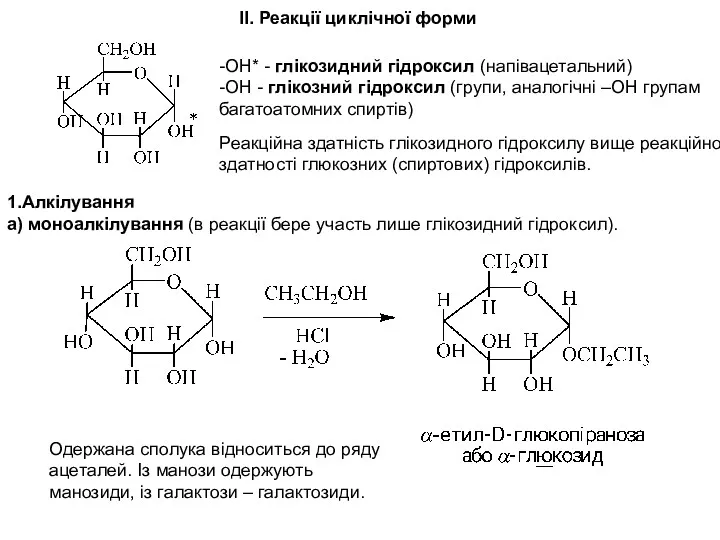
- 33. II. Реакції циклічної форми -ОН* - глікозидний гідроксил (напівацетальний) -ОН - глікозний гідроксил (групи, аналогічні –ОН
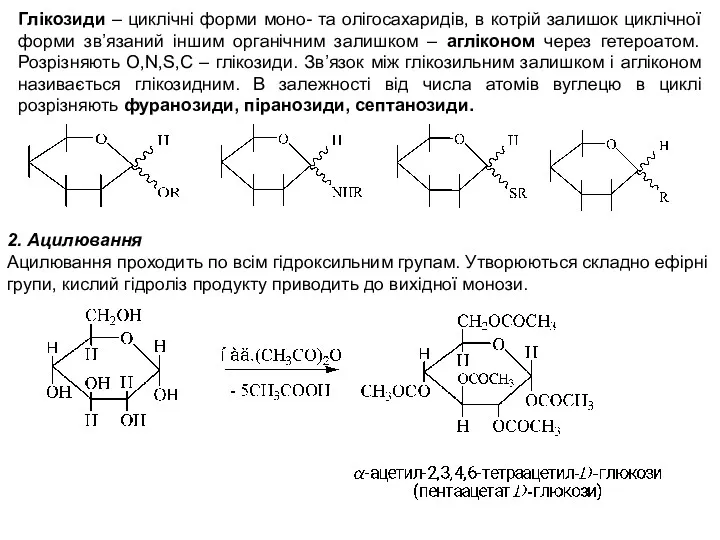
- 34. Глікозиди – циклічні форми моно- та олігосахаридів, в котрій залишок циклічної форми зв’язаний іншим органічним залишком
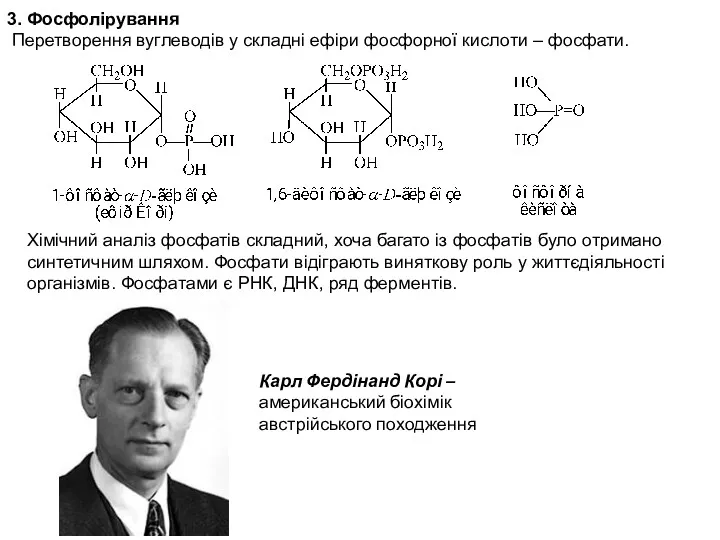
- 35. 3. Фосфолірування Перетворення вуглеводів у складні ефіри фосфорної кислоти – фосфати. Хімічний аналіз фосфатів складний, хоча
- 37. Скачать презентацию



 Крахма́л (C6H10O5)n
Крахма́л (C6H10O5)n Закон сохранения массы. Химические уравнения
Закон сохранения массы. Химические уравнения Химические волокна
Химические волокна Классификация химических реакций
Классификация химических реакций Щелочные металлы
Щелочные металлы Промышленное производство аммиака
Промышленное производство аммиака Л3. Учение о растворах (Химия)
Л3. Учение о растворах (Химия) Биологически важные реакции карбонильных соединений. Масс-спектрометрия
Биологически важные реакции карбонильных соединений. Масс-спектрометрия Что такое химия. Техника безопасности. Интересные факты (урок 1)
Что такое химия. Техника безопасности. Интересные факты (урок 1) Создание косметических средств
Создание косметических средств Химия аминокислот, пептидов и белков
Химия аминокислот, пептидов и белков Натуральные, искуственные и синтетические материалы
Натуральные, искуственные и синтетические материалы АЛКАНЫ 9 класс
АЛКАНЫ 9 класс Оксиды. Классификация. Химические и физические свойства
Оксиды. Классификация. Химические и физические свойства Калийные Удобрения
Калийные Удобрения Актуальные вопросы содержания контрольных измерительных материалов ЕГЭ в 2019 г
Актуальные вопросы содержания контрольных измерительных материалов ЕГЭ в 2019 г Сплави алюмінію. Характеристики та застосування
Сплави алюмінію. Характеристики та застосування Structural, substructural properties and chemical composition
Structural, substructural properties and chemical composition Количество вещества. Моль
Количество вещества. Моль Общая характеристика углеводов: глюкоза
Общая характеристика углеводов: глюкоза Комплексные соединения и лигандообменные равновесия
Комплексные соединения и лигандообменные равновесия Галогены. Общая характеристика галогенов
Галогены. Общая характеристика галогенов Аммиак
Аммиак Технология переработки полимеров
Технология переработки полимеров Тепловой эффект химических реакций. Расчёты по термохимическим уравнениям (ТХУ)
Тепловой эффект химических реакций. Расчёты по термохимическим уравнениям (ТХУ) Алюминий и его соединения
Алюминий и его соединения Периодический закон Д.И. Менделеева. Периодическая система химических элементов
Периодический закон Д.И. Менделеева. Периодическая система химических элементов Непредельные углеводороды. Алкены
Непредельные углеводороды. Алкены