Содержание
- 2. Аналитическая химия - 1 Жидкостная хроматография В зависимости от: диаметра и длины колонки размера частиц сорбента
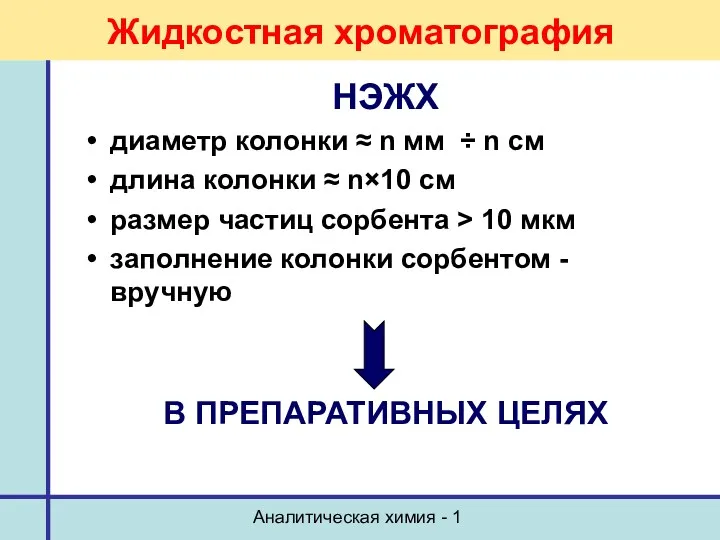
- 3. Аналитическая химия - 1 НЭЖХ диаметр колонки ≈ n мм ÷ n см длина колонки ≈
- 4. Аналитическая химия - 1 ВЭЖХ Изократическая Градиентная Мультиколоночная Многоколоночная Микроколоночная Капиллярная В АНАЛИТИЧЕСКИХ ЦЕЛЯХ
- 5. Аналитическая химия - 1 Отличие ВЭЖХ от ГХ В ГХ газ-носитель не сорбируется неподвижной фазой, а
- 6. Аналитическая химия - 1 Особенности ВЭЖХ Параметры удерживания и селективность в ГХ зависят только от НФ,
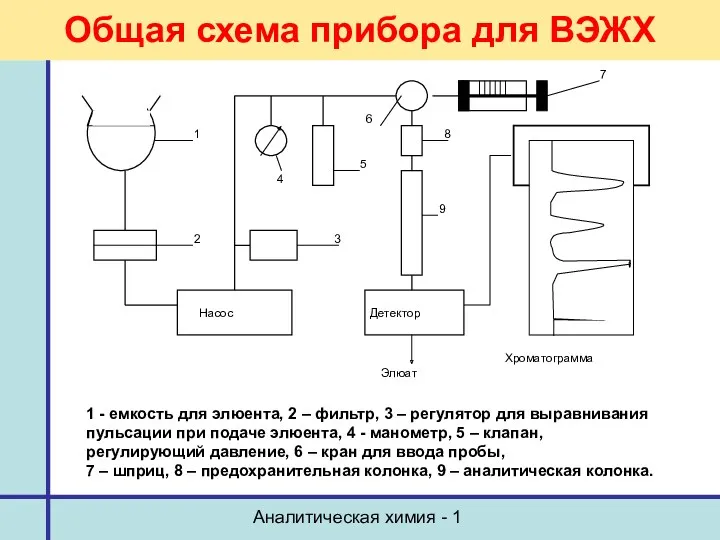
- 7. Аналитическая химия - 1 Общая схема прибора для ВЭЖХ 1 - емкость для элюента, 2 –
- 8. Аналитическая химия - 1 Колонки Предохранительная колонка - короткая, защищает аналитическую колонку от пыли, смол и
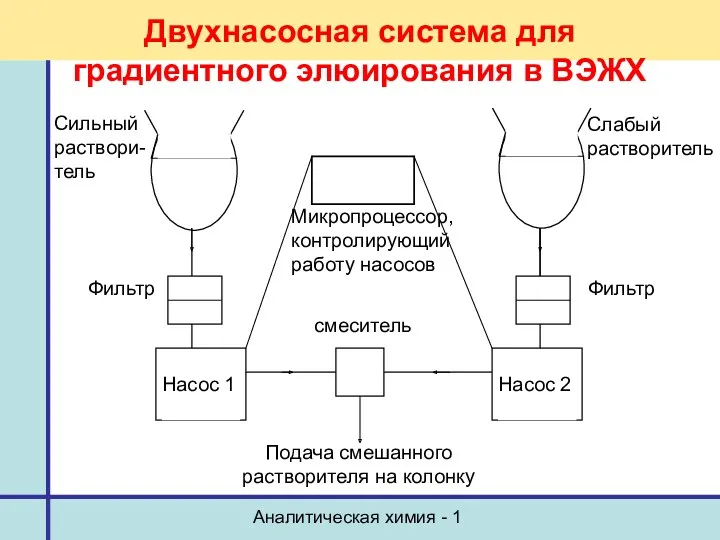
- 9. Аналитическая химия - 1 Двухнасосная система для градиентного элюирования в ВЭЖХ
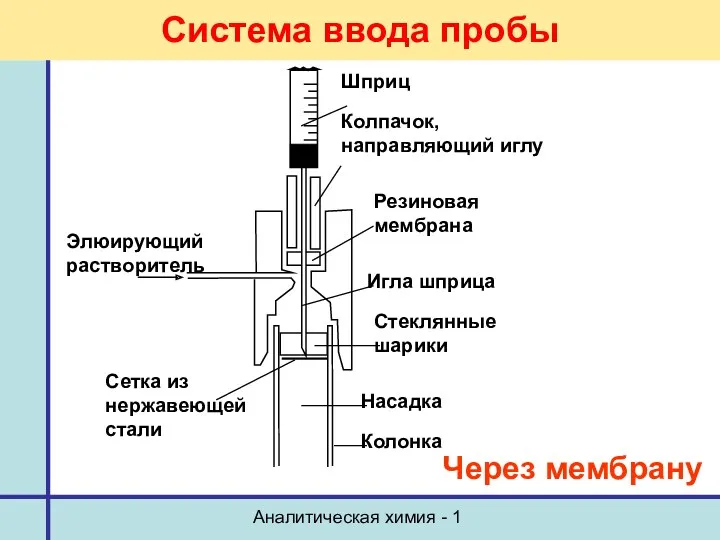
- 10. Аналитическая химия - 1 Система ввода пробы Через мембрану
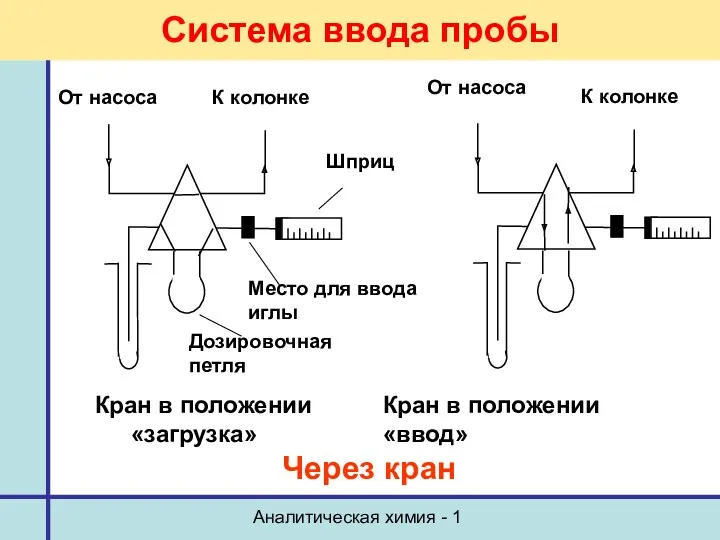
- 11. Аналитическая химия - 1 Система ввода пробы Через кран Кран в положении Кран в положении «загрузка»
- 12. Аналитическая химия - 1 Детекторы УФ (254 нм) Альдегиды, кетоны, ароматические соединения. Требования к элюенту: прозрачность
- 13. Аналитическая химия - 1 Детекторы Дифференциальный рефрактометр ПО 10-6 г, диапазон линейности ~4 порядка концентрации. Предельные
- 14. Аналитическая химия - 1 Детекторы СФМ (190-650 нм) Поглощение при постоянной длине волны во времени или
- 15. Аналитическая химия - 1 Качественный анализ Построение зависимости tR1 – tR2 или lgtR1 – lgtR2, где
- 16. Аналитическая химия - 1 Адсорбционная - ЖТХ Для разделения неионных соединений – от умеренно неполярных до
- 17. Аналитическая химия - 1 Сорбенты (НФ) Сорбенты правильной сферической формы с узким распределением по размерам (3±0.5,
- 18. Аналитическая химия - 1 Требования к ПФ Чистота Химическая инертность Совместимость с детектором Оптимальная вязкость Безопасность
- 19. Аналитическая химия - 1 Элюенты (ПФ) Элюотропный ряд – расположение растворителей в соответствии с возрастанием их
- 20. Аналитическая химия - 1 Элюенты (ПФ) В нормально-фазовой хроматографии стандарт – пентан, для него ɛо =
- 21. Аналитическая химия - 1 Элюенты (ПФ) Элюотропный ряд зависит от полярности сорбента, т.е. вида хроматографии В
- 22. Аналитическая химия - 1 Распределительная - ЖЖХ Распределение вещества между двумя несмешивающимися жидкостями, разделение - за
- 23. Аналитическая химия - 1 Ионообменная хроматография Динамический процесс замещения ионов, связанных с НФ, ионами элюента. Соотношение
- 24. Аналитическая химия - 1 Ионообменная хроматография Ионообменники при погружении в раствор электролита поглощают из него катионы
- 25. Аналитическая химия - 1 Ионообменная хроматография Катионообменники содержат кислотные группы: -SO3H, -COOH, -OH, -PO3H2, -AsO3H2. Анионообменники
- 26. Аналитическая химия - 1 Ионообменная хроматография Катионообменная реакция: R-H + Na+ ↔ R-Na + H+ Анионообменная
- 27. Аналитическая химия - 1 Ионообменная хроматография Набухание ионообменника в воде Набухание зависит от: - количества гидрофильных
- 28. Аналитическая химия - 1 Ионы удерживаются тем сильнее, чем больше их заряд и размер. Элюирующая способность
- 29. Аналитическая химия - 1 Детекторы Кондуктометрический детектор - измерение электропроводности элюата. Для снижения фоновой электропроводности после
- 30. Аналитическая химия - 1 Детекторы Спектрофотометрический Люминесцентный Полярографический
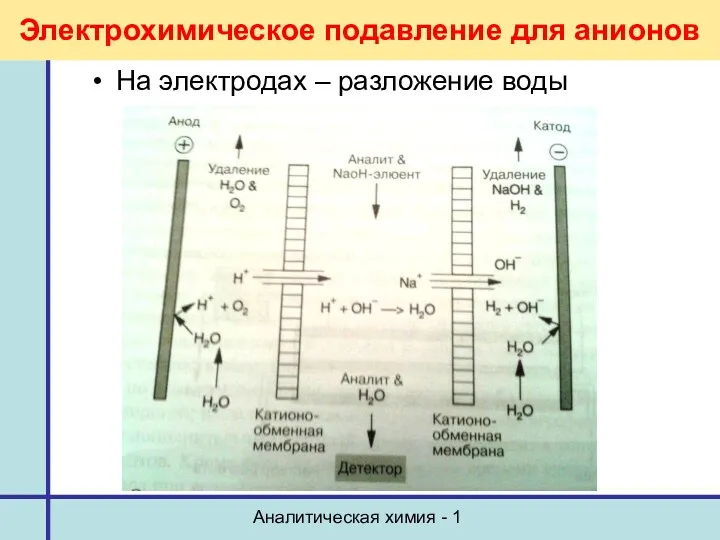
- 31. Аналитическая химия - 1 Электрохимическое подавление для анионов На электродах – разложение воды
- 33. Скачать презентацию






















 Типы химических реакций на примере свойств воды
Типы химических реакций на примере свойств воды Chemical Formulas and Nomenclature of compounds
Chemical Formulas and Nomenclature of compounds Вода - розчинник. Урок 41
Вода - розчинник. Урок 41 Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Внеклассное мероприятие по химии. 9 класс
Внеклассное мероприятие по химии. 9 класс Электронная природа химической связи. Кристаллические и аморфные вещества
Электронная природа химической связи. Кристаллические и аморфные вещества Своя игра Знаешь ли ты химические элементы?
Своя игра Знаешь ли ты химические элементы? Строение и свойства циклоалканов.
Строение и свойства циклоалканов. Горение жидкого топлива
Горение жидкого топлива Химическая связь
Химическая связь Комплексиметрическое титрование
Комплексиметрическое титрование Органическая химия. Лекция - Гидроксикислоты
Органическая химия. Лекция - Гидроксикислоты Топливо. Загрязнения воздуха, способы его предотвращения. Химия. 8 класс
Топливо. Загрязнения воздуха, способы его предотвращения. Химия. 8 класс Физические и химические свойства алканов
Физические и химические свойства алканов Ионные уравнения реакций
Ионные уравнения реакций Практическое занятие по основам биохимии с методами клинико-биохимических исследований
Практическое занятие по основам биохимии с методами клинико-биохимических исследований Вода. Растворимость, растворы
Вода. Растворимость, растворы Глоссарий
Глоссарий Кислоты в свете ТЭД
Кислоты в свете ТЭД Хімічний склад жувальної гумки
Хімічний склад жувальної гумки драгоценные и поделочные
драгоценные и поделочные Металлы в природе. Общие способы их получения
Металлы в природе. Общие способы их получения Свойства минералов
Свойства минералов Интересные свойства редких металлов
Интересные свойства редких металлов Вторичная переработка нефти. Лекция 9
Вторичная переработка нефти. Лекция 9 Золь-гель технология. Прорыв XXI века
Золь-гель технология. Прорыв XXI века Introduction to effective permeability and relative permeability
Introduction to effective permeability and relative permeability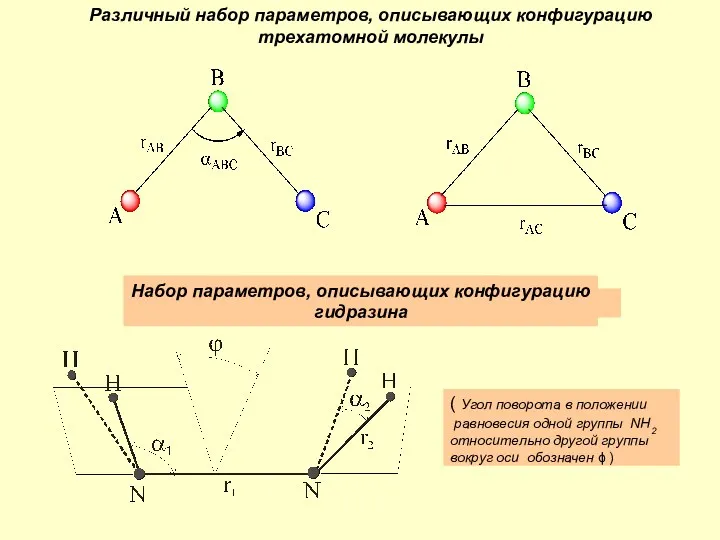 Различный набор параметров, описывающих конфигурацию трехатомной молекулы
Различный набор параметров, описывающих конфигурацию трехатомной молекулы