Содержание
- 2. Властивості хімічних елементів, простих речовин, а також склад і властивості сполук перебувають у періодичній залежності від
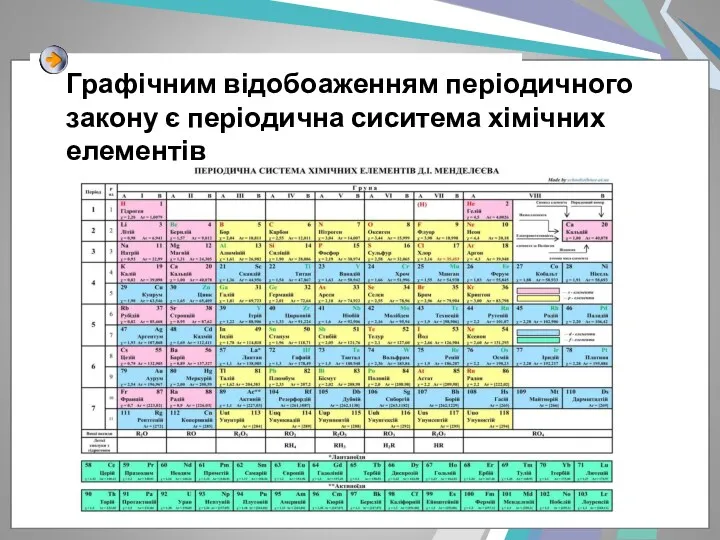
- 3. Графічним відобоаженням періодичного закону є періодична сиситема хімічних елементів
- 4. Минуло більш як 150 років, але періодичний закон та періодична система з успіхом застосовується і донині.
- 5. Періодичний закон – один із найфундаментальніших законів природи. Йому підпорядковані всі хімічні елементи всесвіту. А оскільки
- 6. Пропоную вам таку гру: я читаю вірш, а ви, там де я зупиняюся, вставляєте потрібне слово,
- 8. Елементи струнко в ряд, Мов солдатики стоять. Ось періоди, їх…… сім- Неоднакові усі: Є … великі,
- 9. Груп в таблиці є октет- Вертикальний силует. В них підгрупи підопічні , Є і …. головні
- 10. Ось родина в першій групі Є у головній підгрупі. Це метали надактивні, Інколи аж дуже дивні.
- 11. В сьомій групі - …. галогени, Ніби спрвжні джентельмени. Люблять завжди в парі бути - Це
- 13. Що за горді,наче ружі, І до всіх завжди байдужі Елементи в восьмій групі Є у головній
- 14. Дві сім'ї є тут чималі, Місця стало їм замало- Гуртожитки збудували, Спільні прізвища обрали. Звуть їх
- 15. Ось така в нас є структура- Справжня абревіатура. Кожна клітка - чиєсь житло, Інформацію всю спритно
- 16. Про ядро і електрони, Про заряд його, протони, Що за вигляд атом має, Що у нім
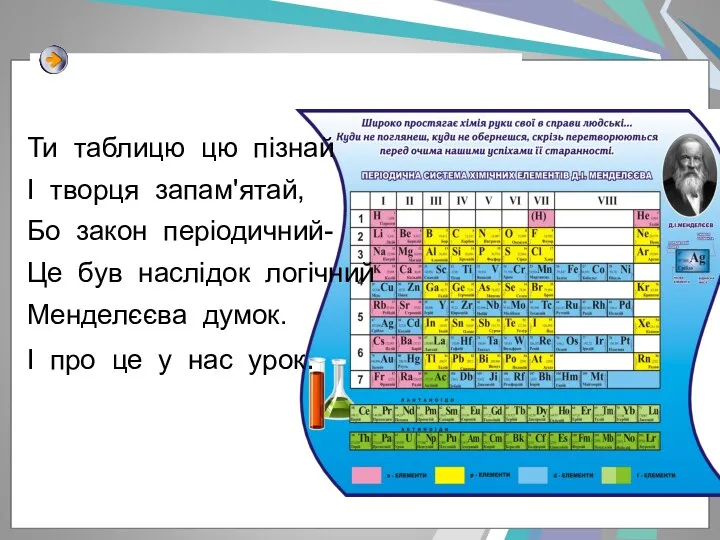
- 17. Ти таблицю цю пізнай І творця запам'ятай, Бо закон періодичний- Це був наслідок логічний Менделєєва думок.
- 18. Наукове значення періодичного закону Періодичний закон Д.І. Менделєєва один із основних і найзагальніших законів природи, закон,
- 19. Періодичний закон Д.І. Менделєєва дав можливість пояснювати явища, в яких беруть участь хімічні елементи, та передбачати
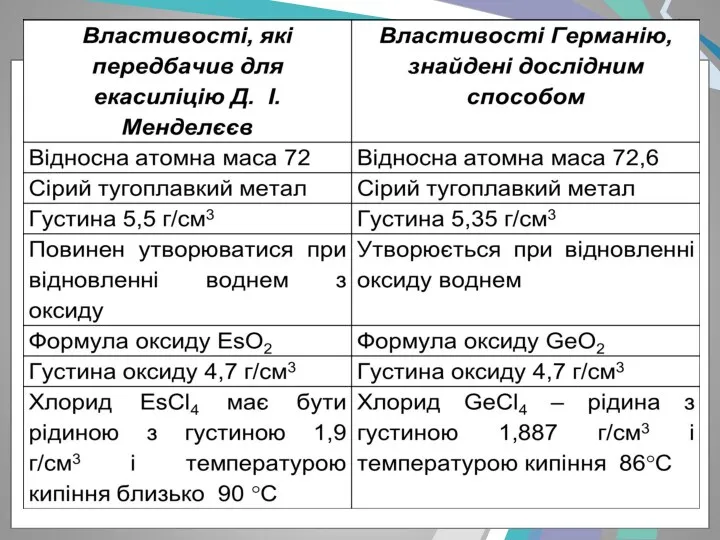
- 20. - Д. І. Менделєєв дуже докладно описав властивості трьох ще не відкритих елементів і назвав їх
- 22. На основі періодичного закону і періодичної системи вбуло виправлено відносні атомні маси багатьох елементів ( берилію,
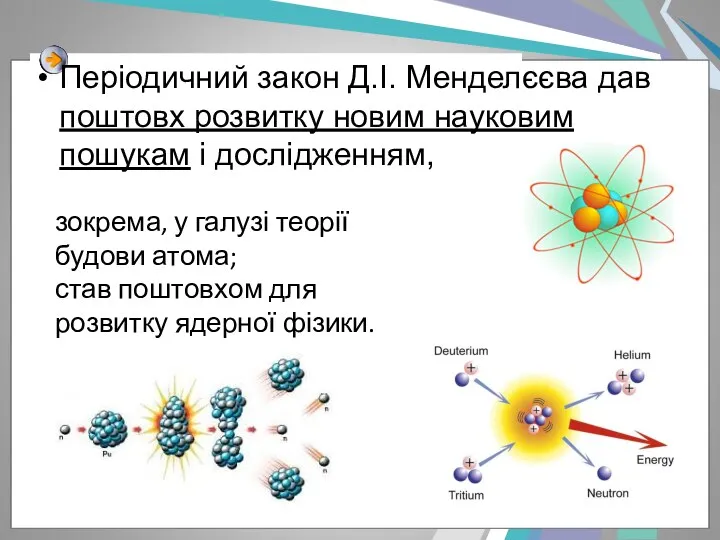
- 23. Періодичний закон Д.І. Менделєєва дав поштовх розвитку новим науковим пошукам і дослідженням, зокрема, у галузі теорії
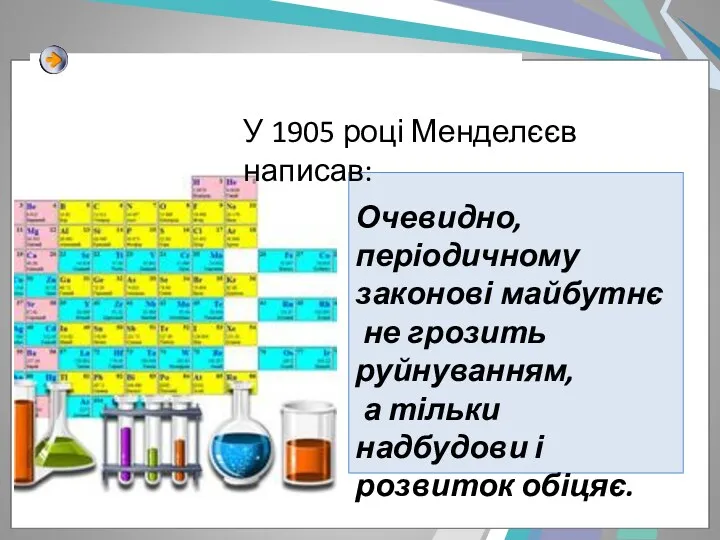
- 24. Очевидно, періодичному законові майбутнє не грозить руйнуванням, а тільки надбудови і розвиток обіцяє. У 1905 році
- 25. Оцінюючи велич діянь Д.І. Менделєєва, видатні вчені недарма називали періодичний закон «компасом» (Рамсей В.), «яскравим маяком»
- 26. Д.І.Менделєєв був найбільш визнаним у світі ученим – він мав понад ста почесних звань, зокрема був
- 27. Перевірте свої знання: 1. Виберіть сучасне формулювання Періодичного закону А Властивості хімічних елементів і утворених ними
- 28. 2. Укажіть порядковий номер хімічного елемента Е, який належить до ІІІ періоду періодичної системи й утворює
- 29. 3. У якій групі періодичної системи (коротка форма) містяться лише металічні елементи? А ІІ. Б ІV.
- 30. 4. У періодичній системі хімічних елементів Карбон і Титан належать до: А одного періоду Б однієї
- 31. 5. Флуор, Хлор, Бром належать до: А f-елементів, Б d-елементів, В p-елементів, Г s-елементів
- 32. 6. Як розташовані хімічні елементи в періодичній системі Д. І. Менделєєва? А кожний період закінчується металічним
- 33. 7. Як змінюється склад електронної оболонки атомів хімічних елементів 3-го періоду періодичної системи Д.І. Менделєєва зі
- 34. 8. Укажіть символи хімічних елементів однієї підгрупи періодичної системи Д.І. Менделєєва. А K, Cu, Rb. Б
- 35. 9. Розташуйте хімічні елементи за зменшенням радіусів атомів. А Аl. Б Si. В С . Г
- 36. 10. Чому Сульфур і Хром розташовано в одній групі періодичної системи елементів Д.І. Менделєєва А атоми
- 37. 11. На підставі періодичного закону було виправлено: А) порядкові номери хімічних елементів; Б) назви хімічних елементів;
- 38. Хімічні елементи у періодичній системі розміщені у порядку зростання: А) радіусу атома Б) відносних атомних мас;
- 40. Скачать презентацию
































 Аллотропия
Аллотропия Основные классы неорганических соединений
Основные классы неорганических соединений Нуклеиновые кислоты. Нуклеотиды
Нуклеиновые кислоты. Нуклеотиды Тяжелые металлы. Опасность токсичных металлов для организма
Тяжелые металлы. Опасность токсичных металлов для организма Основные синтетические полимеры
Основные синтетические полимеры Кислотные дожди
Кислотные дожди Механизмы трансформации энергии в фотосинтезе
Механизмы трансформации энергии в фотосинтезе 20230330_zakony_termodinamiki_i_kinetika
20230330_zakony_termodinamiki_i_kinetika S-элементтердің жалпы сипаттамасы
S-элементтердің жалпы сипаттамасы 20230219_prezentatsiya_k_uroku_neft
20230219_prezentatsiya_k_uroku_neft Общая характеристика элементов главной подгруппы второй группы
Общая характеристика элементов главной подгруппы второй группы Розв’язування задач на приготування розчинів із кристалогідратів
Розв’язування задач на приготування розчинів із кристалогідратів Термодинамика растворов неэлектролитов
Термодинамика растворов неэлектролитов Химическое равновесие. Азот и Фосфор. 9 класс
Химическое равновесие. Азот и Фосфор. 9 класс Технология монокристаллов и особо чистых веществ
Технология монокристаллов и особо чистых веществ Оксиды и гидроксиды металлов. 11 класс
Оксиды и гидроксиды металлов. 11 класс Химические реакции или химические явления
Химические реакции или химические явления Почвенный раствор. Химический состав почвенных растворов. Водный режим почв. Кислотность и щелочность почвенных растворов
Почвенный раствор. Химический состав почвенных растворов. Водный режим почв. Кислотность и щелочность почвенных растворов Игровая программа по химии Самый умный. Химические свойства оксидов, оснований, кислот и солей
Игровая программа по химии Самый умный. Химические свойства оксидов, оснований, кислот и солей Факторы и процессы формирования химического состава подземных вод
Факторы и процессы формирования химического состава подземных вод Комплексиметрическое титрование
Комплексиметрическое титрование Электролиз. Классификация
Электролиз. Классификация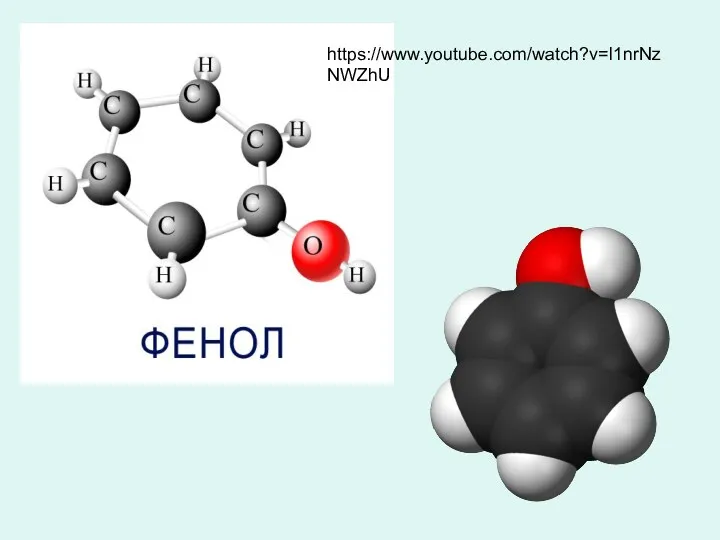 Фенол. Феноловая катастрофа
Фенол. Феноловая катастрофа Составление формул молекулярных простых веществ
Составление формул молекулярных простых веществ Щавелевая кислота
Щавелевая кислота Нанотехнологии и Наноматериалы
Нанотехнологии и Наноматериалы Кислоты. Определение и классификация
Кислоты. Определение и классификация Исследование Е. Е. Вагнера в области терпенов и камфоры
Исследование Е. Е. Вагнера в области терпенов и камфоры