Слайд 2

Белки – носители жизни.
Из них состоят все животные и растительные
организмы.
В человеческом организме около 100.000 разновидностей белков, отличающихся по строению, составу и свойствам.
В крови человека примерно 300 разных белков
В белке куриного яйца содержится 5 индивидуальных белков
Слайд 3

Содержание белков
(в % к сухой массе)
Мышцы человека
Кожа человека
Печень человека
Мозг человека
Кости
человека
80 %
63 %
57 %
45 %
28 %
Слайд 4

ФУНКЦИИ БЕЛКОВ
ТРАНСПОРТНАЯ (например белок крови гемоглобин переносит кислород ко всем органам)
СТРОИТЕЛЬНАЯ
(«кирпичики» из которых построен животный организм – это белки)
ФЕРМЕНТАТИВНАЯ (в нашем организме происходит десятки тысяч реакций. Идут они благодаря белкам-ферментам)
ЗАЩИТНАЯ (антитела, благодаря которым вырабатывается иммунитет – это белковые вещества)
ГОРМОНАЛЬНАЯ (белками являются и все гормоны: эстроген и тестостерон-половые гормоны, эндорфин и сератонин дают ощущение счастья, мелатонин-гормон сна, адреналин – гормон страха)
И т.д.
Слайд 5
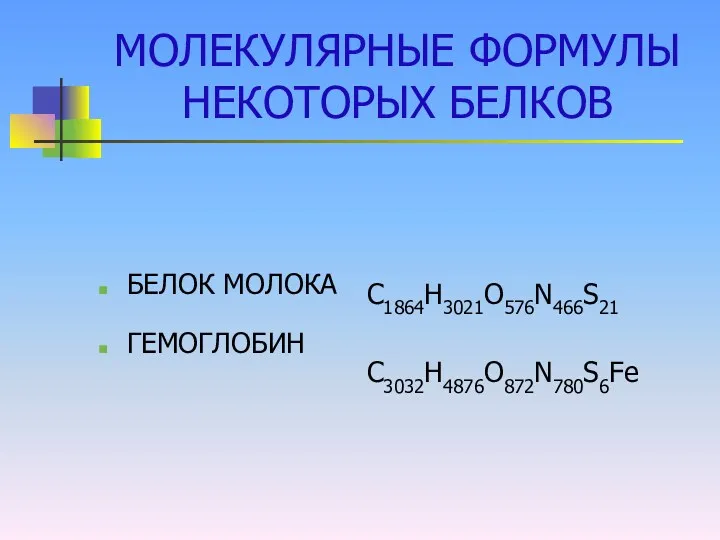
МОЛЕКУЛЯРНЫЕ ФОРМУЛЫ НЕКОТОРЫХ БЕЛКОВ
БЕЛОК МОЛОКА
ГЕМОГЛОБИН
С1864Н3021О576N466S21
С3032Н4876О872N780S6Fe
Слайд 6

Что же такое белки с точки зрения химии?
Белки – полипептиды, природные
полимеры, вещества, состоящие из остатков α-аминокислот.
Слайд 7
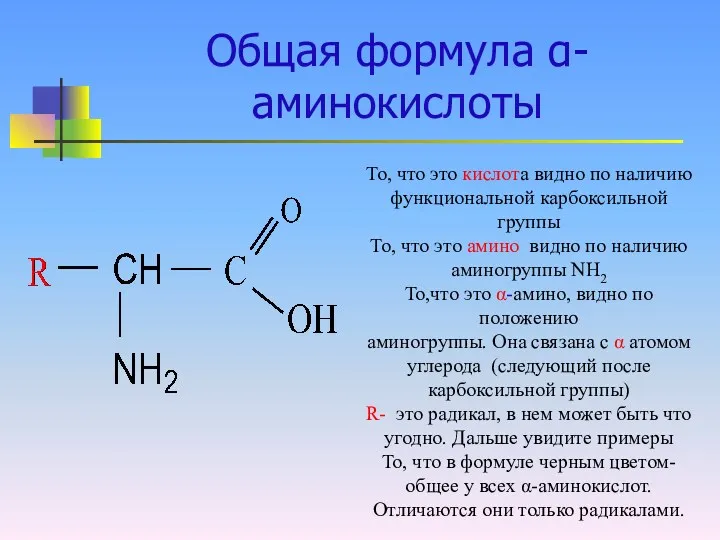
Общая формула α-аминокислоты
То, что это кислота видно по наличию
функциональной карбоксильной группы
То,
что это амино видно по наличию аминогруппы NH2
То,что это α-амино, видно по положению
аминогруппы. Она связана с α атомом углерода (следующий после карбоксильной группы)
R- это радикал, в нем может быть что угодно. Дальше увидите примеры
То, что в формуле черным цветом- общее у всех α-аминокислот. Отличаются они только радикалами.
Слайд 8
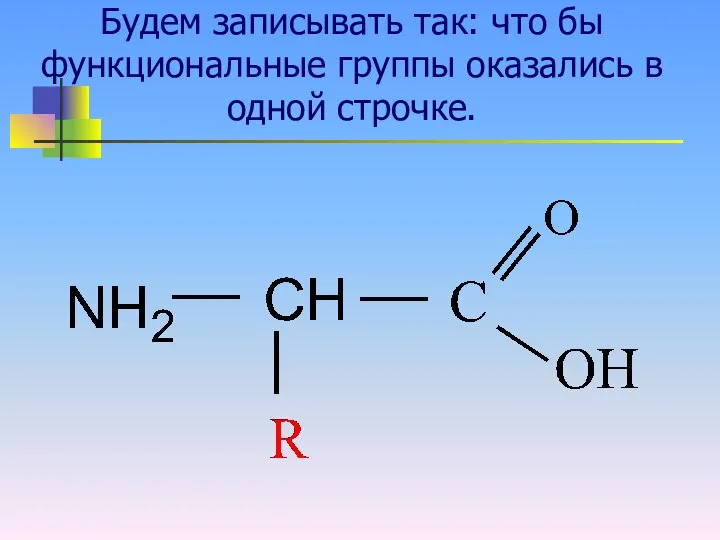
Будем записывать так: что бы функциональные группы оказались в одной строчке.
Слайд 9

В состав белков входят 20 видов
α-аминокислот.
Им всем дали еще
специальные названия.
Например аминоуксусная кислота называется глицин или гли (берут первые 3 буквы)
Ниже я даю формулы 10 α-аминокислот для примера. Себе законспектируйте 4-5
Слайд 10
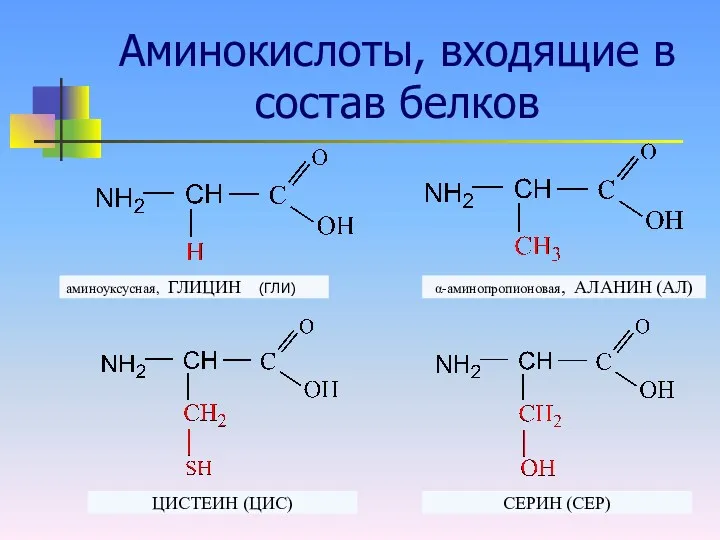
Аминокислоты, входящие в состав белков
аминоуксусная, ГЛИЦИН (ГЛИ)
α-аминопропионовая, АЛАНИН (АЛ)
ЦИСТЕИН (ЦИС)
СЕРИН
(СЕР)
Слайд 11
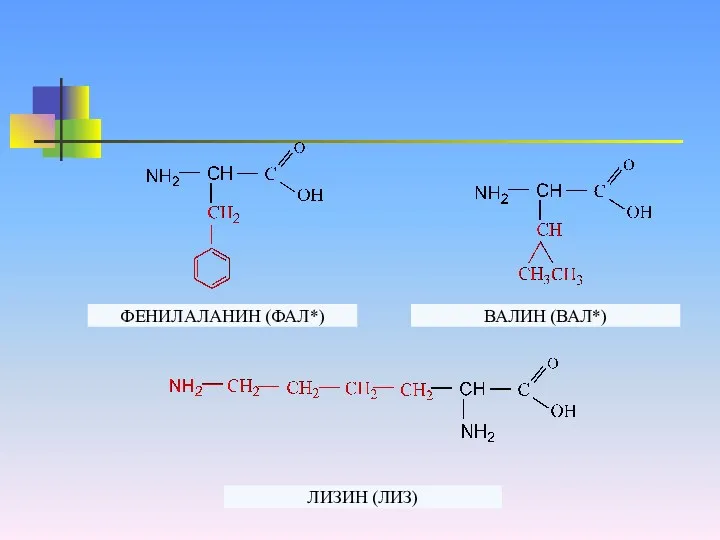
ФЕНИЛАЛАНИН (ФАЛ*)
ВАЛИН (ВАЛ*)
ЛИЗИН (ЛИЗ)
Слайд 12
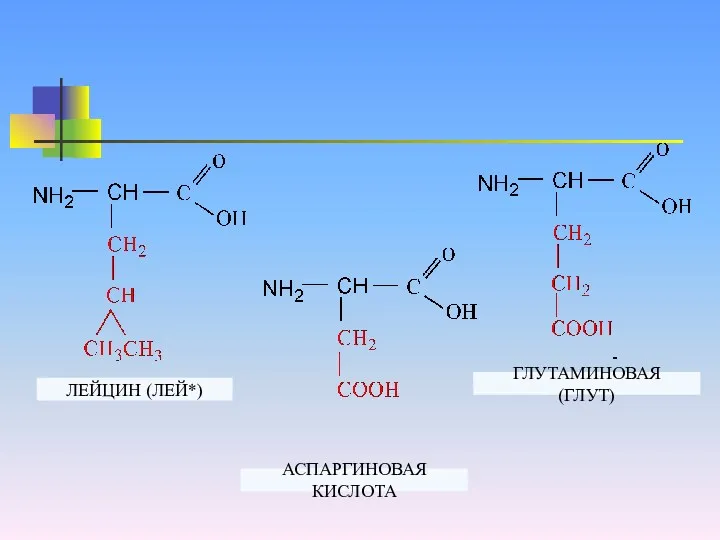
ЛЕЙЦИН (ЛЕЙ*)
ГЛУТАМИНОВАЯ (ГЛУТ)
АСПАРГИНОВАЯ КИСЛОТА
Слайд 13
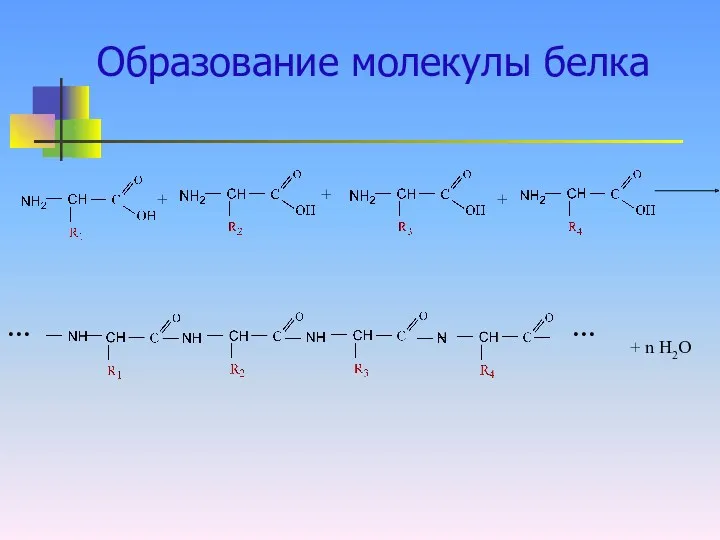
Образование молекулы белка
+
+
+
…
…
+ n Н2О
Слайд 14
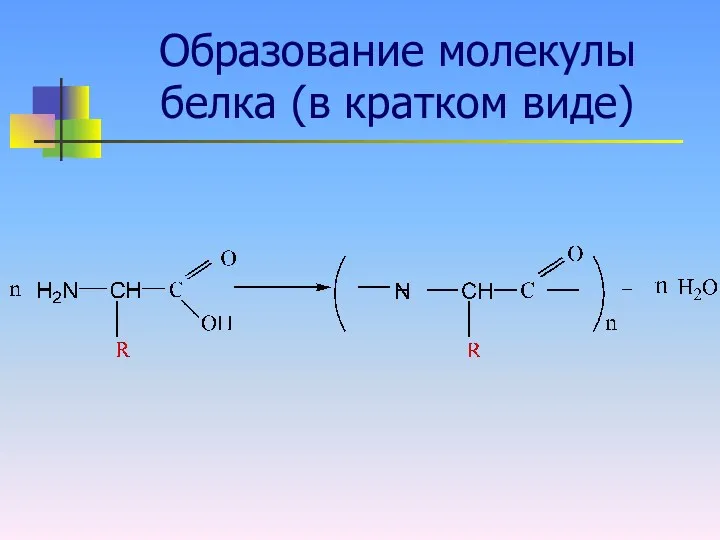
Образование молекулы белка (в кратком виде)
Слайд 15
Слайд 16

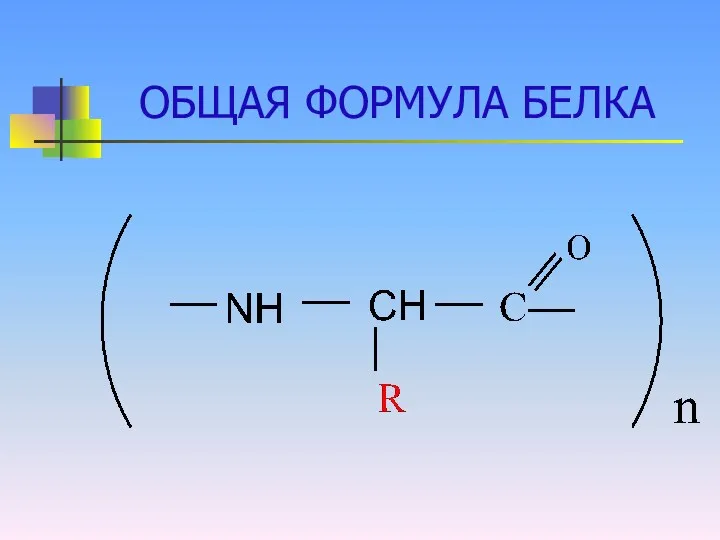
Первичная структура белка
-последовательность чередования различных аминокислотных звеньев в полипептидной цепи
Слайд 17

Первичная структура инсулина человека
Цепь А – 21 аминокислотный остаток:
Гли-иле-вал-глу-глн-цис-цис-три-сер-иле-цис-сер-лей-тир-глн-лей-глу-асн-тир-цис-асн.
Это надо
понимать так: Молекула глицина (гли) реагирует с молекулой изолейцина (иле), затем с молекулой валина (вал) и т.д.
Слайд 18

Цепь В – 30 аминокислотных остатков:
фал-вал-асн-глн-гис-лей-цис-гли-сер-гис-лей-вал-глу-ала-лей-тир-лей-вал-цис-гли-цис-гли-глут-арг-гли-фал-фал-тир-тре-про-лиз-ал
Слайд 19
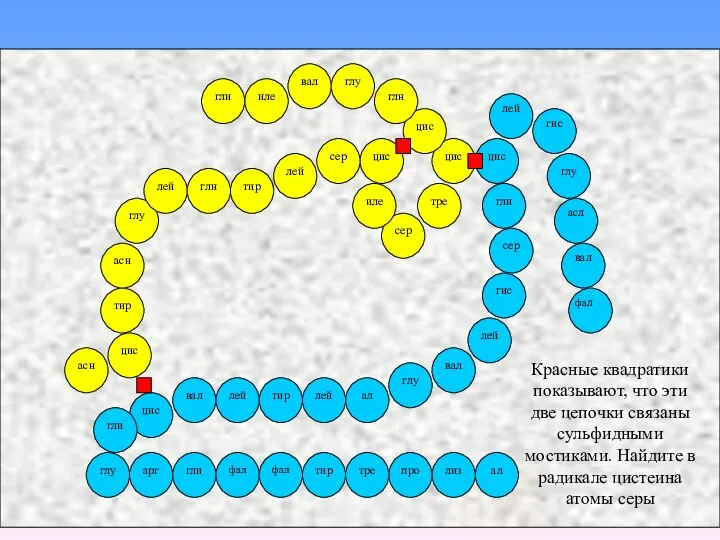
Красные квадратики показывают, что эти две цепочки связаны сульфидными мостиками. Найдите
в радикале цистеина атомы серы
Слайд 20

Полипептидная цепочка молекулы белка сворачивается в спираль определенного вида.
У каждого
белка она своя. Между соседними витками устанавливается водородная связь. (Посмотрите в теме «Химическая связь»)
Она обозначается тремя точечками.
Найдите ее на следующем слайде
Слайд 21
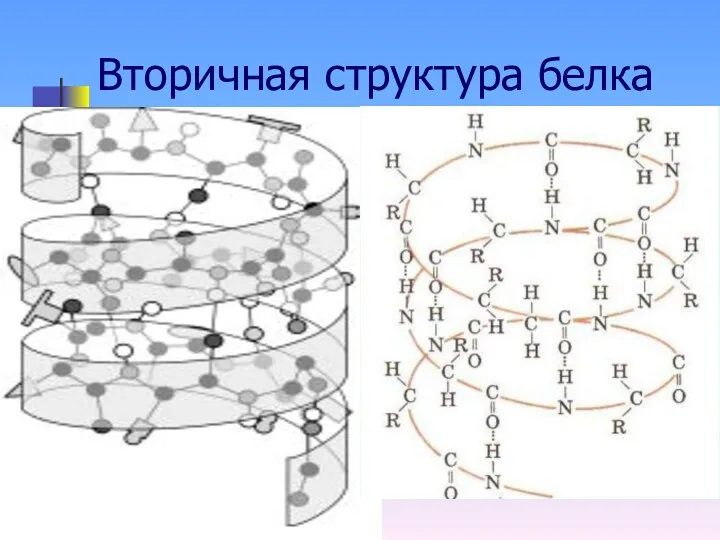
Вторичная структура белка
Слайд 22

Спираль молекулы белка сворачивается в клубок «глобулу» (Однокоренное слово-глобус)
Слайд 23
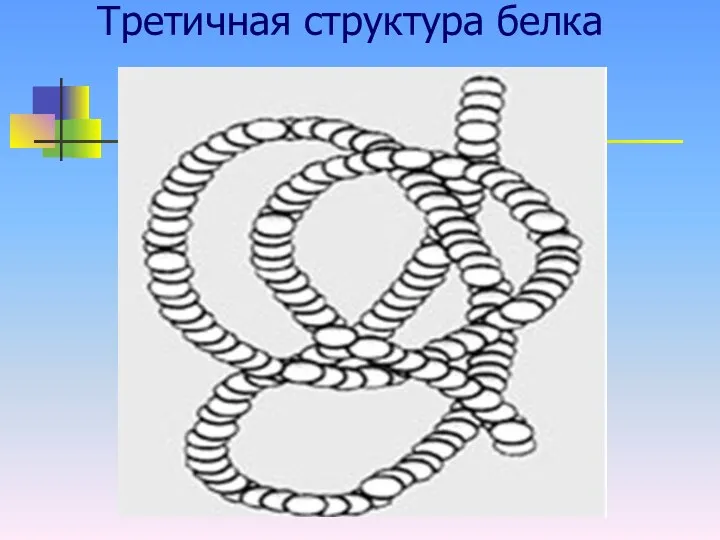
Третичная структура белка
Слайд 24

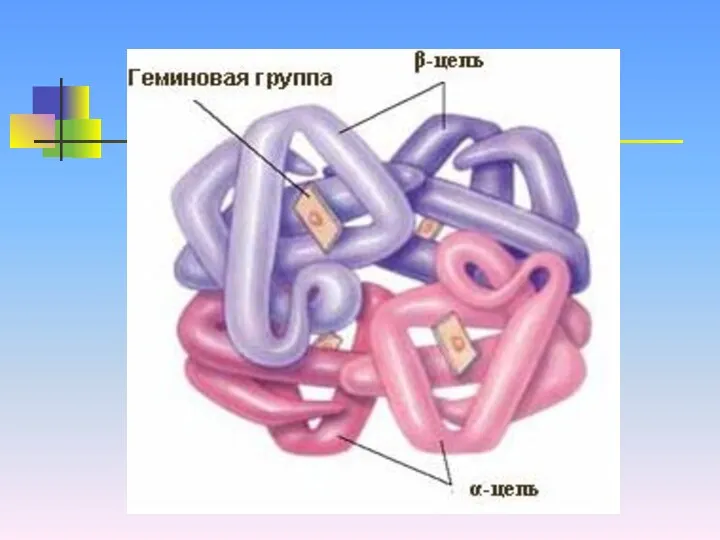
У некоторых белков существует и четвертичная структура.
Это взаимное расположение глобул
относительно друг друга
На следующем слайде представлена схематически четвертичная структура молекулы гемоглобина. 4 глобулы вот так собираются вместе, образуя макромолекулу. Вот туда в серединку «залезает» кислород и с кровью переносится по организму.
Слайд 25
Слайд 26

Свойства белков
1. Денатурация (натура-это природа, натуральный- значит природный, не искусственный -
созданный человеком. Частица «де» придает слову противоположный смысл. Т.е. получается в итоге- разрушение того, что создала природа)
Происходит под действием высоких и низких температур, действии химических веществ (кислот, щелочей, солей тяжелых металлов, спиртов). На лабораторной увидим попозже.
Слайд 27

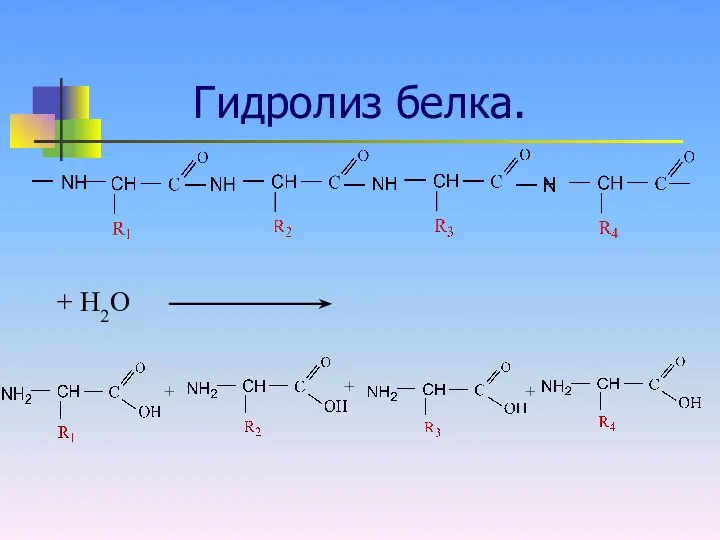
Гидролиз.
На 30 слайде в режиме «Показ слайдов» посмотрите анимацию.
Уравнение реакции на
31 слайде
Слайд 28
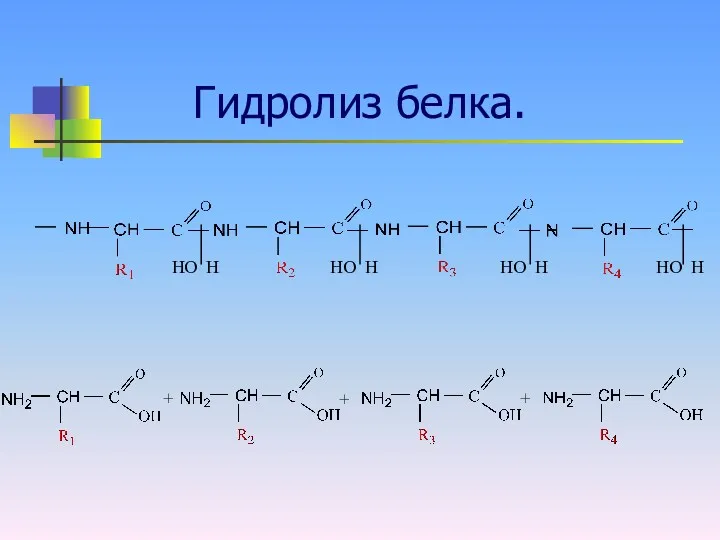
Гидролиз белка.
HO H
HO H
HO H
HO H
+
+
+
Слайд 29
Слайд 30

Качественные реакции на белки
Это мы посмотрим на лабораторной работе





























 Разделение углеводородных газов
Разделение углеводородных газов Бутадиеновые каучуки
Бутадиеновые каучуки Решение заданий по теме: Оксиды
Решение заданий по теме: Оксиды Метаморфические породы. (Лекция 10)
Метаморфические породы. (Лекция 10) Химический состав и физические свойства продовольственных товаров
Химический состав и физические свойства продовольственных товаров Контрольная работа. Разбор. 9 класс
Контрольная работа. Разбор. 9 класс Камни и Козерог
Камни и Козерог Поляризация электродов
Поляризация электродов Химия и повседневная жизнь человека
Химия и повседневная жизнь человека Количество вещества. 8 класс
Количество вещества. 8 класс Методы определения механических свойств полимерных композиционных материалов
Методы определения механических свойств полимерных композиционных материалов Благородные металлы
Благородные металлы Золото. Что о нём мы можем рассказать?
Золото. Что о нём мы можем рассказать? Салыстырмалы тығыздығы мен элементтердің массалық үлестері бойынша газ күйіндегі заттардың молекулалық формулаларын табу
Салыстырмалы тығыздығы мен элементтердің массалық үлестері бойынша газ күйіндегі заттардың молекулалық формулаларын табу Зиянды организмдерге қарсы органикалық және органикалық емес қосылыстарды қолдануға негізделген тәсіл
Зиянды организмдерге қарсы органикалық және органикалық емес қосылыстарды қолдануға негізделген тәсіл Скорость химических реакций
Скорость химических реакций Галогены (солеобразующие)
Галогены (солеобразующие) Техника безопасности для учащихся в кабинете химии
Техника безопасности для учащихся в кабинете химии Гидролиз солей
Гидролиз солей Влияние циклогексанола селективную очистку масляных фракций нефти N-метилпирролидоном (N-МП)
Влияние циклогексанола селективную очистку масляных фракций нефти N-метилпирролидоном (N-МП) Фенолдар. Анықтама
Фенолдар. Анықтама Витаминные препараты
Витаминные препараты 20230419_gidroliz_soley
20230419_gidroliz_soley Реакции ионного обмена
Реакции ионного обмена Игровая программа по химии Самый умный. Химические свойства оксидов, оснований, кислот и солей
Игровая программа по химии Самый умный. Химические свойства оксидов, оснований, кислот и солей Тепловой эффект химических реакций. 8 класс
Тепловой эффект химических реакций. 8 класс Химическая связь. Виды химической связи
Химическая связь. Виды химической связи Коррозия металлов. Методы защиты металлов от коррозии
Коррозия металлов. Методы защиты металлов от коррозии