Содержание
- 2. Ионная химическая связь. Особенности ионной связи Ионная связь – это притяжение ионов как разноименно заряженных тел.
- 3. Ионная связь Рассмотрим образование молекулы NaCl:
- 4. Ионная связь Хлор имеет 7 электронов на внешней электронной оболочке, до стабильного электронного состояния ему не
- 5. Ионная связь Натрий имеет 1 электрон на последней электронной оболочке и 8 электронов на предпоследней, отдавая
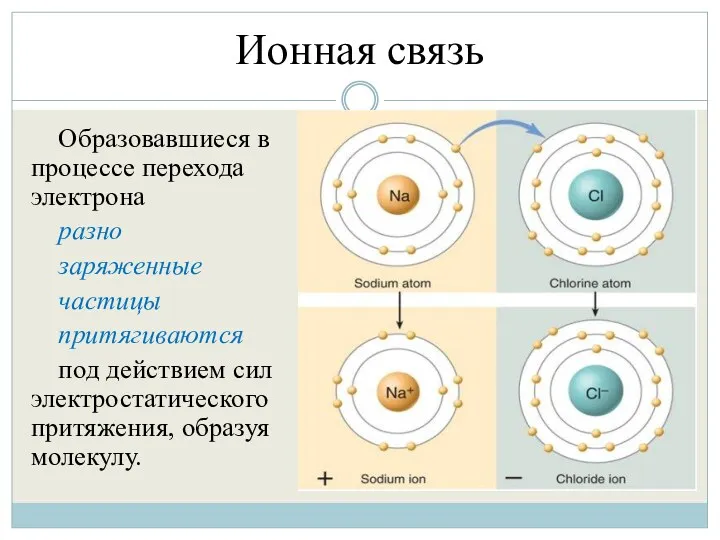
- 6. Ионная связь Образовавшиеся в процессе перехода электрона разно заряженные частицы притягиваются под действием сил электростатического притяжения,
- 7. Характеристики ионной связи 1. Отсутствие направленности (в отличие от ковалентной связи), что объясняется тем, что электрическое
- 8. Характеристики ионной связи Поэтому в твердых веществах с ионной связью невозможно выделить отдельную молекулу.
- 9. Характеристики ионной связи 2. Отсутствие насыщенности. Как отмечалось выше, система из двух зарядов, одинаковых по величине,
- 10. Характеристики ионной связи Все ионные соединения в твердом состоянии имеют ионную кристаллическую решетку, в которой каждый
- 11. Характеристики ионной связи
- 12. СВЯЗЬ Металлическая
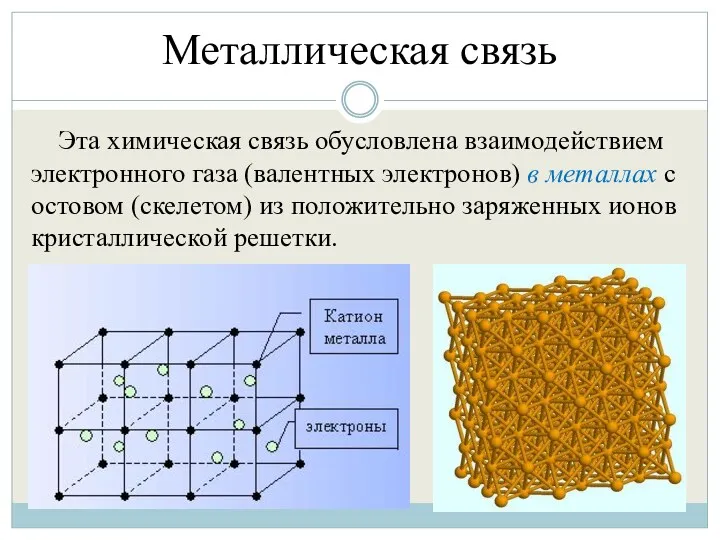
- 13. Металлическая связь Эта химическая связь обусловлена взаимодействием электронного газа (валентных электронов) в металлах с остовом (скелетом)
- 14. Металлическая связь Металлическая связь имеет сходство как с ионной связью: образуется за счёт взаимодействия заряженных частиц:
- 15. Металлическая связь Рассмотрим образование связи на примере металла натрия. У натрия, как и у других металлов,
- 16. Металлическая связь Свободные электроны в металлическом кристалле находятся на перекрывающихся орбиталях и, в какой-то мере, обобществляются,
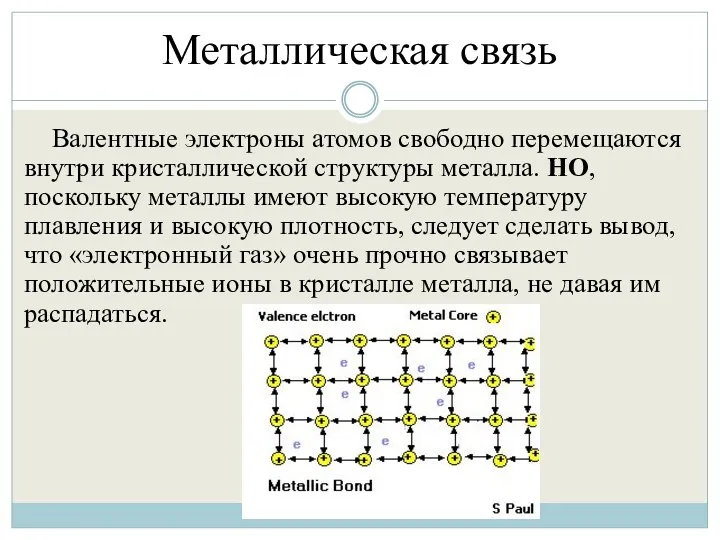
- 17. Металлическая связь Валентные электроны атомов свободно перемещаются внутри кристаллической структуры металла. НО, поскольку металлы имеют высокую
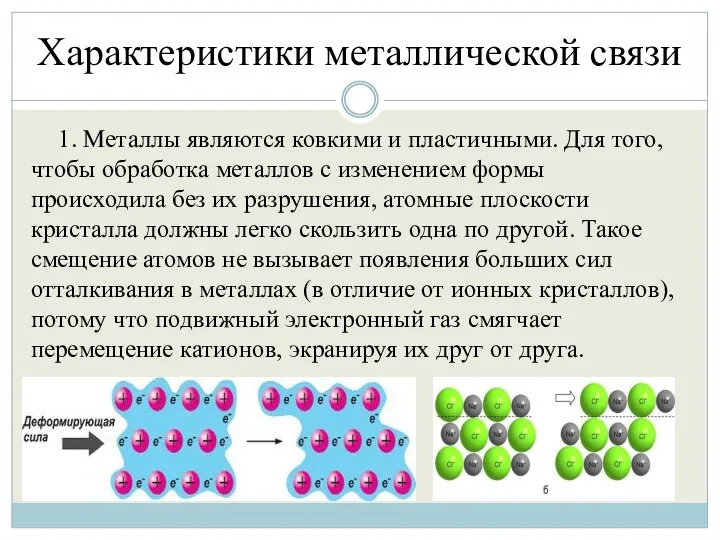
- 18. Характеристики металлической связи 1. Металлы являются ковкими и пластичными. Для того, чтобы обработка металлов с изменением
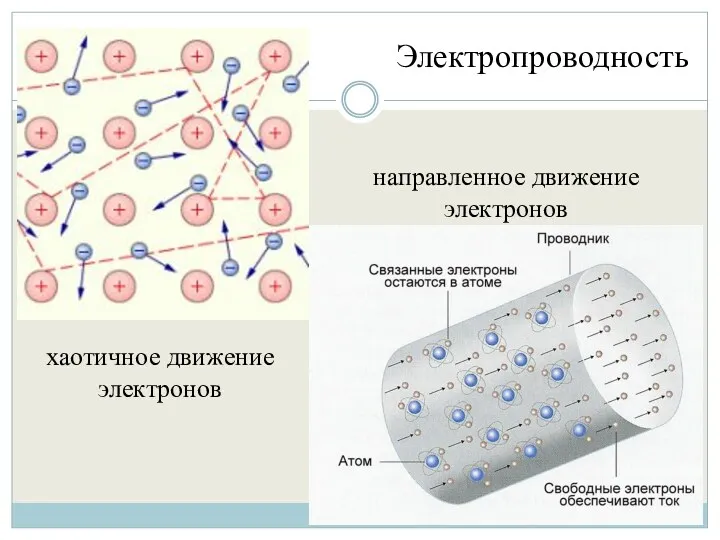
- 19. Характеристики металлической связи 2. Электропроводность. Электроны в металле свободны и перемещаются по пересеченным атомным орбиталям кристалла
- 20. Электропроводность хаотичное движение электронов направленное движение электронов
- 21. СВЯЗЬ Водородная
- 22. Водородная связь Это форма взаимодействия электроотрицательного атома и атома водорода H, связанного ковалентной связью с другим
- 25. Водородная связь Возникновение водородной связи объясняется действием электростатических сил. Так, в молекуле воды при образовании полярной
- 26. Водородная связь В результате атом кислорода приобретает частичный отрицательный заряд, а атом водорода – частичный положительный,
- 27. Характеристики водородной связи Энергия водородной связи (8 - 40 кДж/моль) меньше энергии обычной ковалентной связи (150
- 28. Характеристики водородной связи Вещества с водородными связями имеют высокие температуры кипения (например, вода, спирты, жидкий HF,
- 29. Характеристики водородной связи 2. Водородные связи являются причиной другого уникального свойства воды – при плавлении ее
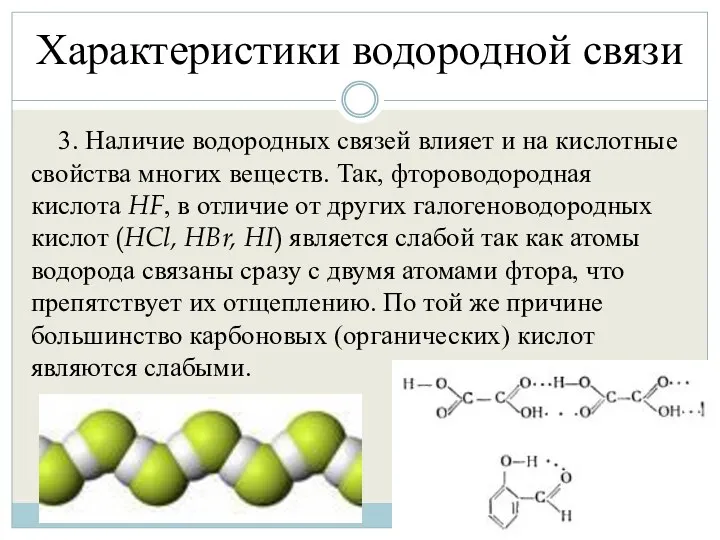
- 30. Характеристики водородной связи 3. Наличие водородных связей влияет и на кислотные свойства многих веществ. Так, фтороводородная
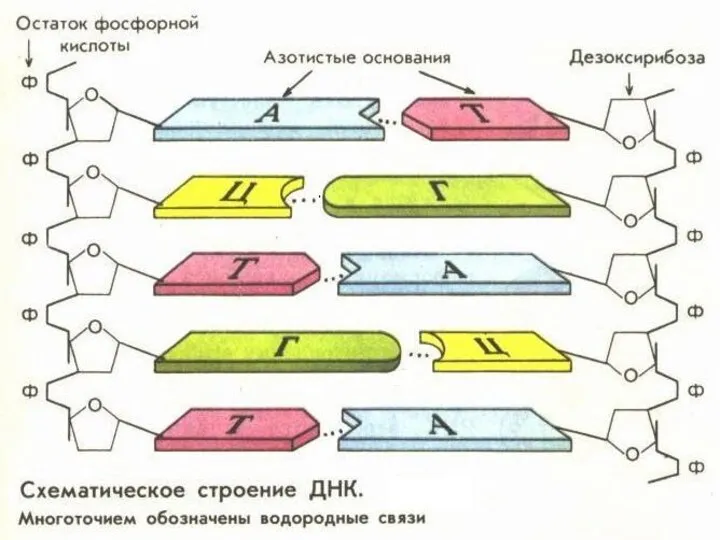
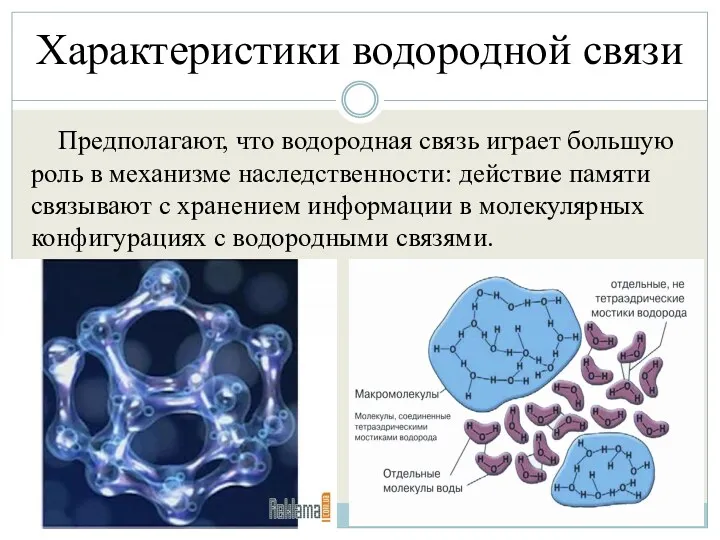
- 31. Характеристики водородной связи Предполагают, что водородная связь играет большую роль в механизме наследственности: действие памяти связывают
- 33. МОЛЕКУЛ Полярность
- 34. Полярность молекул Полярные вещества в химии – это вещества, молекулы которых обладают электрическим дипольным моментом. Дипольный
- 35. Полярность молекул Полярными являются молекулы: Образованные ионной химической связью.
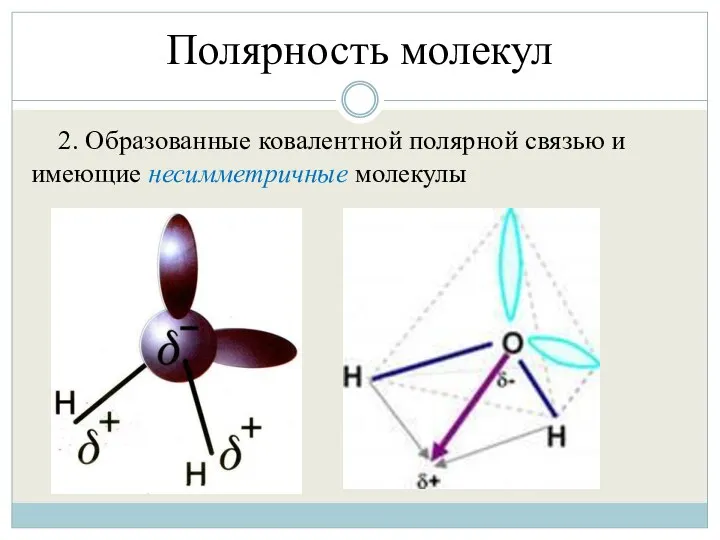
- 36. Полярность молекул 2. Образованные ковалентной полярной связью и имеющие несимметричные молекулы
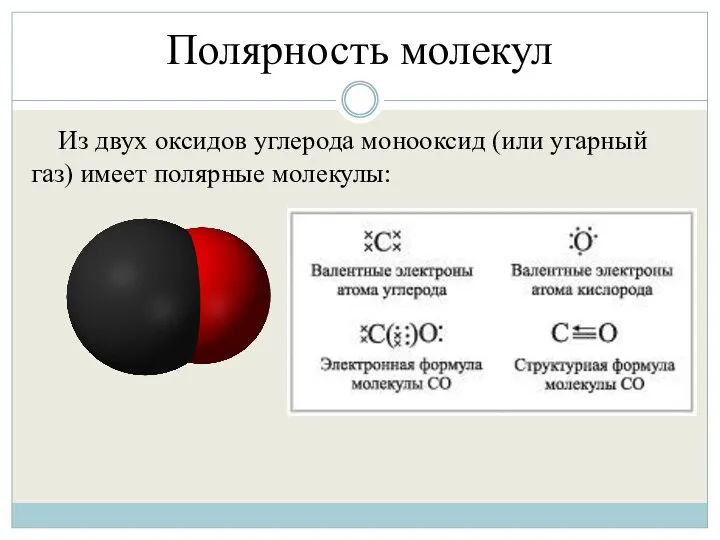
- 37. Полярность молекул Из двух оксидов углерода монооксид (или угарный газ) имеет полярные молекулы:
- 38. Полярность молекул Если сравнивать полярность неорганических и органических веществ, то у последних она ниже. Это объясняется
- 39. Полярность молекул (уменьшается слева направо) уксусная кислота масляная кислота стеариновая кислота
- 40. Полярность молекул Неполярными являются молекулы: 1. Образованные неполярными связями (ковалентной неполярной или металлической). азот сера медь
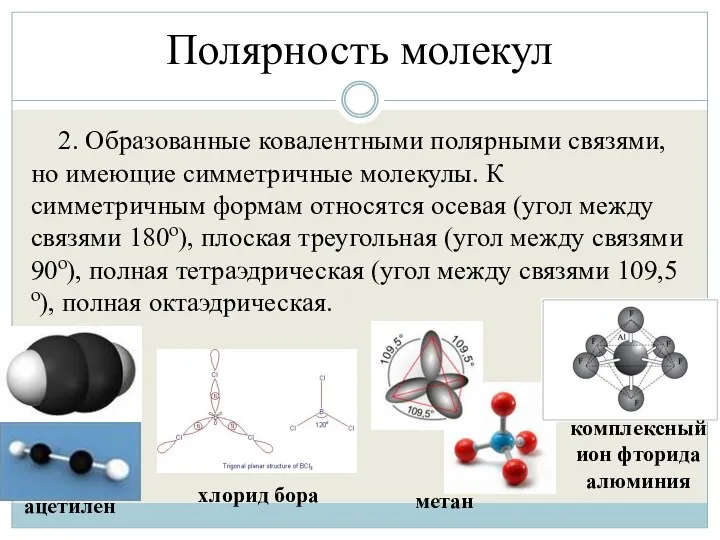
- 41. Полярность молекул 2. Образованные ковалентными полярными связями, но имеющие симметричные молекулы. К симметричным формам относятся осевая
- 43. Скачать презентацию

























 Галогены. Фтор, хлор, бром, йод, астат
Галогены. Фтор, хлор, бром, йод, астат Пропилен-алкены(пропен)
Пропилен-алкены(пропен) Теория строения органических соединений
Теория строения органических соединений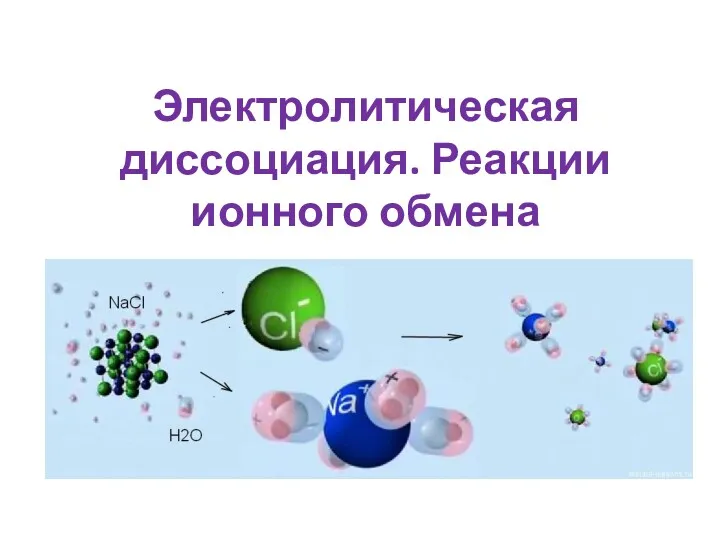 Электролитическая диссоциация. Реакции ионного обмена
Электролитическая диссоциация. Реакции ионного обмена 20230205_okislitelno-_vosstanovitelnye_reaktsii
20230205_okislitelno-_vosstanovitelnye_reaktsii Скорость химических реакций. Катализ. Химическое равновесие
Скорость химических реакций. Катализ. Химическое равновесие Соли. Классификация. Физические и химические свойства солей
Соли. Классификация. Физические и химические свойства солей Current Condition(Revision C)
Current Condition(Revision C) Состояние электронов в атоме
Состояние электронов в атоме Измерение и оценка химического фактора. Лекция 9
Измерение и оценка химического фактора. Лекция 9 Фосфор и его соединения
Фосфор и его соединения Прочность полимеров
Прочность полимеров Скорость химических реакций. Химическое равновесие
Скорость химических реакций. Химическое равновесие Бензол молекуласында байланыстардың түзілу сызбанұсқасы
Бензол молекуласында байланыстардың түзілу сызбанұсқасы Полімери. Їх властивості та застосування
Полімери. Їх властивості та застосування Периодический закон Д.И. Менделеева
Периодический закон Д.И. Менделеева Щелочные металлы
Щелочные металлы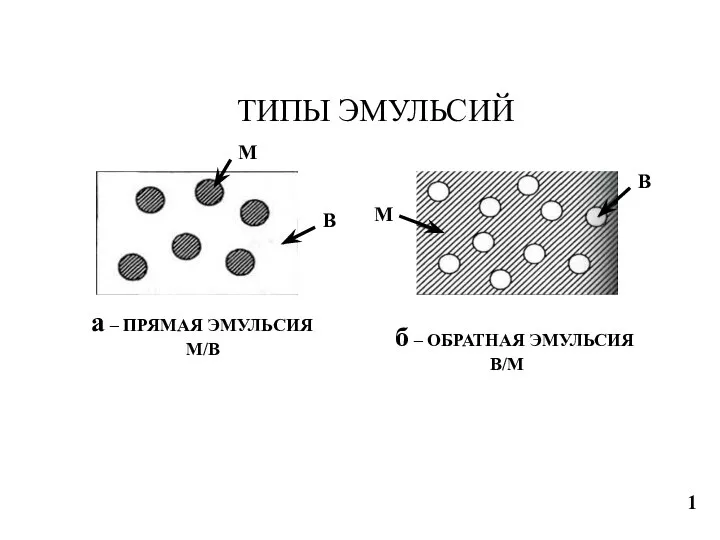 Типы эмульсий. Фракционный состав нефти. Типы нефти
Типы эмульсий. Фракционный состав нефти. Типы нефти Счастливый случай. Право первого хода
Счастливый случай. Право первого хода Газообразные вещества
Газообразные вещества Химическая коррозия. Методы защиты от химической коррозии
Химическая коррозия. Методы защиты от химической коррозии Алкины. Гомологический ряд
Алкины. Гомологический ряд Теория строения органического вещества. 10 класс
Теория строения органического вещества. 10 класс Самое удивительное на свете вещество - вода
Самое удивительное на свете вещество - вода АЛКАНЫ Строение молекулы метана.
АЛКАНЫ Строение молекулы метана. Сапалық талдау. Сапалық аналитикалық реакциялар
Сапалық талдау. Сапалық аналитикалық реакциялар Кислород. Химия. 8 класс
Кислород. Химия. 8 класс Физические свойства металлов
Физические свойства металлов