Содержание
- 2. Модуль 1. Химическая коррозия Лекция 1.2 Изменение природы металла (жаростойкое легирование) Применение жаростойких защитных покрытий Применение
- 3. Модуль 1. Химическая коррозия Лекция 1.2 Существуют 3 теории жаростойкого легирования 1. Теория уменьшения деффектности, получающегося
- 4. Жаростойкое легирование Легирующий компонент должен: обладать большим сродством к кислороду; растворяться в оксиде основного; валентность должна
- 5. Жаростойкое легирование Модуль 1. Химическая коррозия Лекция 1.2 2. Теория защитного оксида Теория справедлива для среднего
- 6. Жаростойкое легирование Легирующий компонент должен: Легко окисляться; Размер его должен быть меньше основного; Оксид его должен
- 7. Теория образования высокозащитных двойных окислов Согласно теории, наиболее полно сформулированной В.И. Архаровым для сплавов на железной
- 8. Теория образования высокозащитных двойных оксидов Оптимальными по этой теории являются такие легирующие элементы, которые уменьшают возможность
- 9. Основные элементы жаростойкого легирования Cr, Al, Si. Самый главный элемент Cr, вводится в количестве от 4-5%
- 10. 15Х5М, 12Х5МА – 550-600о С; 15Х6СМ - 650-700о С; 10Х9С2Ю, 12Х13 - 700 – 750о С;
- 11. Никелевые сплавы Нихром XН60ВТ, ХН70МВТЮБ Нимоник 18-21 % Сr, 2-20% Со, 1,8-2,7 % Тi. Хастеллой 15-23%
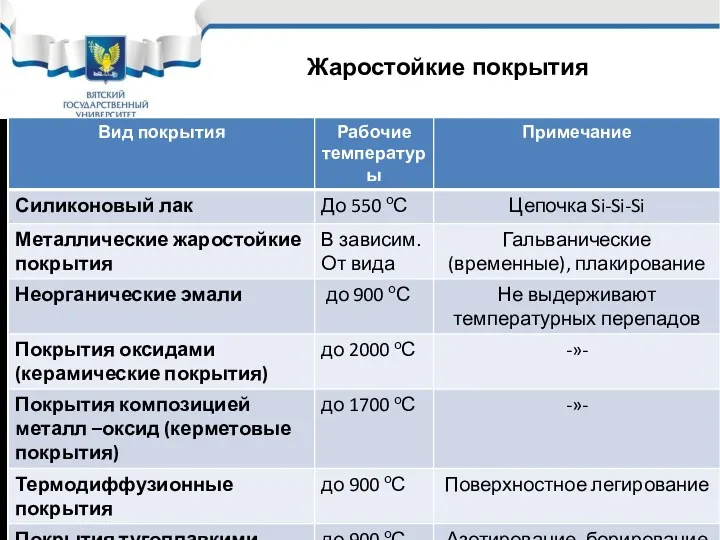
- 12. Жаростойкие покрытия
- 13. Жаростойкие покрытия Модуль 1. Химическая коррозия Лекция 1.2 1. Из наиболее широко применяемых жаростойких покрытий применяются
- 14. Жаростойкие покрытия 1. Термодиффузионные покрытия – поверхностное легирование стали жаростойкими компонентами. Хром – термохромирование, алюминий –
- 15. Керметы Материалы получаемые методом порошковой металлургии. В состав входят: металлическая связка и керамические компоненты (оксиды, карбиды,
- 16. Защитные атмосферы Модуль 1. Химическая коррозия Лекция 1.2 Применяются широко при сварке. Сварка идет при температуре
- 17. Химическая коррозия в не электролитах Органические жидкости, в частности, продукты перегонки нефти (бензин, керосин, лигроин, масла
- 18. Химическая коррозия в не электролитах 3. Химическая реакция реагента с металлом; Диффузия продуктов коррозии от металла.
- 20. Скачать презентацию
















 Химикаты для сельского хозяйства
Химикаты для сельского хозяйства Алкены (олефины, этиленовые углеводороды)
Алкены (олефины, этиленовые углеводороды) Химия s-элементов. Общая характеристика
Химия s-элементов. Общая характеристика Третья группа, главная подгруппа. 9 класс
Третья группа, главная подгруппа. 9 класс Оксид водорода (H2O)
Оксид водорода (H2O) Силикатное производство
Силикатное производство Реакции SR в ряду алканов
Реакции SR в ряду алканов Золото и серебро
Золото и серебро Керамические материалы
Керамические материалы Особенности организации обучения химии в рамках компетентностно-ориентированной модели образования
Особенности организации обучения химии в рамках компетентностно-ориентированной модели образования Алкены. Химические свойства этилена
Алкены. Химические свойства этилена Phosphorus
Phosphorus Предмет органической химии. Органические вещества
Предмет органической химии. Органические вещества Введение в токсикологическую химию. Объекты химико-токсикологического исследования
Введение в токсикологическую химию. Объекты химико-токсикологического исследования Заходи з ліквідації наслідків хімічної небезпечної надзвичайної ситуації. Особливості ведення хімічної розвідки та контролю
Заходи з ліквідації наслідків хімічної небезпечної надзвичайної ситуації. Особливості ведення хімічної розвідки та контролю Железо в периодической таблице химических элементов и строение его атома
Железо в периодической таблице химических элементов и строение его атома Основные этапы первичного процесса переработки нефти
Основные этапы первичного процесса переработки нефти Углеводы. Глюкоза
Углеводы. Глюкоза Электролиз. Классификация
Электролиз. Классификация Классификация и номенклатура органических соединений. (Лекция 1)
Классификация и номенклатура органических соединений. (Лекция 1) Каталитический риформинг
Каталитический риформинг Многоатомные спирты
Многоатомные спирты Коррозия металлов. Часть 2. Лекция №11
Коррозия металлов. Часть 2. Лекция №11 Периодическая система элементов, предсказание химических свойств элементов на основе таблицы
Периодическая система элементов, предсказание химических свойств элементов на основе таблицы Классы неорганических веществ. Лекция №2
Классы неорганических веществ. Лекция №2 Теорія сильних і слабких електролітів. Рівновага в розчинах малорозчинних електролітів
Теорія сильних і слабких електролітів. Рівновага в розчинах малорозчинних електролітів Строение атома в соответствии с положением в периодической системе химических элементов Д.И. Менделеева
Строение атома в соответствии с положением в периодической системе химических элементов Д.И. Менделеева Электронный помощник по химии (8 класс)
Электронный помощник по химии (8 класс)