Карбонилсодержащие соединения. Строение и химические свойства карбоновых кислот. Липиды. Фосфолипиды презентация
Содержание
- 2. Альдегиды, кетоны, карбоновые кислоты, сложные эфиры, галогено ангидриды, амиды относятся к карбонил содержащим соединениям.
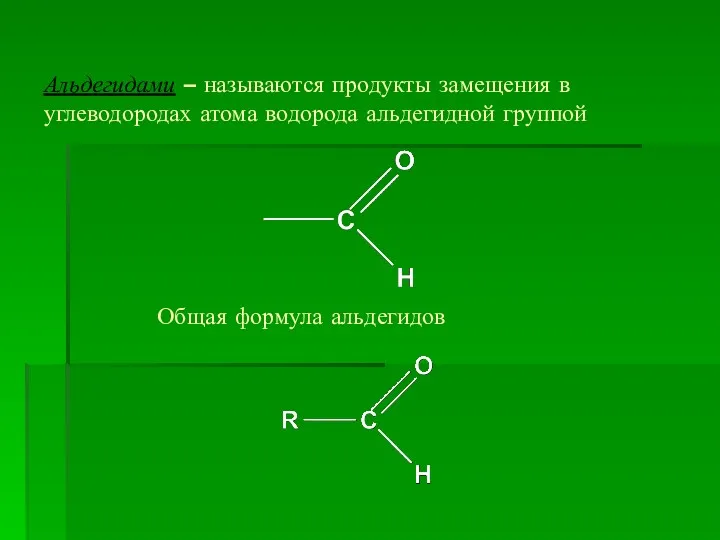
- 3. Альдегидами – называются продукты замещения в углеводородах атома водорода альдегидной группой Общая формула альдегидов
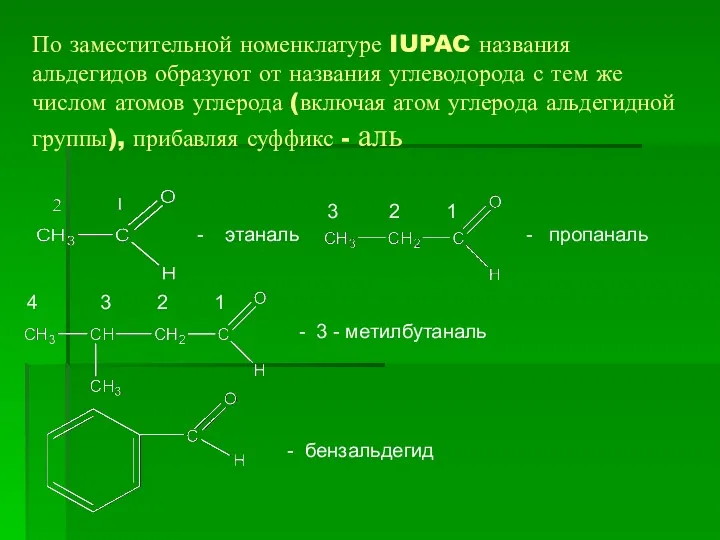
- 4. По заместительной номенклатуре IUPAC названия альдегидов образуют от названия углеводорода с тем же числом атомов углерода
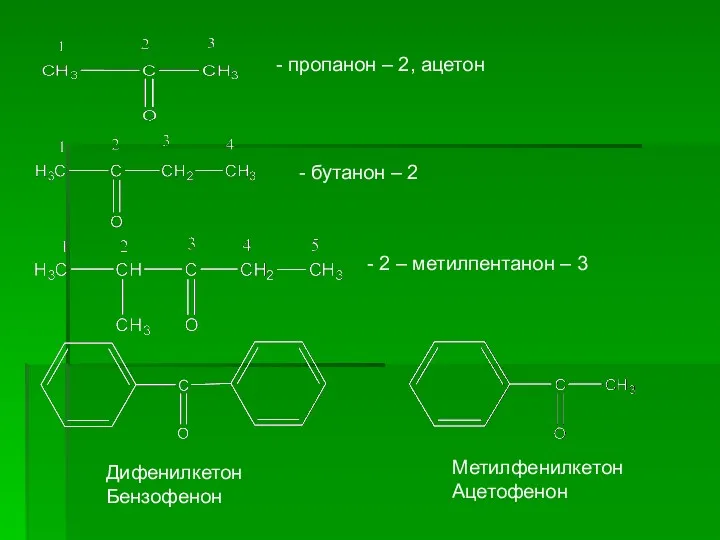
- 5. Кетоны – углеводороды, содержащие карбонильную группу, связанную с двумя радикалами. В кетонах наличие оксо-группы передают (IUPAC)
- 6. - пропанон – 2, ацетон - бутанон – 2 - 2 – метилпентанон – 3 Дифенилкетон
- 7. В зависимости от строения углеводородного радикала альдегиды и кетоны подразделяются на алифатические, алициклические, ароматические, а кетоны
- 8. Строение оксо группы: Тригональный атом углерода в карбонильной группе находится в SP2 гибридизации. Благодаря большой электроотрицательности
- 9. Легкость нуклеофильной атаки зависит от: Величины эффективного + заряда на атоме углерода; Его пространственной доступности; Кислотно-основных
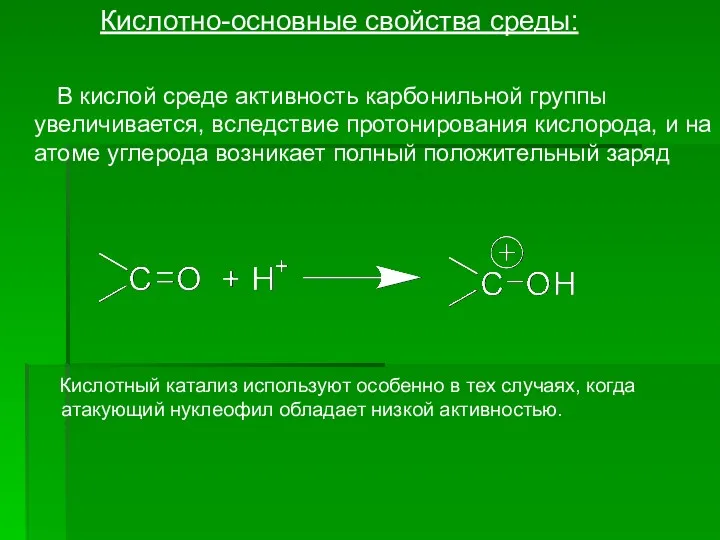
- 10. Кислотно-основные свойства среды: В кислой среде активность карбонильной группы увеличивается, вследствие протонирования кислорода, и на атоме
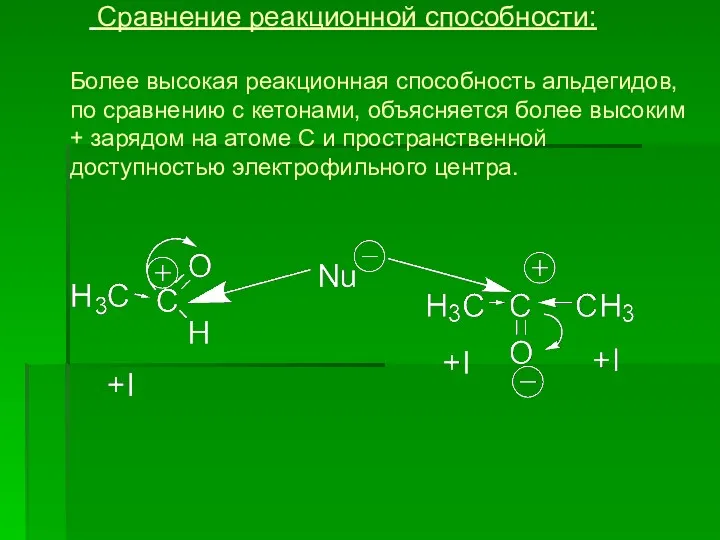
- 11. Сравнение реакционной способности: Более высокая реакционная способность альдегидов, по сравнению с кетонами, объясняется более высоким +
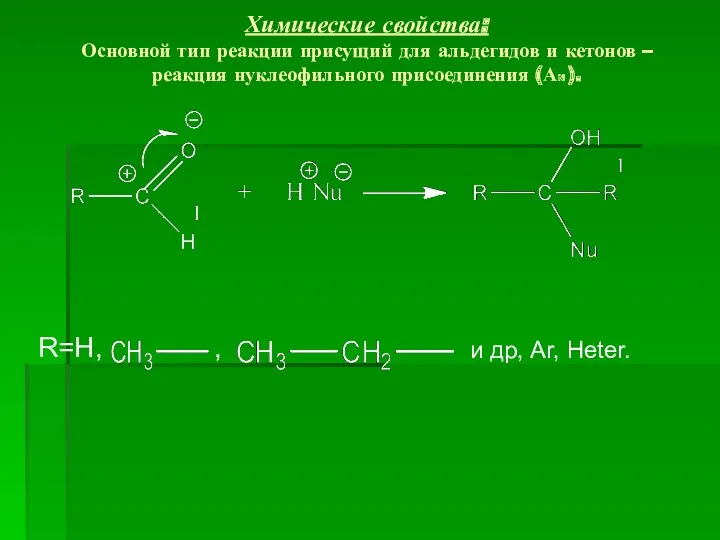
- 12. Химические свойства: Основной тип реакции присущий для альдегидов и кетонов – реакция нуклеофильного присоединения (АN ).
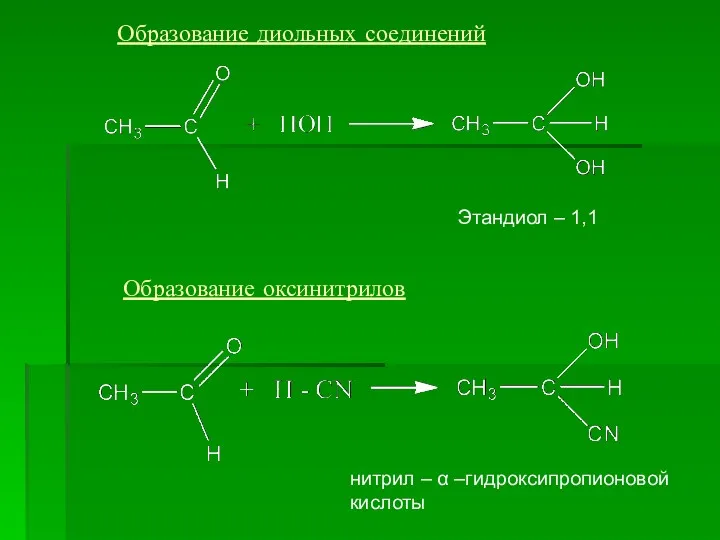
- 13. Образование диольных соединений Образование оксинитрилов Этандиол – 1,1 нитрил – α –гидроксипропионовой кислоты
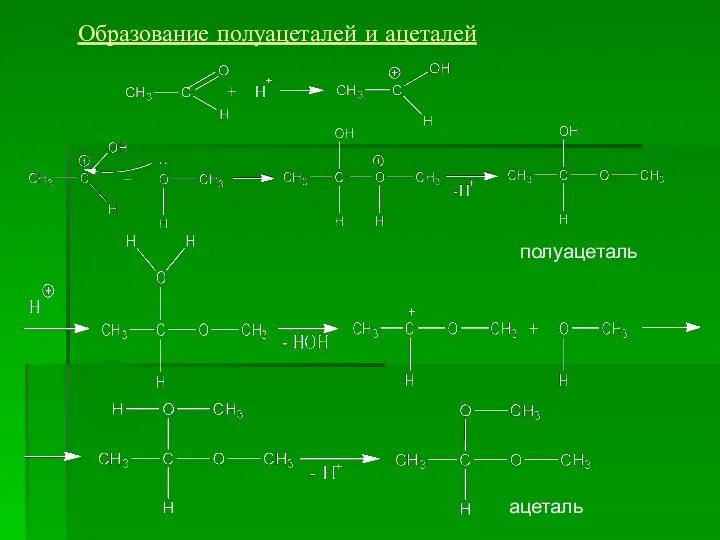
- 14. О Т Образование полуацеталей и ацеталей полуацеталь ацеталь
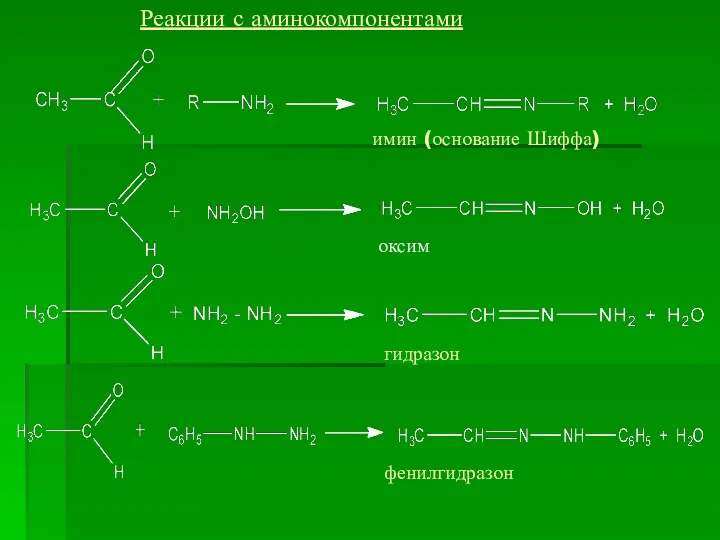
- 15. Реакции с аминокомпонентами имин (основание Шиффа) оксим гидразон фенилгидразон
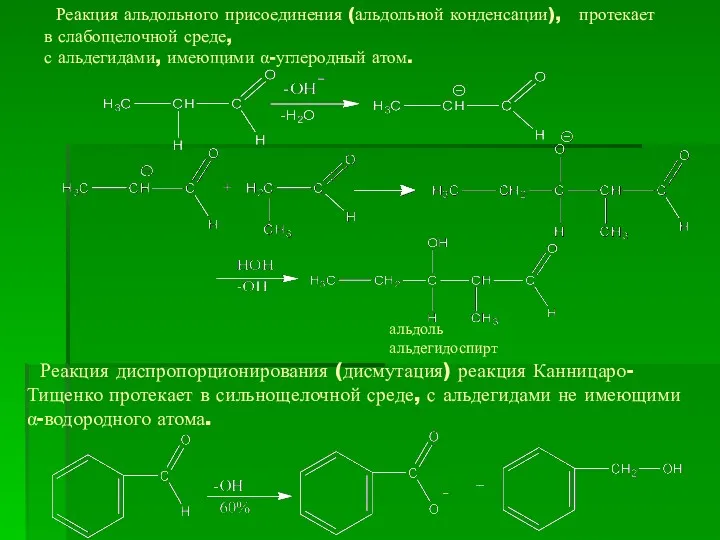
- 16. Реакция альдольного присоединения (альдольной конденсации), протекает в слабощелочной среде, с альдегидами, имеющими α-углеродный атом. Реакция диспропорционирования
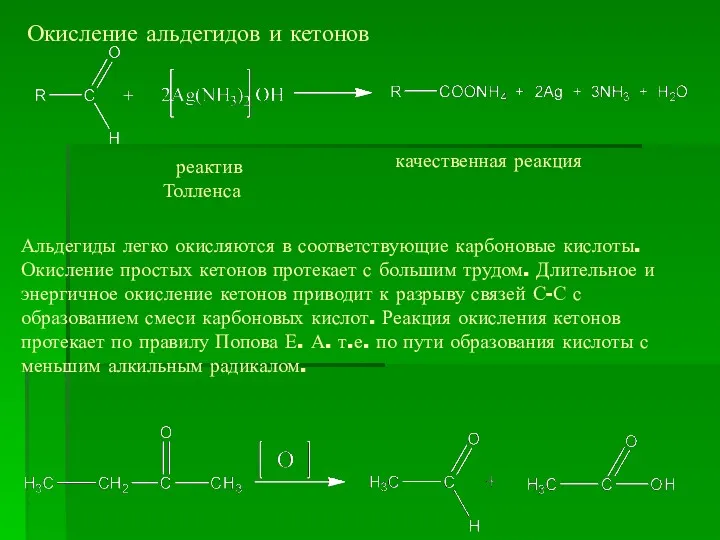
- 17. Окисление альдегидов и кетонов качественная реакция реактив Толленса Альдегиды легко окисляются в соответствующие карбоновые кислоты. Окисление
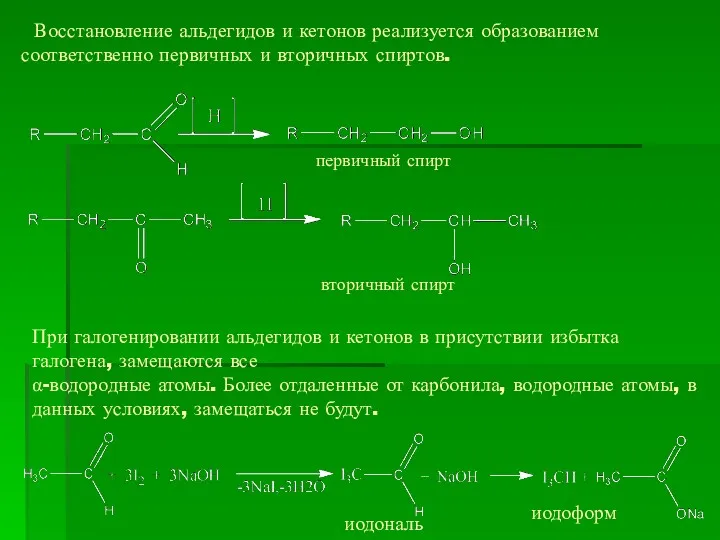
- 18. Восстановление альдегидов и кетонов реализуется образованием соответственно первичных и вторичных спиртов. первичный спирт вторичный спирт При
- 19. Карбоновые кислоты – строение и химические свойства. Липиды. Фосфолипиды.
- 20. Одноосновные карбоновые кислоты – это производные углеводородов, у которых один или несколько атомов водорода замещены карбоксильной
- 21. Классификация В зависимости от радикала с которым связана карбоксильная группа различают: насыщенные, ненасыщенные, ароматические и гетероароматические
- 22. Строение карбоксильной группы: Электронографическое изучение карбоновых кислот показало, что в молекуле имеется карбонильная и гидроксильная группа.
- 23. Это может быть показано при помощи двух крайних структур или одной формулы с отрицательными зарядами, расположенными
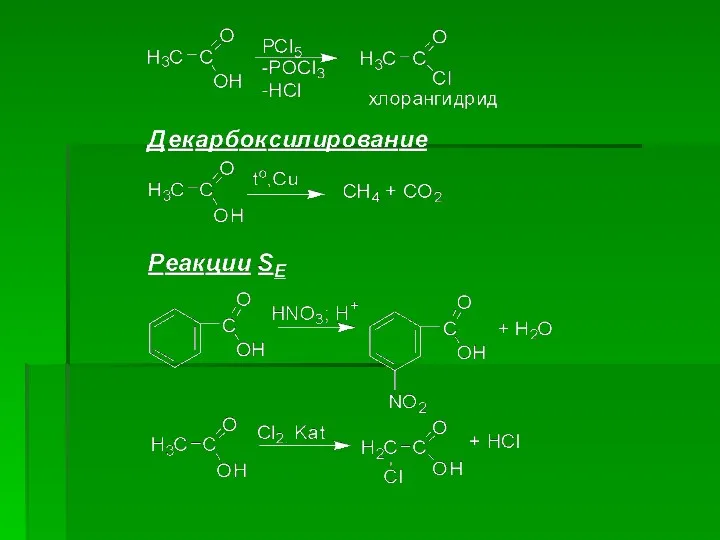
- 24. Химические свойства монокарбоновых кислот определяются электрнным строением карбоксильной группы, в которой различают три реакционных центра.
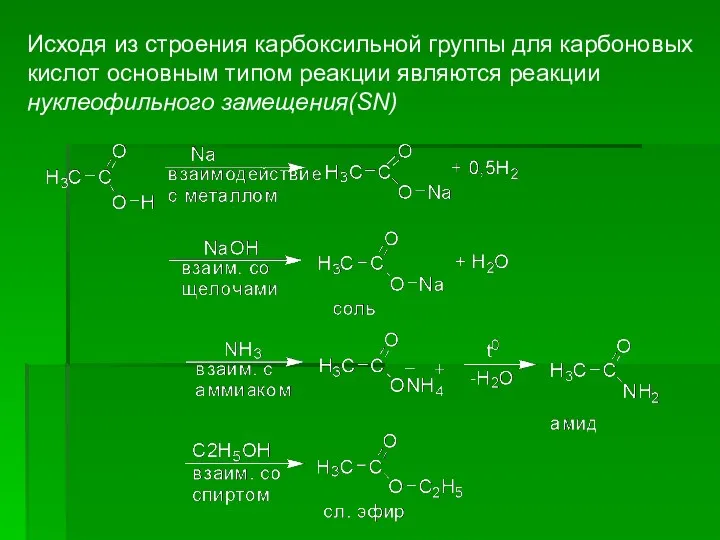
- 25. Исходя из строения карбоксильной группы для карбоновых кислот основным типом реакции являются реакции нуклеофильного замещения(SN)
- 27. Липиды(жиры) – представляют собой смеси сложных эфиров, образованных трехатомным спиртом глицерином и высшими жирными кислотами. Общая
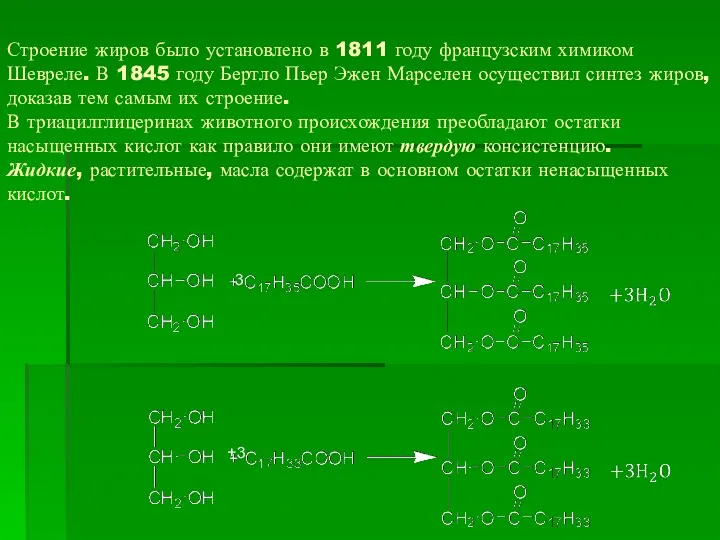
- 28. Строение жиров было установлено в 1811 году французским химиком Шевреле. В 1845 году Бертло Пьер Эжен
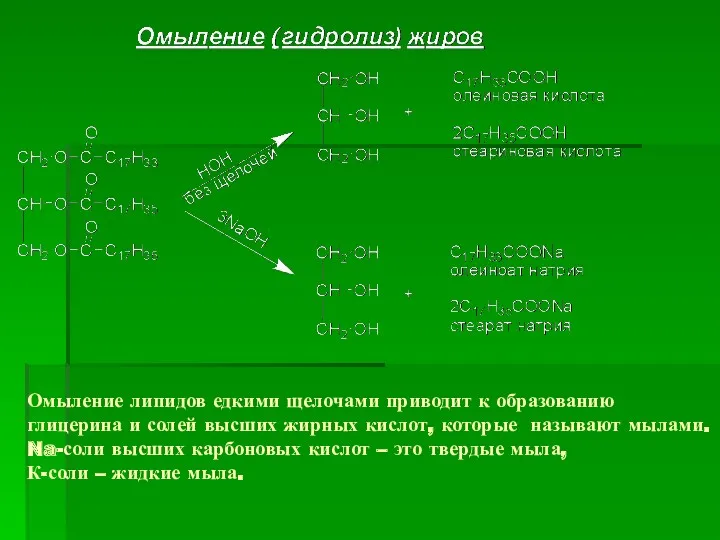
- 29. Омыление липидов едкими щелочами приводит к образованию глицерина и солей высших жирных кислот, которые называют мылами.
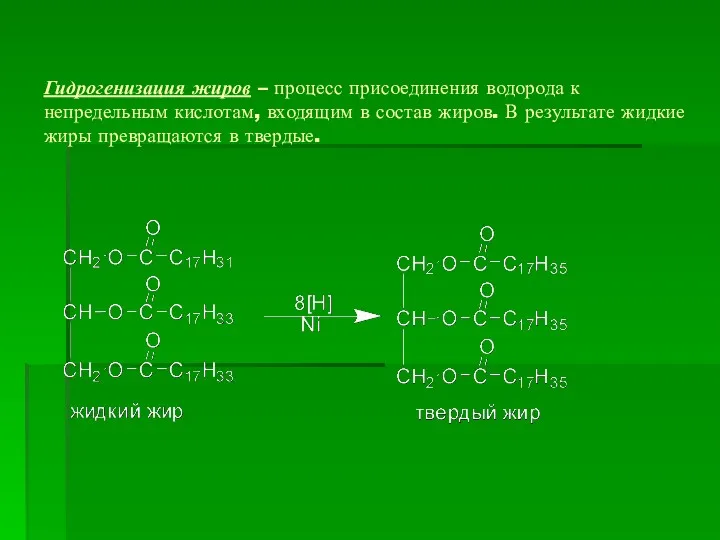
- 30. Гидрогенизация жиров – процесс присоединения водорода к непредельным кислотам, входящим в состав жиров. В результате жидкие
- 31. Для характеристики качества липидов используют аналитические характеристики, которыми являются: Число омыления – это количество миллиграммов КОН,
- 32. Иодное число – служит показателем ненасыщенности жира. Иодное число – это число граммов иода, присоединяющегося к
- 33. Фосфолипиды – липиды, содержащие фосфорную кислоту. Среди глицерофосфолипидов наиболее распространенные сложноэфирные фосфоглицериды – фосфатиды, которые являются
- 34. Представителями фосфатидов являются кефалины – содержащие аминоспирт коламин. При полном гидролизе из молекулы кефалина образуется: глицерин,
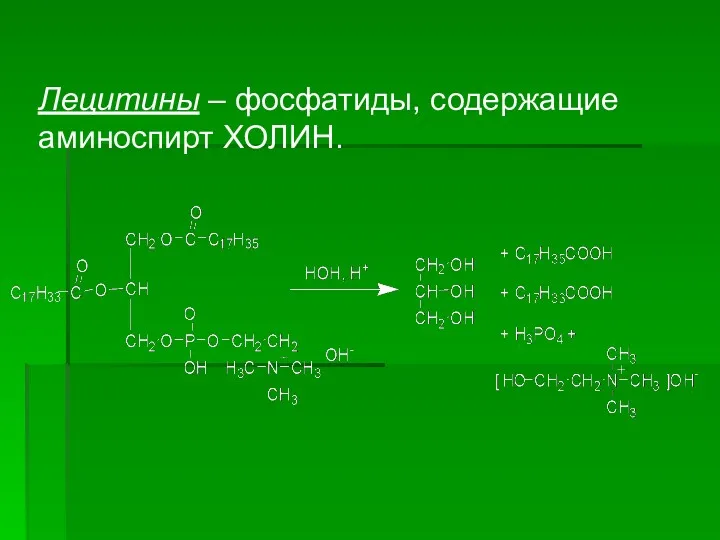
- 35. Лецитины – фосфатиды, содержащие аминоспирт ХОЛИН.
- 37. Скачать презентацию
















 Формування поняття про окисно-відновні реакції в процес і вивчення шкільного курсу хімії
Формування поняття про окисно-відновні реакції в процес і вивчення шкільного курсу хімії Табиғи нанокристалдар
Табиғи нанокристалдар Гетероатомные соединения нефти
Гетероатомные соединения нефти Що ховається за цифрами? Харчові домішки
Що ховається за цифрами? Харчові домішки Химическая связь
Химическая связь Химия и повседневная жизнь человека
Химия и повседневная жизнь человека Воспользуйтесь ЛСМ Химические реакции
Воспользуйтесь ЛСМ Химические реакции Классификация химических реакций по тепловому эффекту
Классификация химических реакций по тепловому эффекту Детонаційна стійкість бензину
Детонаційна стійкість бензину Фазовые и агрегатные состояния полимеров
Фазовые и агрегатные состояния полимеров Химические свойства основных классов неорганических веществ
Химические свойства основных классов неорганических веществ Строение и свойства металлов. Физические и механические свойства металлов
Строение и свойства металлов. Физические и механические свойства металлов Аминокислоты алифатического ряда и их производные
Аминокислоты алифатического ряда и их производные Берилій
Берилій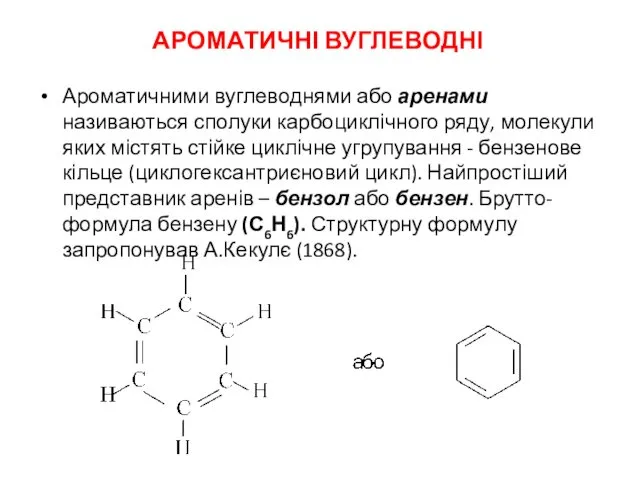 Ароматичні вуглеводні
Ароматичні вуглеводні Соляная кислота. Хлориды
Соляная кислота. Хлориды Изотопная геохимия
Изотопная геохимия Фракционирование клеточных экстрактов
Фракционирование клеточных экстрактов Химия, как часть естествознания. Предмет химии
Химия, как часть естествознания. Предмет химии Количественный анализ. Титриметрический анализ
Количественный анализ. Титриметрический анализ Химический состав клетки. Неорганические вещества
Химический состав клетки. Неорганические вещества Обратимость химических реакций. Обратимые и необратимые химические реакции. Химическое равновесие
Обратимость химических реакций. Обратимые и необратимые химические реакции. Химическое равновесие Эквиваленты веществ. Жидкое состояние, растворы
Эквиваленты веществ. Жидкое состояние, растворы Основания. 8 класс
Основания. 8 класс Нанотехнологии и Наноматериалы
Нанотехнологии и Наноматериалы Образование ионов
Образование ионов Спирты одноатомные и многоатомные
Спирты одноатомные и многоатомные Нуклеин қышқылдары
Нуклеин қышқылдары