Содержание
- 2. ЧТО ТАКОЕ ОСНОВАНИЯ? Основания- сложные вещества, состоящие из атома металла, связанного с одной или несколькими гидроксогруппами
- 4. Общая формула оснований: Ме(ОН)n, где Ме - металл n-число гидроксогрупп и одновременно валентность металла.
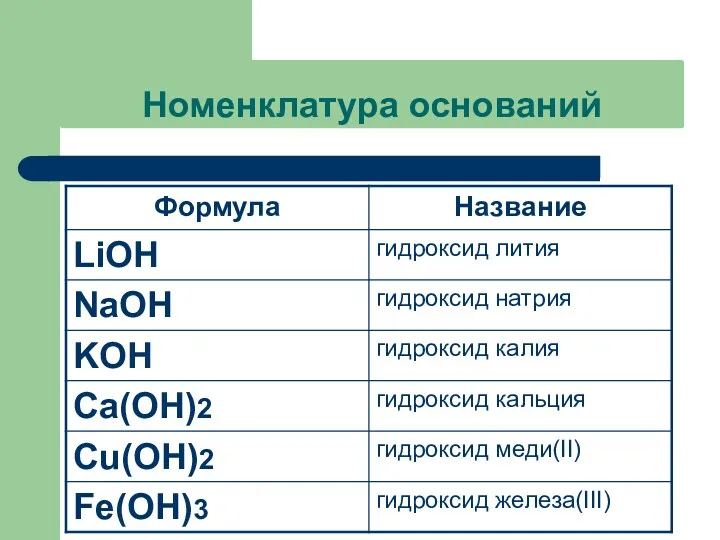
- 5. Номенклатура оснований Название оснований= Гидроксид + название металла в родительном падеже + валентность римскими цифрами (переменная)
- 6. Номенклатура оснований
- 7. Например: Fе(ОН)3 Гидроксид железа (ΙΙΙ) Ва(ОН)2 Гидроксид бария
- 8. Дайте названия гидроксидам: LiOH Ba(OH)2 Fe(OH)2 Al(OH)3 NaOH гидроксид лития гидроксид бария гидроксид железа (II) гидроксид
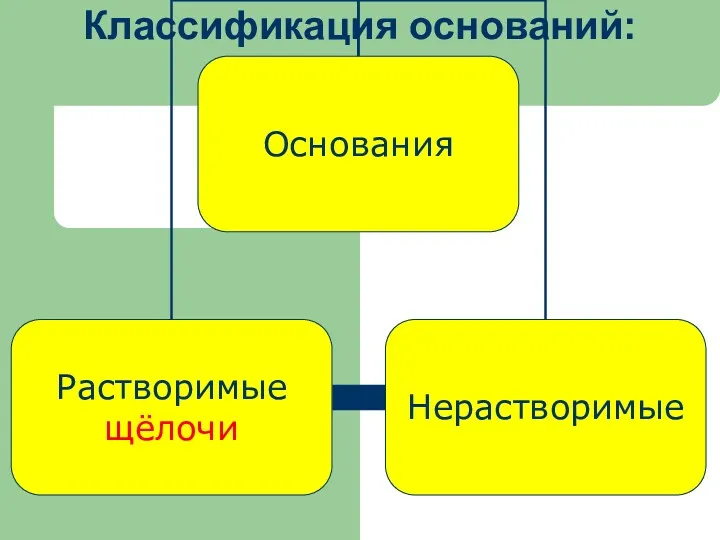
- 9. Классификация оснований:
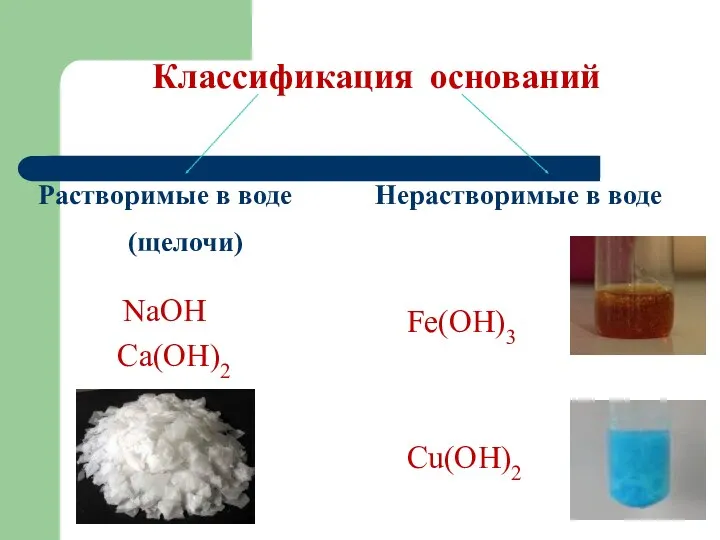
- 10. Классификация оснований Растворимые в воде (щелочи) Нерастворимые в воде NaOH Ca(OH)2 Fe(OH)3 Сu(OH)2
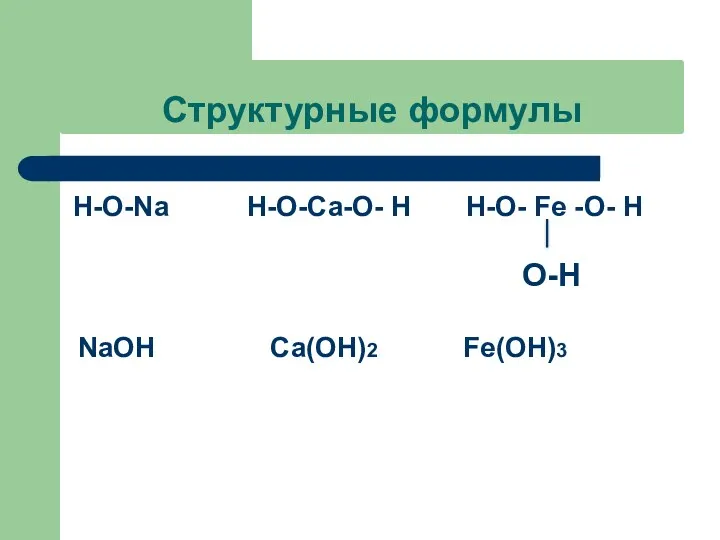
- 11. Структурные формулы Н-О-Na Н-О-Ca-О- Н Н-О- Fe -О- Н NaOH Ca(OH)2 Fe(OH)3 O-H
- 12. Физические свойства Основания - твердые кристаллические вещества. В воде растворимы щелочи: LiOH , NaOH, KOH, CsOH,
- 13. Физические свойства Основания – твердые вещества. Щелочи растворяются в воде ( к ним относят основания металлов
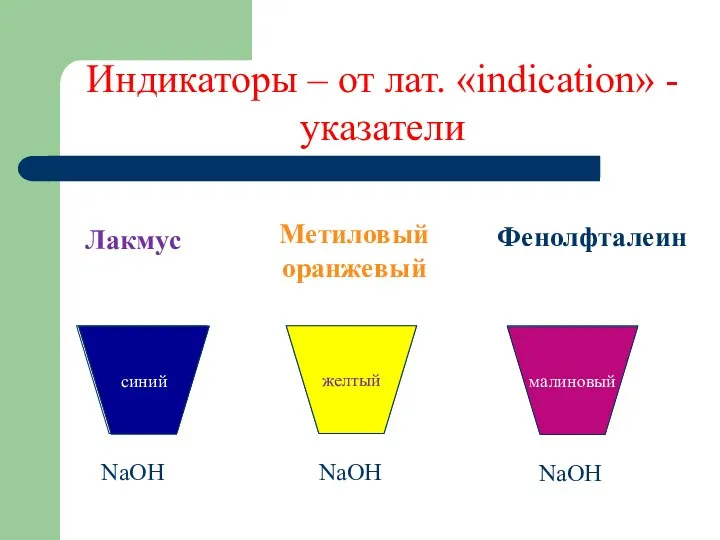
- 14. Индикаторы – от лат. «indication» - указатели NaOH NaOH NaOH Лакмус Метиловый оранжевый Фенолфталеин желтый малиновый
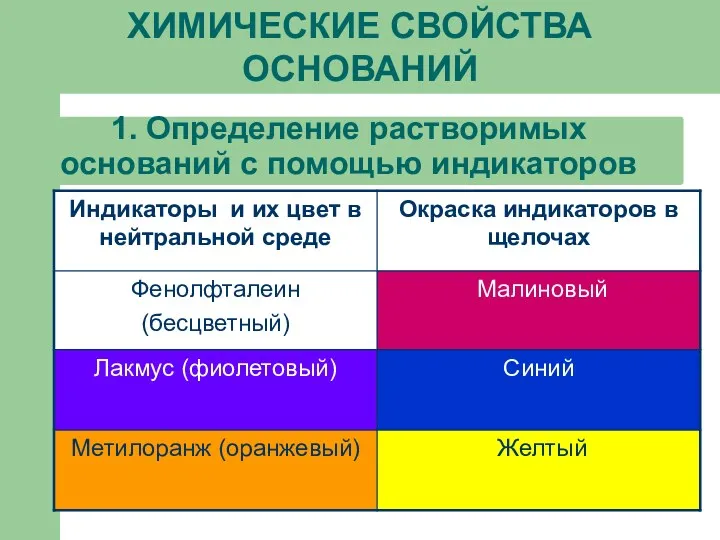
- 15. 1. Определение растворимых оснований с помощью индикаторов ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ
- 16. ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ 2.Взаимодействие с кислотами Основание+кислота=соль+вода KOH+HCl=KCl+H2O Cu(OH)2+2HCl=CuCl2+2H2O
- 17. Взаимодействие с кислотами: 2NaOH + H2SO4 → Na2SO4 + 2H2O реакция нейтрализации
- 18. Cu(OH)2↓+ H2SO4 → CuSO4 +2 H2O
- 19. ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ 3.Взаимодействие с кислотными оксидами Основание+кислотный оксид=соль+вода 2KOH+CO2=K2CO3+H2O
- 20. Взаимодействие с кислотными оксидами Са(ОН)2 + СО2 → СаСО3↓ + Н2О реакция обмена
- 21. ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ 4.Взаимодействие с амфотерными оксидами Основание+ амфотерный оксид=соль+вода 2KOH+ZnO=K2ZnO2+H2O
- 22. ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ 5.Взаимодействие с солями, если образуется малорастворимая соль или малорастворимое основание!!! Основание+соль1=основание2+соль2 2NaOH+CuCl2=Cu(OH)2 +
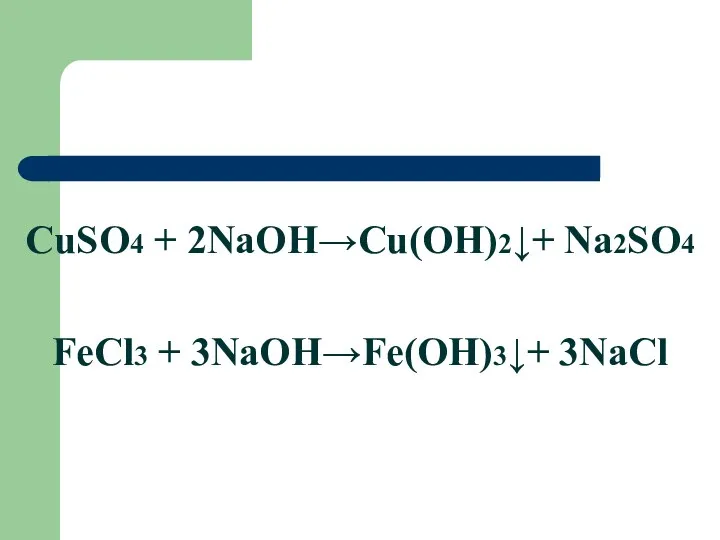
- 23. CuSO4 + 2NaOH→Cu(OH)2↓+ Na2SO4 FeCl3 + 3NaOH→Fe(OH)3↓+ 3NaCl
- 24. ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ 6.При нагревании разлагаются (кроме LiOH): Cu (OH)2 = CuO+H2O Только для нерастворимых оснований!!!
- 25. Отношение оснований к нагреванию Cu(OH)2 → CuO↓ + H2O t
- 26. ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ 7. Амфотерные гидроксиды Al(OH)3, Zn(OH)2, Be(OH)2, Fe(OH)3 и другие взаимодействуют с кислотами Zn
- 27. Важнейшие представители и их применение NaOH, KOH, Ca(OH)2: твердые, очень едкие вещества, растворимые в воде, мылкие
- 28. Щелочи в быту Гидроксид натрия, техническое название едкий натр или каустическая сода. Едкий натр кристаллическое вещество
- 31. ЗАГАДКА Я растворчик изучал. Лакмус в нем синее стал. Поглощал раствор тотчас Кислый углекислый газ! Про
- 32. ЗАГАДКА Капля воды попала на кусок и превратилась в кипяток.
- 34. Задание Не является щёлочью : 1)NaOH; 2)Ca(OH)2; 3)Mg(OH)2; 4)KOH.
- 39. Скачать презентацию





























 Стратегия химической промышленности
Стратегия химической промышленности Chemical reaction rate. Influence of conditions on the rate of chemical reactions. Catalysis. Topic 3.2
Chemical reaction rate. Influence of conditions on the rate of chemical reactions. Catalysis. Topic 3.2 Химия в повседневной жизни человека
Химия в повседневной жизни человека Емтихан сұрақтары
Емтихан сұрақтары Managing chemicals. Green chemistry for every laboratory
Managing chemicals. Green chemistry for every laboratory Классификация химических реакций
Классификация химических реакций 20230419_azot
20230419_azot Органикалық қосылыстар
Органикалық қосылыстар Хозяйственные товары из пластических масс
Хозяйственные товары из пластических масс Металлы побочных подгрупп
Металлы побочных подгрупп Периодический закон и система элементов Д.И. Менделеева
Периодический закон и система элементов Д.И. Менделеева Минералы горных пород
Минералы горных пород Охрана труда в кабинете (лаборатории) химии образовательного учреждения
Охрана труда в кабинете (лаборатории) химии образовательного учреждения Водородная связь
Водородная связь Хроматография. Классификации хроматографических методов
Хроматография. Классификации хроматографических методов Амины. Анилин
Амины. Анилин Шкала не Мооса
Шкала не Мооса Растворы. Лекция №4
Растворы. Лекция №4 Оценка опасности взрыва горючих газов
Оценка опасности взрыва горючих газов Хімічні властивості насичених одноатомних спиртів. Одержання етанолу
Хімічні властивості насичених одноатомних спиртів. Одержання етанолу Нефть, её производство, авиационное и дизельное топливо
Нефть, её производство, авиационное и дизельное топливо Органическая химия. Лекция 13
Органическая химия. Лекция 13 Положение металлов в периодической системе. Металлическая связь. Металлическая решетка. Общие физические свойства металлов
Положение металлов в периодической системе. Металлическая связь. Металлическая решетка. Общие физические свойства металлов Вуглеводні. Підсумковий урок 9 клас
Вуглеводні. Підсумковий урок 9 клас Химия. D-элементтер
Химия. D-элементтер сложные эфиры
сложные эфиры Күрделі белоктар
Күрделі белоктар Простые вещества. Сложные вещества
Простые вещества. Сложные вещества