Содержание
- 2. Нахождение в природе Положение в ПСХЭ Физические свойства Химические свойства Получение Применение Соединения Mn ?
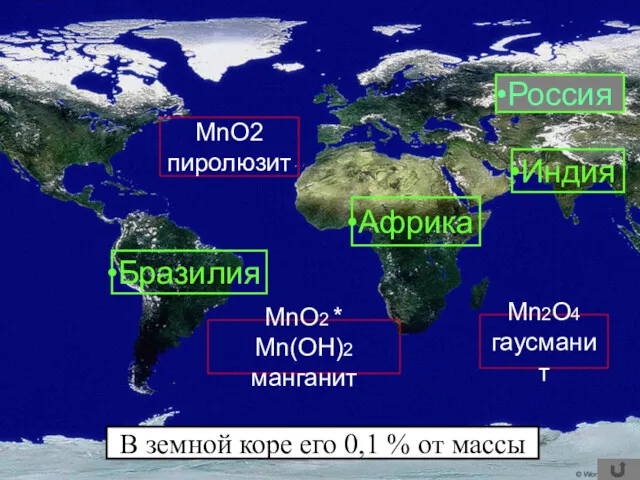
- 3. MnO2 пиролюзит Mn2O4 гаусманит MnO2 * Mn(OH)2 манганит В земной коре его 0,1 % от массы
- 4. хрупкий металл твердый т КИП = 2150 º С плотность = 7,44г/см³ Т ПЛАВ = 1245
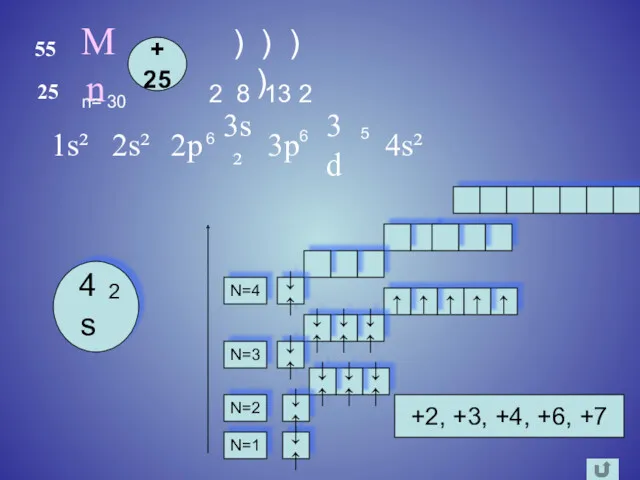
- 5. Mn 55 25 + 25 ) ) ) ) 1s² 2 8 13 2 2s² 2p
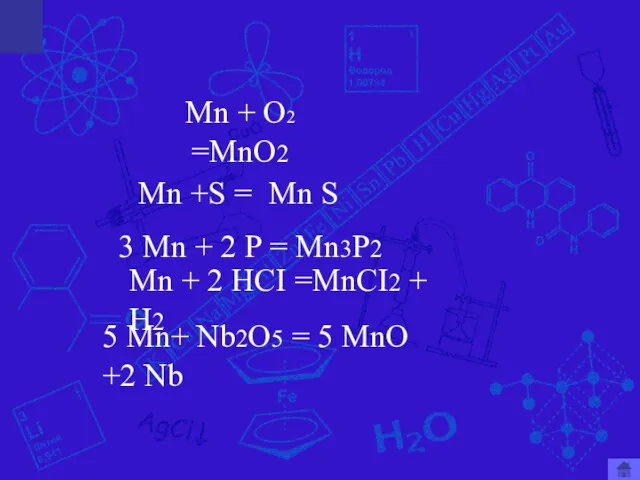
- 6. Mn + O2 =MnO2 Mn +S = Mn + 2 HCI =MnCI2 + H2 Mn S
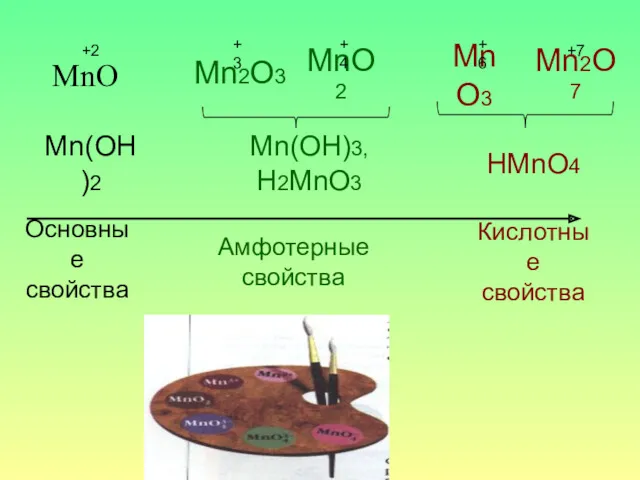
- 7. MnO +2 Mn2O3 MnO2 Mn2O7 Mn(OH)2 Mn(OH)3, H2MnO3 HMnO4 Основные свойства Амфотерные свойства Кислотные свойства +3
- 8. Важнейшие соединения Перманганаты: 2 KMnO4 = K2MnO4 +MnO2 +O2 Манганаты t
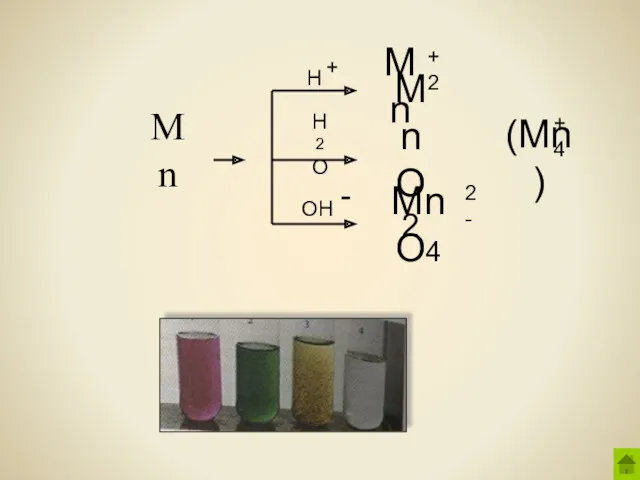
- 9. Mn H H2O OH Mn +2 MnO2 (Mn ) +4 MnO4 2- + -
- 10. Алюминотермия 3MnO2+4AI=2AI2O3+3Mn В промышленности: Электролиз солей
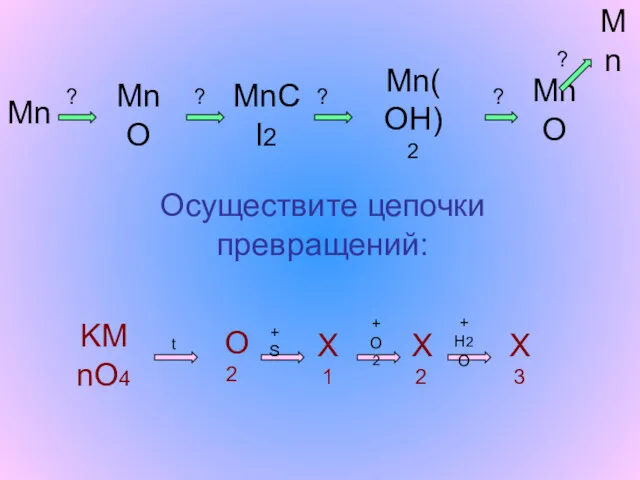
- 12. Mn MnO MnCl2 Mn(OH)2 MnO Mn KMnO4 O2 X1 X2 X3 Осуществите цепочки превращений: +S +O2
- 14. Скачать презентацию





 Классификация химических реакций в неорганической химии
Классификация химических реакций в неорганической химии Химические свойства металлов
Химические свойства металлов Гетероциклды қосылыстар. Алкалоидтар
Гетероциклды қосылыстар. Алкалоидтар Классы органических соединений
Классы органических соединений Применение здм к кислотно-основным равновесиям и их роль в аналитической химии
Применение здм к кислотно-основным равновесиям и их роль в аналитической химии Дисперсные системы
Дисперсные системы Електролітична дисоціація
Електролітична дисоціація Явище ізомерії. Структурна ізомерія, номенклатура насичених вуглеводнів
Явище ізомерії. Структурна ізомерія, номенклатура насичених вуглеводнів Основы коррозии и защиты металлов. Методы исследования коррозии
Основы коррозии и защиты металлов. Методы исследования коррозии Кислородсодержащие соединения азота
Кислородсодержащие соединения азота Актиноиды. Физические и химические свойства
Актиноиды. Физические и химические свойства Сложные эфиры
Сложные эфиры Respiration Module
Respiration Module Синтетические моющие средства
Синтетические моющие средства Катионы IV аналитической группы
Катионы IV аналитической группы Генетическая связь между классами неорганических веществ. 8 класс
Генетическая связь между классами неорганических веществ. 8 класс Бытовая химия
Бытовая химия Стекловолокно. Что такое стекловолокно?
Стекловолокно. Что такое стекловолокно? Создание косметических средств
Создание косметических средств Фазовые равновесия и учение о растворах
Фазовые равновесия и учение о растворах Серная кислота и её свойства
Серная кислота и её свойства Періодичний закон і періодична система хімічних елементів Д.І. Менделєєва. Будова атома
Періодичний закон і періодична система хімічних елементів Д.І. Менделєєва. Будова атома Химический элемент, минерал, горная порода. (Лекция 6)
Химический элемент, минерал, горная порода. (Лекция 6) Щелочноземельные металлы
Щелочноземельные металлы Химия и повседневная жизнь человека
Химия и повседневная жизнь человека Кислоты, их классификация и свойства
Кислоты, их классификация и свойства Ендотермічні реакції на службі людини
Ендотермічні реакції на службі людини Электроотрицательность химических элементов
Электроотрицательность химических элементов