Содержание
- 2. Только в свободном (самородном) виде (благородные металлы - золото, платина); В самородном виде и в виде
- 6. Железный метеорит
- 9. Галенит PbS Киноварь HgS Пирит FeS2 И др. Сульфиды металлов
- 10. Сильвин KCl Галит NaCl Сильвинит KCl • NaCl Карналлит KCl • MgCl2 • 6H2O И др.
- 11. Сульфаты, фосфаты, карбонаты Барит BaSO4 Апатит Ca5(PO4)3(F,CI) Мрамор CaCO3 Магнезит MgCO3 Малахит Cu2(OH)2CO3 И др.
- 12. Оксиды Магнетит Fe3O4 Гематит Fe2O3 Каолин Al2O3 • 2SiO2 • 2H2O И др.
- 13. Минералы и горные породы, содержащие металлы и их соединения и пригодные для промышленного получения металлов, называются
- 15. Металлургия. Металлургия – наука о промышленных способах получения металлов из природного сырья. Металлургия делится на три
- 16. Пирометаллургия. Пирометаллургия – это получение металлов из природных руд реакциями восстановления при высокой температуре.
- 17. Получение из оксидов. 1) Восстановление углеродом. ZnO + C Zn + CO 2) Восстановление угарным газом.
- 18. 3) Восстановление водородом. Cr2O3 + 3H2 → 2Cr + 3H2O WO3 + 3H2 W + 3H2O
- 19. Алюмотермия 4) 3MnO2 + 4Al 3Mn + 2Al2O3 Таким способом получают Mn, Cr, Ti, Mo, W
- 20. Получение из сульфидов. Получение происходит по схеме: сульфиды оксиды металлы
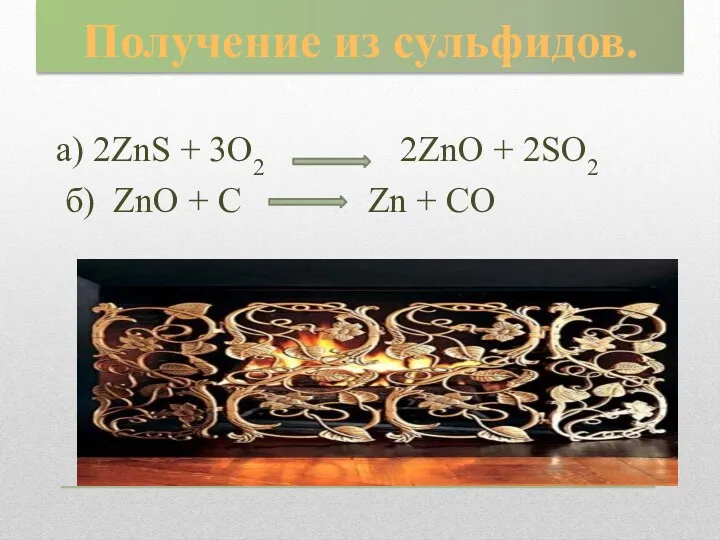
- 21. Получение из сульфидов. а) 2ZnS + 3O2 2ZnO + 2SO2 б) ZnO + C Zn +
- 22. Гидрометаллургия. Гидрометаллургия – получение металлов из растворов их солей. Получение происходит по схеме: Руда раствор соли
- 23. а) CuO + H2SO4(р-р) CuSO4 + H2O б)CuSO4 + Fe FeSO4 + Cu Таким способом получают
- 24. Электрометаллургия. Электрометаллургия – получение металлов с помощью электрического тока (электролиз). 2NaCl Na0 + Cl20 Таким способом
- 26. Скачать презентацию




















 Растворы: состав и их коллигативные свойства
Растворы: состав и их коллигативные свойства Методы прямого секвенирования белков (пептидов)
Методы прямого секвенирования белков (пептидов) Петрология. Классификации магматических горных пород
Петрология. Классификации магматических горных пород Железоуглеродистый сплав чугун
Железоуглеродистый сплав чугун Chemical reactions and heat. (Chapter 1)
Chemical reactions and heat. (Chapter 1) Ступінь окиснення. Визначення ступеня окиснення елемента за хімічною формулою сполуки. Складання формули сполуки
Ступінь окиснення. Визначення ступеня окиснення елемента за хімічною формулою сполуки. Складання формули сполуки Количество вещества. Единица измерения вещества моль
Количество вещества. Единица измерения вещества моль Неметаллы – простые вещества
Неметаллы – простые вещества Алкадиены. Актуализация ранее полученных знаний
Алкадиены. Актуализация ранее полученных знаний Массовая доля элемента в веществе
Массовая доля элемента в веществе Получение и применение альдегидов
Получение и применение альдегидов Побутові хімікати
Побутові хімікати Хімічна рівновага
Хімічна рівновага Растворы ВМС
Растворы ВМС Генетическая связь неорганических соединений
Генетическая связь неорганических соединений Химическая связь в кристаллах
Химическая связь в кристаллах Кристаллическая структура твердых тел. Межатомные взаимодействия и классификация твердых тел
Кристаллическая структура твердых тел. Межатомные взаимодействия и классификация твердых тел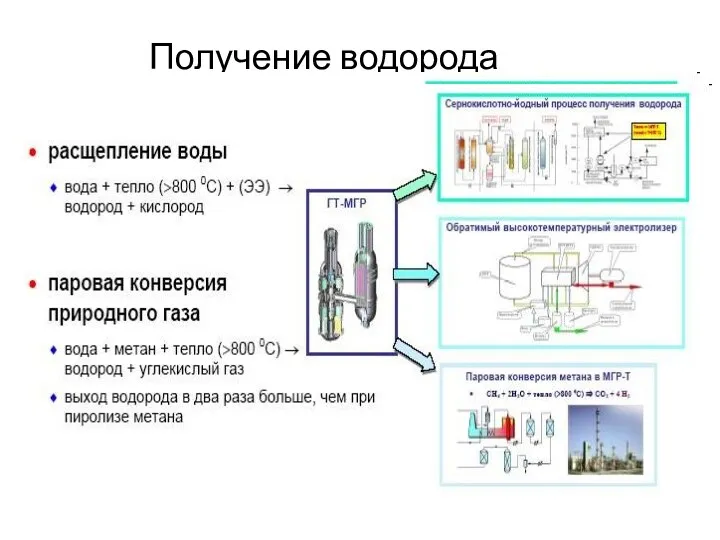 Получение водорода
Получение водорода Алкадиены (диены, диеновые углеводороды)
Алкадиены (диены, диеновые углеводороды)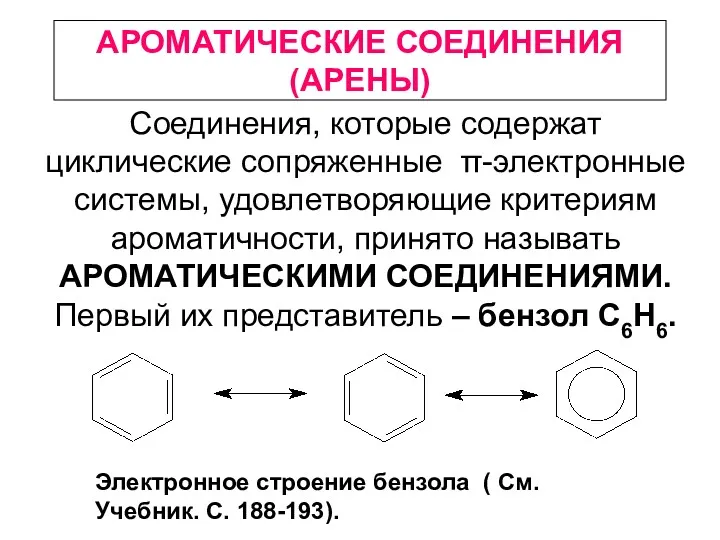 Ароматические соединения (арены)
Ароматические соединения (арены) Концентрация кобальта
Концентрация кобальта Цинк и его соединения
Цинк и его соединения Закон сохранения массы веществ. Химические уравнения
Закон сохранения массы веществ. Химические уравнения Соли. Классификация и свойства солей
Соли. Классификация и свойства солей Дисперсные системы
Дисперсные системы Типы химических реакций. Систематизация и обобщение знаний
Типы химических реакций. Систематизация и обобщение знаний Granite
Granite 20231113_tipy_him._reaktsiy_prezentatsiya
20231113_tipy_him._reaktsiy_prezentatsiya