Содержание
- 2. Обобщение по теме «Неметаллы» Разминка Прочитать формулы, назвать вещества: H2SiO3, P2O5, Na3PO4, CaCO3, SiO2, H3PO4, KHSiO3,
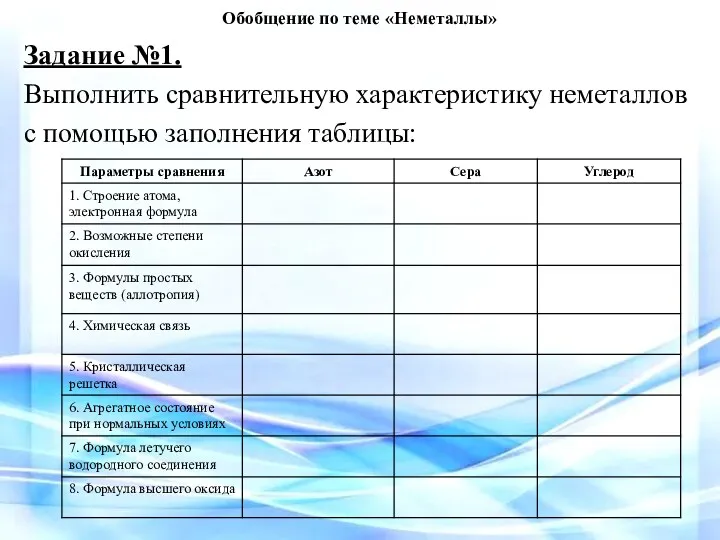
- 3. Обобщение по теме «Неметаллы» Задание №1. Выполнить сравнительную характеристику неметаллов с помощью заполнения таблицы:
- 4. Обобщение по теме «Неметаллы» Задание №2 (ОГЭ №1). Четыре электрона находятся во внешнем электронном слое атомов
- 5. Обобщение по теме «Неметаллы» Задание №2 (ОГЭ №1). Химический элемент, в атомах которого распределение электронов по
- 6. Обобщение по теме «Неметаллы» Задание №2 (ОГЭ №1). Атомы химических элементов, находящиеся в одной группе в
- 7. Обобщение по теме «Неметаллы» Задание №3 (ОГЭ №2). В каком ряду химических элементов ослабевают неметаллические свойства
- 8. Обобщение по теме «Неметаллы» Задание №3 (ОГЭ №2). Наибольшей окислительной активностью обладает: 1) Na 2) Cu
- 9. Обобщение по теме «Неметаллы» Задание №3 (ОГЭ №2). Свойства оксидов в ряду SO3 → Р2O3 →
- 10. Обобщение по теме «Неметаллы» Задание №4 (ОГЭ №3, 4, 5). Назвать вещества, указать класс, вид химической
- 11. Обобщение по теме «Неметаллы» Задание №4. Проклассифицировать кислоты по всем изученным признакам, расставить степени окисления каждого
- 12. Обобщение по теме «Неметаллы» Задание №5. Какая схема генетического ряда неМе неточная? Почему?: 1) Si →
- 13. Обобщение по теме «Неметаллы» Задание №5 (ОГЭ №9-12). Какая реакция возможна? 1) O2 + Cl2 →
- 14. Обобщение по теме «Неметаллы» Задание №6 (ОГЭ №9-12). Закончить и проклассифицировать химическую реакцию по всем возможным
- 15. Обобщение по теме «Неметаллы» Задание №7 (ОГЭ №15). Массовая доля серы в сульфате алюминия равна 1)
- 16. Обобщение по теме «Неметаллы» Экспериментальная задача №8 (ОГЭ №18). Определить в какой из пробирок находятся хлорид
- 17. Обобщение по теме «Неметаллы» Задание №9 (ОГЭ №20). Используя метод электронного баланса, составьте уравнение реакции: 1)
- 19. Скачать презентацию















 Летучие яды. Токсичные газы
Летучие яды. Токсичные газы Галогены. Астат
Галогены. Астат Минеральные удобрения
Минеральные удобрения Iron Oxide
Iron Oxide Алкадиены или диеновые углеводороды
Алкадиены или диеновые углеводороды Історія відкриття періодичної системи хімічних елементів
Історія відкриття періодичної системи хімічних елементів Азотсодержащие органические соединения. Амины. Анилинароматический амин
Азотсодержащие органические соединения. Амины. Анилинароматический амин Бета-окисление жирных кислот
Бета-окисление жирных кислот Окислительно - восстановительные реакции (ОВР) (часть 1)
Окислительно - восстановительные реакции (ОВР) (часть 1) Химические свойства карбоновых кислот
Химические свойства карбоновых кислот Углерод. Аллотропные модификации
Углерод. Аллотропные модификации Свойства НЦ
Свойства НЦ Сероводород, сульфиды
Сероводород, сульфиды Валентність хімічного елемента
Валентність хімічного елемента Концентрация растворов. Массовая доля растворенного вещества. Урок 1
Концентрация растворов. Массовая доля растворенного вещества. Урок 1 Относительная атомная и молекулярная массы
Относительная атомная и молекулярная массы Основания. Классификация оснований
Основания. Классификация оснований Дизельное топливо
Дизельное топливо Каучук и резина
Каучук и резина Валентність хімічних елементів
Валентність хімічних елементів Кристаллическое строение металлов и сплавов
Кристаллическое строение металлов и сплавов Металлы и сплавы, их строение. Классификация и маркировка сталей. Влияние химических элементов на свариваемость
Металлы и сплавы, их строение. Классификация и маркировка сталей. Влияние химических элементов на свариваемость Химические волокна
Химические волокна Колебания кристаллической решетки и ее тепловые свойства. Тепловые свойства
Колебания кристаллической решетки и ее тепловые свойства. Тепловые свойства Железо и его соединения
Железо и его соединения Учение о растворах
Учение о растворах Кислоты. Классификация кислот по строению кислотного остатка
Кислоты. Классификация кислот по строению кислотного остатка Драгоценные камни
Драгоценные камни