Содержание
- 2. Теоретические задачи курса Рассмотрение различных способов модификации поверхностей адсорбционное модифицирование (физическая адсорбция и хемосорбция) 2. Исследование
- 3. Популярные задачи промышленности: Подобрать стабилизатор(ы) и получить кинетически- и термодинамически- устойчивые дисперсии. Примеры (кафедральных проектов/грантов/договоров): получение
- 4. Температуры фазовых переходов веществ и поверхностное натяжение Избыточная энергия модифицируемой поверхности определяется природой вещества, типом связи
- 5. Термодинамика поверхности 1 Дебай = 3,3*10-30 Кл*м
- 6. Таблица 1а. Составляющие поверхностного натяжения некоторых жидкостей на границе с воздухом Составляющие пов. энергии поверхностей
- 7. Составляющие поверхностного натяжения некоторых жидкостей на границе с воздухом
- 8. адгезия между двумя несмешивающимися жидкостями (приближение Фоукса). Термодинамика адгезии
- 9. В общем виде, межфазное натяжение (interface tension) для любых двух несмешивающихся жидкостей Пример: н-гексан: имеется только
- 10. Термодинамическое уравнение адгезии. Уравнение Дюпре
- 11. Уравнение Юнга S - слюда
- 12. Вода вокруг гидрофобной трубки
- 13. Адгезия жидкостей к твердым поверхностям
- 14. Энергия взаимодействия жидкостей с твердыми поверхностями
- 15. Дисперсионная и полярная составляющие свободной поверхностной энергии некоторых полимеров (тв.) при комнатной температуре
- 16. Адгезия частиц в дисперсиях суммарное изменение энергии Гиббса (численно равно работе адгезии, W) при взаимодействии двух
- 17. Межфазная энергия, работа адгезии Оценка константы Гамакера и расчет полной энергии взаимодействия между частицами требуют учета
- 18. Типичное состояние металлической поверхности без предварительной обработки и очистки
- 19. Поверхности металлов
- 20. Окисление поверхностей на воздухе
- 21. Увеличение адгезии при обработке поверхности. Сдвиговая прочность адгезионного соединения на эпоксидном связующем
- 22. Классификация типов обработки поверхности Удаление загрязнений Усиление адгезии/защита поверхности
- 23. Очистка растворителями Cutting oil = СОЖ и т.д. Смотреть, чтоб не растворился субстрат (для пластиков и
- 24. Кислотная обработка Хромовая кислота - для очистки полиолефинов
- 25. Составы и способы химической обработки при подготовке поверхностей. Металлы Copyright ©2009 The Adhesive and Sealant Council,
- 26. Пластики
- 27. Использование праймеров и промотеров адгезии Задачи: Изменить поверхностную энергию субстрата Промотировать химическую реакцию между адгезивом и
- 29. Скачать презентацию
 Альтернативная бытовая химия
Альтернативная бытовая химия Легированные стали
Легированные стали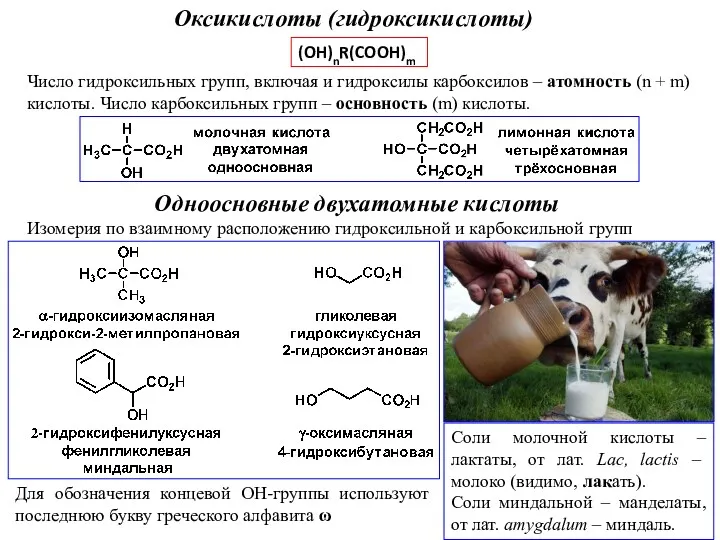 Оксикислоты (гидроксикислоты)
Оксикислоты (гидроксикислоты) Vi топ элементтері. Оттегі, күкірт қасиеттері және қосылыстары
Vi топ элементтері. Оттегі, күкірт қасиеттері және қосылыстары Электрохимия. Окислительно-восстановительные реакции
Электрохимия. Окислительно-восстановительные реакции Анализ качества лекарственных веществ, определяемых методом комплексонометрии
Анализ качества лекарственных веществ, определяемых методом комплексонометрии Соляные породы
Соляные породы Ионы. Проверочная работа
Ионы. Проверочная работа Основные свойства и механизмы упрочнения КМ
Основные свойства и механизмы упрочнения КМ Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Классы неорганических веществ
Классы неорганических веществ Биохимия
Биохимия Основания. Степени окисления элементов в соединениях
Основания. Степени окисления элементов в соединениях Галогены
Галогены Энергетический обмен
Энергетический обмен Побочная подгруппа VI группы периодической системы
Побочная подгруппа VI группы периодической системы Соли аммония
Соли аммония Экстракция. Понятия в экстракции
Экстракция. Понятия в экстракции Высокоэффективная жидкостная хроматография 1
Высокоэффективная жидкостная хроматография 1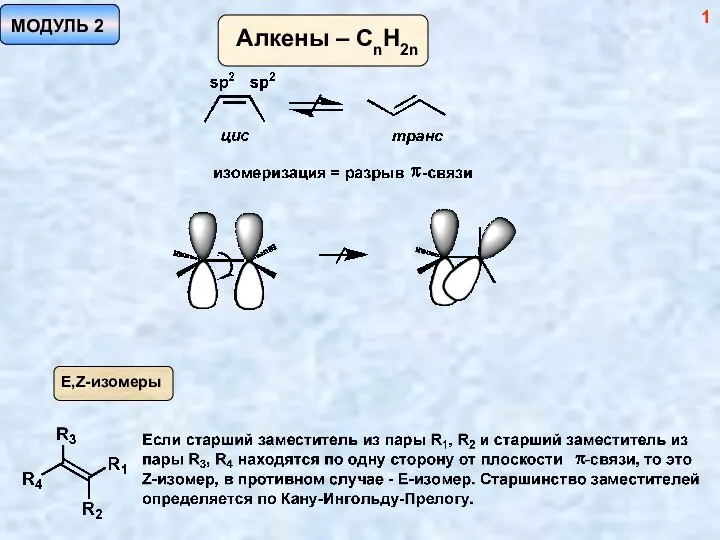 Методы синтеза алкенов. (Модуль 2)
Методы синтеза алкенов. (Модуль 2) Галогены. Получение и применение галогенов
Галогены. Получение и применение галогенов Кислоты. Классификация неорганических веществ
Кислоты. Классификация неорганических веществ Геохимия стабильных изотопов, Радиоуглеродный метод
Геохимия стабильных изотопов, Радиоуглеродный метод Оксиды. Номенклатура, классификация, физические свойства
Оксиды. Номенклатура, классификация, физические свойства Эко-упаковка
Эко-упаковка Вчення про розчини. Рівновага в розчинах електролітів
Вчення про розчини. Рівновага в розчинах електролітів Оксиды
Оксиды Катализ и катализаторы
Катализ и катализаторы