Слайд 2

Серная кислота H2SO4 :
сильная двухосновная кислота, отвечающая высшей степени окисления серы (+6).
тяжёлая маслянистая жидкость без цвета и запаха
в технике серной кислотой называют её смеси как с водой, так и с серным ангидридом SO3.
Слайд 3

бесцветная маслянистая жидкость
Кислота серная техническая.
Слайд 4

Структурная формула серной кислоты
Сырьём для получения серной кислоты служат
сера
сульфиды металлов
сероводород
отходящие газы теплоэлектростанций
сульфаты железа
кальция
Слайд 5

Основные стадии получения серной кислоты:
Обжиг сырья с получением SO2
Окисление SO2 в SO3
Абсорбция SO3
В промышленности применяют
два метода окисления SO2 в производстве серной кислоты:
контактный — с использованием твердыхкатализаторов(контактов)
нитрозный — с оксидами азота.
Слайд 6
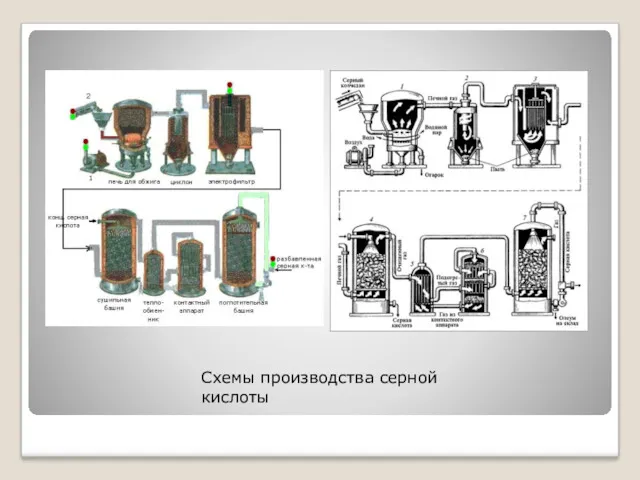
Схемы производства серной кислоты
Слайд 7

реакции по производству серной кислоты из минерала пирита на катализаторе — оксиде
ванадия (V).
4FeS2 + 11O2 = 2Fe2O3 + 8SO2
2SO2 + O2 (V2O5) → 2SO3
Нитрозный метод получения серной кислоты
SO2 + NO2 → SO3 + NO↑.
2NO+O2 → 2NO2
Слайд 8

При реакции SO3 с водой выделяется огромное количество теплоты и серная кислота начинает закипать
с образованием "туманов"
SO3 + H2O = H2SO4 + Q Поэтому SO3смешивается с H2SO4, образуя раствор SO3 в 91% H2SO4 - олеум
Получение серной кислоты из железного купороса - термическое разложение сульфата железа (II) с последующим охлаждением смеси
2FeSO4·7H2O→Fe2O3+SO2+H2O+O2
SO2+H2O+O2 ⇆ H2SO4
Слайд 9

Естественные источники серной кислоты








 Эндогенная серия. Альбитит-грейзеновая группа
Эндогенная серия. Альбитит-грейзеновая группа Алюминий, его амфотерные свойства
Алюминий, его амфотерные свойства Крахмал. Физические свойства
Крахмал. Физические свойства Оксид углерода II. Угарный газ
Оксид углерода II. Угарный газ Нано-порошки. Способы получения нано-порошков
Нано-порошки. Способы получения нано-порошков Функциональные производные с простой связью C-“Э. Галогенпроизводные. (Лекция 5)
Функциональные производные с простой связью C-“Э. Галогенпроизводные. (Лекция 5) Стратегия химической промышленности
Стратегия химической промышленности Своя игра Знаешь ли ты химические элементы?
Своя игра Знаешь ли ты химические элементы? Олимпиадные задачи муниципального этапа по химии
Олимпиадные задачи муниципального этапа по химии Хімічний зв'язок і будова речовини
Хімічний зв'язок і будова речовини Типы химических реакций
Типы химических реакций Виды химической связи
Виды химической связи Теплота горения
Теплота горения Химические свойства альдегидов
Химические свойства альдегидов Углеводородное сырье для промышленности органических веществ. Лекция 1. Часть 1
Углеводородное сырье для промышленности органических веществ. Лекция 1. Часть 1 Признаки химических реакций. (Практическая работа 5,4)
Признаки химических реакций. (Практическая работа 5,4) Галогены. Нахождение в природе
Галогены. Нахождение в природе Эквиваленты веществ. Жидкое состояние, растворы
Эквиваленты веществ. Жидкое состояние, растворы Природные источники углеводородов
Природные источники углеводородов Химия элементов VA группы (пниктогены или пникти́ды)
Химия элементов VA группы (пниктогены или пникти́ды) Биологически важные реакции карбонильных соединений. Масс-спектрометрия
Биологически важные реакции карбонильных соединений. Масс-спектрометрия Трансформация ионной химической связи в металлическую при восстановлении металлов в комплексных оксидах
Трансформация ионной химической связи в металлическую при восстановлении металлов в комплексных оксидах Бытовая химия
Бытовая химия Химия элементов VIA группы
Химия элементов VIA группы Р-элементы IV группы
Р-элементы IV группы Особенности сжигания газообразного топлива и топливосжигающие устройства
Особенности сжигания газообразного топлива и топливосжигающие устройства Использование информационных технологий при обучении химии
Использование информационных технологий при обучении химии Основы термической и химико-термической обработки стали. Теория и технология термической обработки стали. Лекция 3. Тема 7
Основы термической и химико-термической обработки стали. Теория и технология термической обработки стали. Лекция 3. Тема 7