Свеча – органическое вещество, содержащее углерод и водород. Оно является твердым
топливом. Растворение свечи является физическим процессом. А горение химическим процессом.
Над горящей восковой свечей удерживали перевернутый стакан, затем его опустили. Кобальтовая бумага находящаяся в стакане изменила цвет с синего до розового, что является признаком наличия воды. Если налить известковую воду в стакан, то она мутнеет, что является признаком наличия углекислого газа.
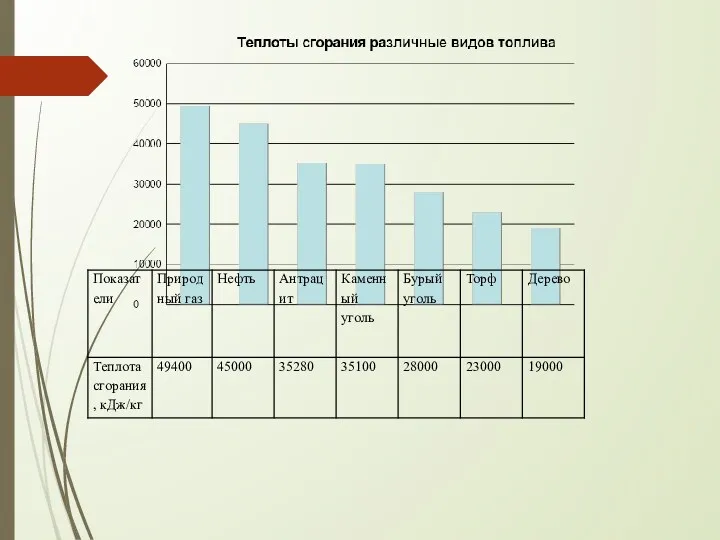
Топливо + кислород = диоксид углерода + вода
Углекислый газ + известковая вода→ помутнение
Кобальтовая бумага синего цвета + вода → цвет кобальтовой бумаги изменяется на розовый.











 Тамақ өнімдерінің құрылымын және физико-химиялық қасиеттерін өзгертетін тағамдық қоспалар
Тамақ өнімдерінің құрылымын және физико-химиялық қасиеттерін өзгертетін тағамдық қоспалар Чистые вещества и смеси
Чистые вещества и смеси Способы получения и очистки металлов
Способы получения и очистки металлов Кислоты. Классификация. Химические свойства. 8 класс
Кислоты. Классификация. Химические свойства. 8 класс Мыла и синтетические моющие срдства
Мыла и синтетические моющие срдства Валентность и степень окисления
Валентность и степень окисления Алкины. Ацетиленовые углеводороды
Алкины. Ацетиленовые углеводороды Основные физико-химические свойства нефти и нефтепродуктов
Основные физико-химические свойства нефти и нефтепродуктов Теория электролитической диссоциации
Теория электролитической диссоциации Минералы группы кварца
Минералы группы кварца Периодический закон и свойства химических элементов
Периодический закон и свойства химических элементов Металлические сплавы
Металлические сплавы КИСЛОРОД
КИСЛОРОД Формы выделения минералов
Формы выделения минералов Хімічні формули речовин
Хімічні формули речовин Классификация и свойства кислот
Классификация и свойства кислот Розділення неоднорідної суміші. Практична робота № 2
Розділення неоднорідної суміші. Практична робота № 2 Альдегидтер
Альдегидтер Organic compounds: nomenclature
Organic compounds: nomenclature Ступінь окиснення. Визначення ступеня окиснення елемента за хімічною формулою сполуки
Ступінь окиснення. Визначення ступеня окиснення елемента за хімічною формулою сполуки Координационные соединения
Координационные соединения Менделеевские уроки. День науки
Менделеевские уроки. День науки Природные источники углеводородов и их переработка
Природные источники углеводородов и их переработка Окислительно-востановительные реакции в растворах
Окислительно-востановительные реакции в растворах Применение закона действующих масс к гетерогенным равновесиям. Ионное произведение растворимости. (Лекция 5)
Применение закона действующих масс к гетерогенным равновесиям. Ионное произведение растворимости. (Лекция 5) Electronică aplicată. (Curs 2)
Electronică aplicată. (Curs 2) Химические свойства солей
Химические свойства солей Терминология и основные понятия в химии высокомолекулярных соеденений
Терминология и основные понятия в химии высокомолекулярных соеденений