Содержание
- 2. 2.1 Открытие периодического закона
- 3. "Легко предположить, что ныне пока нет еще возможности доказать… что атомы простых тел суть сложные вещества,
- 4. 2.2 Предпосылки открытия строения атома 1878 г. – опыты с катодными лучами
- 5. Опыты Перрена
- 8. А.Г. Столетов – доказал, что электроны есть во всех атомах
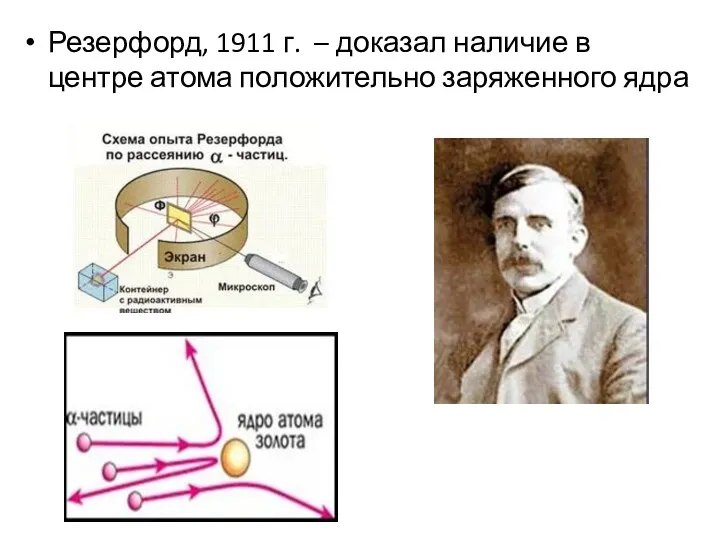
- 10. Резерфорд, 1911 г. – доказал наличие в центре атома положительно заряженного ядра
- 11. 2.3 Модели строения атома Томсон, «Капельная» модель (арбуз), 1903 г. Положительный заряд равномерно распределен в объеме
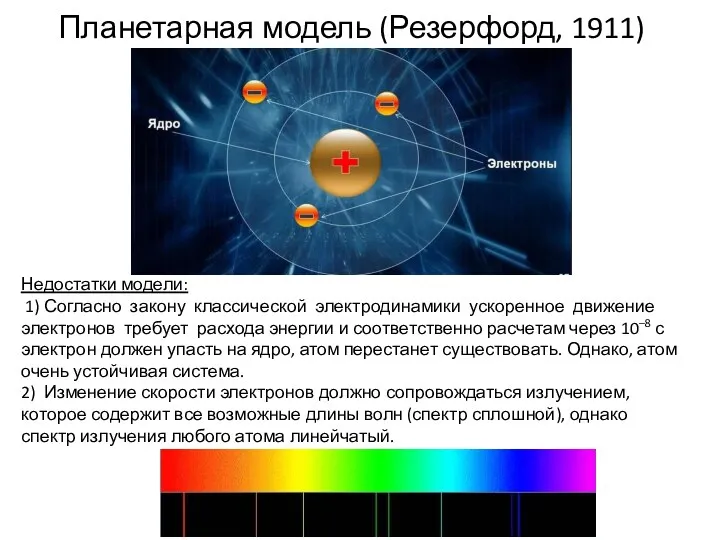
- 12. Планетарная модель (Резерфорд, 1911) Недостатки модели: 1) Согласно закону классической электродинамики ускоренное движение электронов требует расхода
- 13. Нильс Бор, 1913 г. Постулаты Бора: 1) электрон в атоме может вращаться вокруг ядра только по
- 14. Недостатки теории Н. Бора: 1) не пригодна для объяснения строения сложных атомов начиная с гелия; 2)
- 15. Луи де Бройль, 1924 (гипотеза): любая движущаяся частица или предмет обладает волновыми свойствами с частотой связанной
- 18. 2.5 Состав атомных ядер и атомов Д.Д. Иваненко и Е.Н. Гапон (1932) - протонно-нейтронная теория строения
- 19. Понятия и термины: Энергия, выделяющаяся при образовании ядра из протонов и нейтронов, называется энергией связи. Энергия,
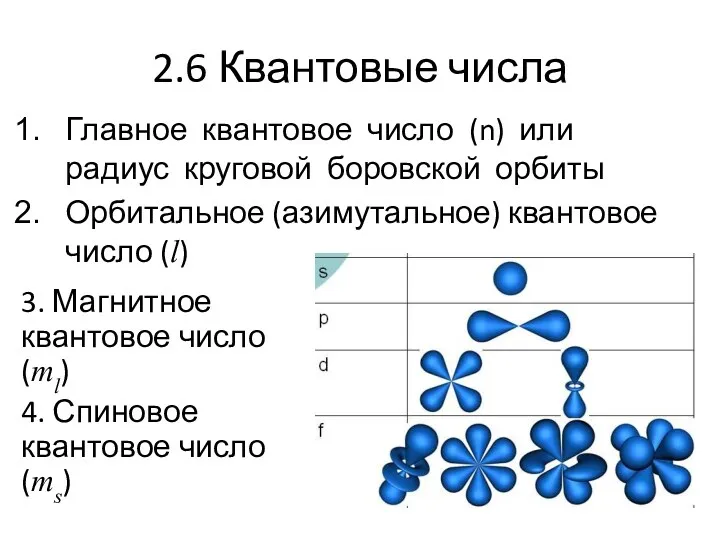
- 20. 2.6 Квантовые числа Главное квантовое число (n) или радиус круговой боровской орбиты Орбитальное (азимутальное) квантовое число
- 21. 2.7 Размещение электрона в атоме Принцип Паули: в атоме не может быть двух электронов, характеризующихся одинаковым
- 22. Правило Клечковского: заполнение электронных подуровней с увеличением порядкового номера атома элемента происходит от меньшего значения (n
- 23. 2.8 Периодический закон в свете теории строения атома Свойства химических элементов, а также формы и свойства
- 24. полудлинная, 18-клеточная
- 25. длинная, 32-клеточная
- 29. Период Совокупность элементов, первые представители которого имеют строение наружного слоя ns1, последнего ns2np6, называется периодом. Совокупность
- 30. Группа Элементы, объединенные сходным электронным строением, называются группой. Номер группы указывает число электронов, которые могут участвовать
- 31. Семейства элементов s-элементы p-элементы d-элементы f-элементы
- 32. 2.9 Свойства нейтральных атомов и их изменение по периодам и группам Металлические и неметаллические свойства Радиус
- 35. Скачать презентацию


























 Химическая технология. Введение
Химическая технология. Введение Щелочные металлы. Периодическая система химических элементов Д.И. Менделеева
Щелочные металлы. Периодическая система химических элементов Д.И. Менделеева Определение качественного состава минеральных вод
Определение качественного состава минеральных вод Хром и его соединения
Хром и его соединения Биоорганическая химия
Биоорганическая химия Растворы. Общие свойства растворов
Растворы. Общие свойства растворов Активные формы кислорода. Антиоксиданты их физиологическая роль
Активные формы кислорода. Антиоксиданты их физиологическая роль Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Фенолы+
Фенолы+ Природні гази
Природні гази Вирощування кристалів в додомашніх умовах
Вирощування кристалів в додомашніх умовах Неомыляемые липиды. Изопреноиды
Неомыляемые липиды. Изопреноиды Химическая очистка сточных вод. Окисление и восстановление
Химическая очистка сточных вод. Окисление и восстановление Железо и его соединения
Железо и его соединения Химический состав клетки. Неорганические вещества
Химический состав клетки. Неорганические вещества М.В.Ломоносов о пользе стекла
М.В.Ломоносов о пользе стекла Хімічні властивості алкенів
Хімічні властивості алкенів Закономірності протікання хімічних реакцій
Закономірності протікання хімічних реакцій Фосфонсірке қышқылының антипирендік қасиеттерін зерттеу
Фосфонсірке қышқылының антипирендік қасиеттерін зерттеу Термический анализ. Прибор синхронного термического анализа
Термический анализ. Прибор синхронного термического анализа Месторождения турмалина
Месторождения турмалина Уравнения химических реакций
Уравнения химических реакций Кальцій
Кальцій Соединения азота. Оксиды азота
Соединения азота. Оксиды азота Электролитическая диссоциация. 9 класс
Электролитическая диссоциация. 9 класс Химические методы синтеза наночастиц
Химические методы синтеза наночастиц Супрамолекулярные системы – мост между неживой и живой материей
Супрамолекулярные системы – мост между неживой и живой материей Анализ качества лекарственных средств органической природы из группы галогенпроизводных углеводородов жирного ряда
Анализ качества лекарственных средств органической природы из группы галогенпроизводных углеводородов жирного ряда