Содержание
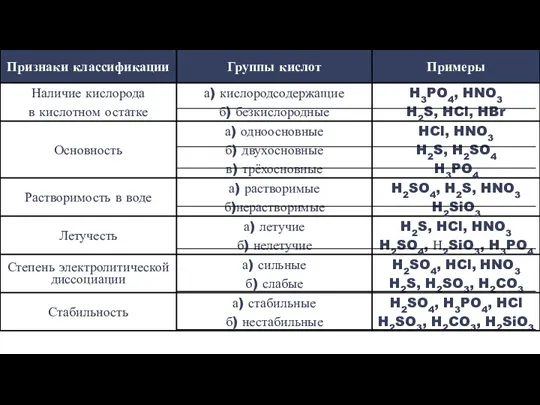
- 3. Кислоты – это электролиты, при диссоциации которых в водных растворах в качестве катионов образуются ионы водорода
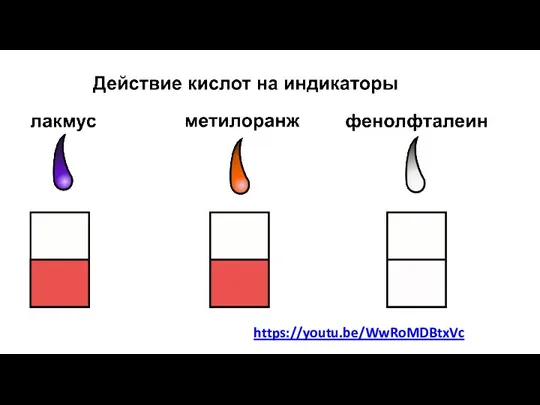
- 4. https://youtu.be/WwRoMDBtxVc
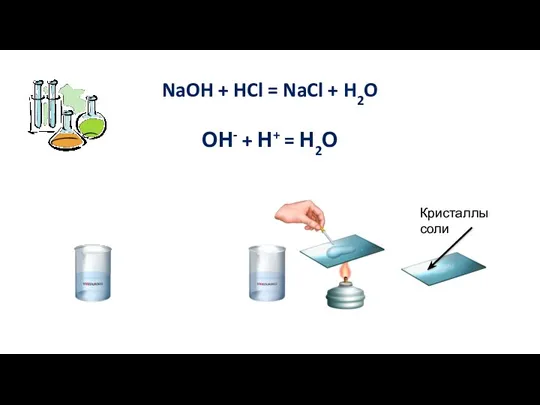
- 5. 2. Реакция с основаниями Кислота + основание = соль + вода Реакция обмена
- 6. NaOH + HCl = NaCl + H2O ОН- + Н+ = Н2О Кристаллы соли
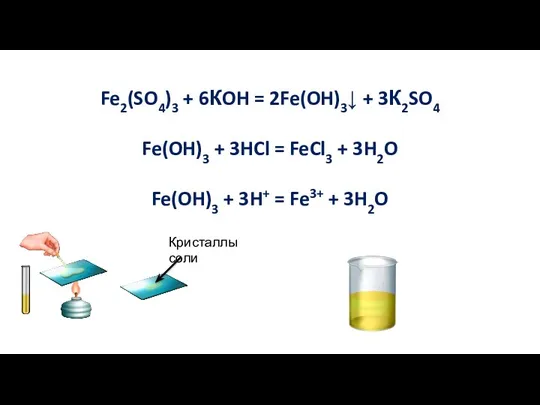
- 7. Fe2(SO4)3 + 6КOH = 2Fe(OH)3↓ + 3К2SO4 Fe(OH)3 + 3HCl = FeCl3 + 3H2O Fe(OH)3 +
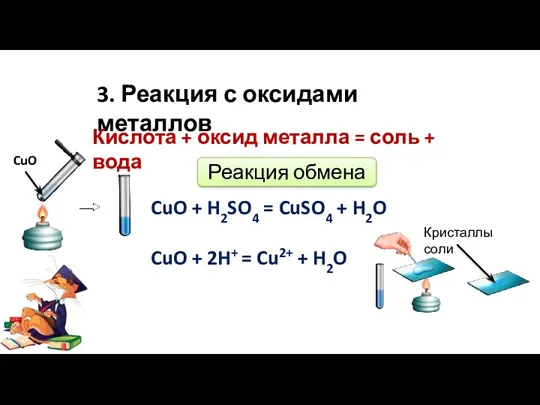
- 8. 3. Реакция с оксидами металлов CuO + H2SO4 = CuSO4 + H2O CuO + 2H+ =
- 9. 4. Реакции с металлами Кислота + металл = соль + водород Реакции замещения
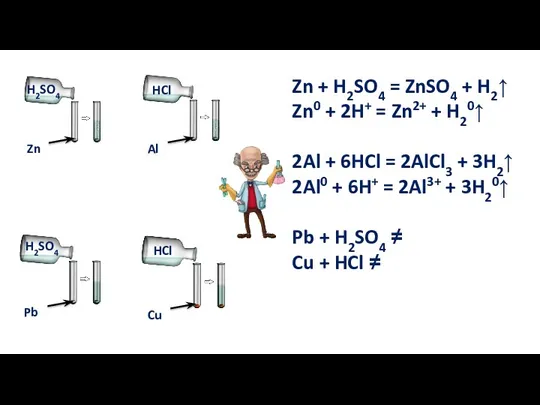
- 10. Для этих реакций необходимы условия: Металл должен находиться в ряду напряжений до водорода; Должна получиться растворимая
- 11. Zn + H2SO4 = ZnSO4 + H2↑ Zn0 + 2H+ = Zn2+ + H20↑ 2Al +
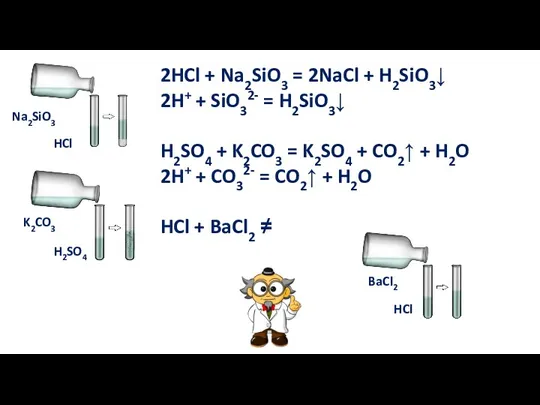
- 12. 5. Реакция с солями Кислота + соль = новая кислота + новая соль Реакция обмена
- 13. 2HCl + Na2SiO3 = 2NaCl + H2SiO3↓ 2H+ + SiO32- = H2SiO3↓ H2SO4 + K2CO3 =
- 14. СВОЙСТВА ОСНОВАНИЙ В СВЕТЕ ТЕОРИИ ЭЛЕКТРОЛИТИЧЕСКОЙ ДИССОЦИАЦИИ
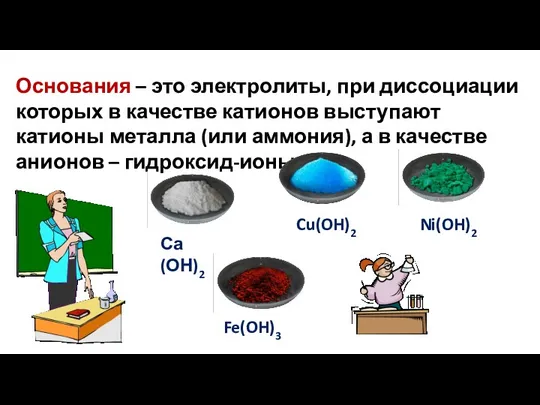
- 15. Основания – это электролиты, при диссоциации которых в качестве катионов выступают катионы металла (или аммония), а
- 16. 1. Диссоциация оснований NaOH = Na+ + OH- https://youtu.be/WwRoMDBtxVc
- 17. 2. Реакции оснований с кислотами (реакции обмена) Основание + кислота = соль + вода NaOH +
- 18. 3. Реакции оснований с оксидами неметаллов (реакции обмена) Основание + оксид неметалла = соль + вода
- 19. 4. Реакции оснований с солями (реакции обмена) Основание + соль = новая соль + новое основание
- 20. NaOH + NH4Cl = NaCl + NH3↑ + H2O OH- + NH4+ = NH3↑ + H2O
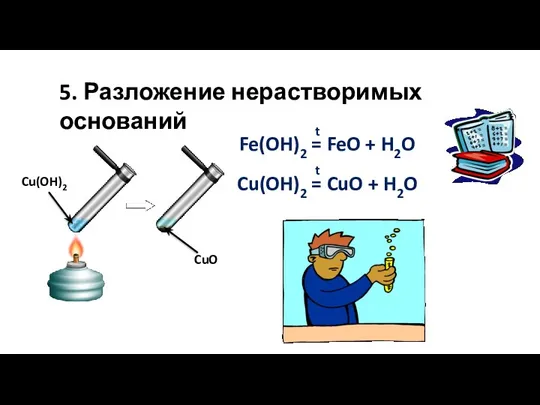
- 21. 5. Разложение нерастворимых оснований Fe(OH)2 = FeO + H2O t Cu(OH)2 = CuO + H2O t
- 23. Амфотерность — это способность некоторых соединений проявлять как кислотные, так и основные свойства в зависимости от
- 24. Взаимодействие амфотерных оксидов со щелочами Al2О3 + 2NaOH = 2NaAlO2 + H2O В реакции между оксидом
- 26. Скачать презентацию










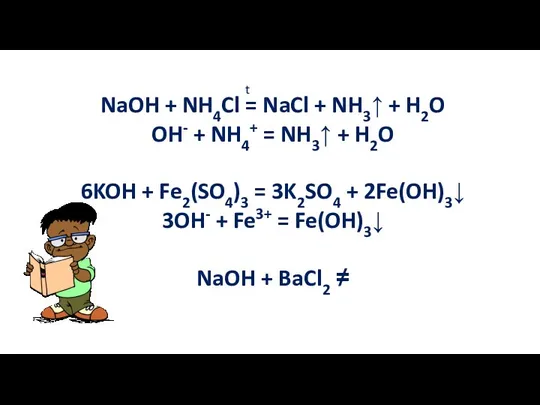



 Оксиди нітрогену
Оксиди нітрогену Биологически важные реакции карбонильных соединений. Масс-спектрометрия
Биологически важные реакции карбонильных соединений. Масс-спектрометрия Phosphorus
Phosphorus большая стирка
большая стирка Хроматография әдісінің негізі
Хроматография әдісінің негізі Классификация химических реакций в неорганической химии
Классификация химических реакций в неорганической химии Спирты. Классификация
Спирты. Классификация Галогены
Галогены Коллоидные ПАВ. Мицеллообрaзование в растворах коллоидных ПАВ. Солюбилизация
Коллоидные ПАВ. Мицеллообрaзование в растворах коллоидных ПАВ. Солюбилизация Причина отказа повреждений технологического оборудования и принятия мер по их устранению установки производства газовой серы
Причина отказа повреждений технологического оборудования и принятия мер по их устранению установки производства газовой серы Ациклические углеводороды
Ациклические углеводороды Химическая кинетика
Химическая кинетика Физические и химические свойства алкенов
Физические и химические свойства алкенов Реакции нейтрализации
Реакции нейтрализации Урок химии по теме Бериллий, магний и щелочноземельные металлы,9 класс
Урок химии по теме Бериллий, магний и щелочноземельные металлы,9 класс Горение жидкого топлива
Горение жидкого топлива Вода: фізичні та хімічні властивості. Поширеність в природі
Вода: фізичні та хімічні властивості. Поширеність в природі Redox Reactions
Redox Reactions Топлива и их свойства. Топлива автомобилей
Топлива и их свойства. Топлива автомобилей Периодический закон и периодическая система химических элементов Д.И. Менделеева
Периодический закон и периодическая система химических элементов Д.И. Менделеева Органическая химия. Пособие
Органическая химия. Пособие Кислотно-основные свойства органических соединений
Кислотно-основные свойства органических соединений Элементтер-органогендер. өмір металдары. Көміртек – органикалық қосылыстардың негізін құраушы
Элементтер-органогендер. өмір металдары. Көміртек – органикалық қосылыстардың негізін құраушы Коррозия металлов
Коррозия металлов Штучні та природні речовини
Штучні та природні речовини Технология производства аминоальдегидных смол
Технология производства аминоальдегидных смол Инертные газы
Инертные газы Химические свойства кислот
Химические свойства кислот