Слайд 2
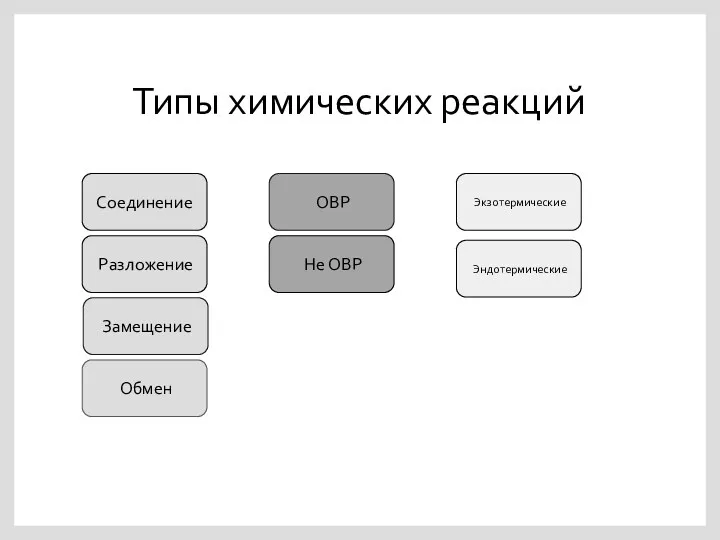
Типы химических реакций
Соединение
Разложение
Замещение
Обмен
ОВР
Не ОВР
Экзотермические
Эндотермические
Слайд 3

Слайд 4

ОПЫТ. РАЗЛОЖЕНИЕ КАРБОНАТА КАЛЬЦИЯ
Слайд 5

Слайд 6

Экзотермическими реакциями являются реакции окисления, горения, соединения металлов с другими элементами
и т. д.
К Эндотермическим реакциям относятся реакции разложения.
Слайд 7

Тепловой эффект реакции
Тепловой эффект реакции - количество выделенной (или поглощённой) в
ходе реакции теплоты
Q, кДж
В экзотермической реакции +Q
В эндотермической -Q
Слайд 8
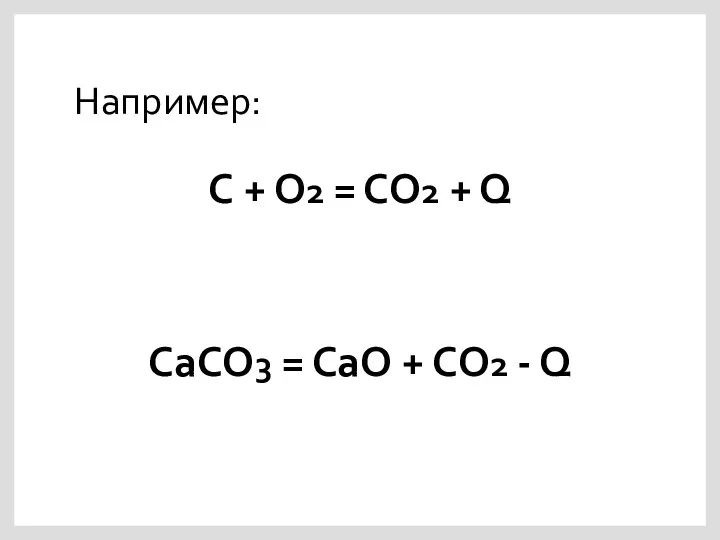
Например:
C + O2 = CO2 + Q
CaCO3 = CaO + CO2
- Q
Слайд 9

Термохимические уравнения
C + O2 = CO2 + 394 кДж
в экзотермической реакции
образования 1 моль углекислого газа из простых веществ выделяется 394 кДж теплоты
CaCO3 = CaO + CO2 – 1200 кДж
в эндотермической реакции разложения 1 моль карбоната кальция поглощается 1200 кДж теплоты
В термохимических уравнениях также указываются агрегатные состояния веществ:
(г) — газ;
(ж) — жидкость;
(т) или (к) — твёрдое (кристаллическое) вещество
H2(г) + Cl2(г) = 2HCl(г) + 184,6 кДж
Слайд 10

Слайд 11
![Некоторые формулы для решения задач Количество вещества [моль] ν =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/604405/slide-10.jpg)
Некоторые формулы для решения задач
Количество вещества [моль]
ν = m/M = V/VM
Масса
[г]
m = ν×M
М – молярная масса, [г/моль]
VM – молярный объем, равный 22,4 л/моль
Слайд 12

Задача №1
Определите, сколько теплоты выделяется при сгорании
15 моль углерода, если термохимическое уравнение имеет вид:
C(тв)
+ O2 (г) = CO2 (г) + 394 кДж
Слайд 13

Задача №2
Найдите, какой объём (л) метана (н. у.) сгорел в кислороде, если при
этом выделилось 80,4 кДж теплоты.
Термохимическое уравнение имеет вид:
CH4 (г) + 2O2(г) = CO2(г) + 2H2O(г) + 804 кДж
Слайд 14

Задача №3
Рассчитайте, сколько метана (г) сгорело в кислороде, если известно, что при этом выделилось
кДж теплоты.
Термохимическое уравнение имеет вид:
CH4 (г) + 2O2(г) = CO2(г) + 2H2O(г) + 804 кДж






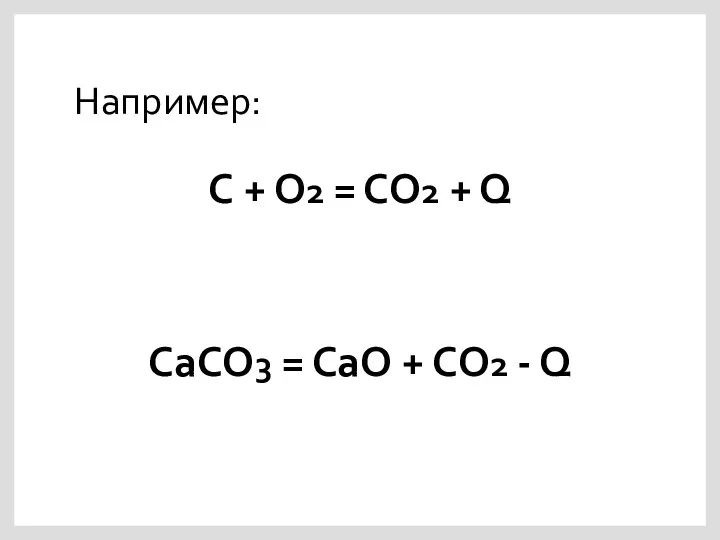


![Некоторые формулы для решения задач Количество вещества [моль] ν =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/604405/slide-10.jpg)



 Основы химической термодинамики. Термохимические расчеты
Основы химической термодинамики. Термохимические расчеты Органикалық қосылыстар. Көмірсутектерден жасалған
Органикалық қосылыстар. Көмірсутектерден жасалған Теория строения органических соединений А.М. Бутлерова
Теория строения органических соединений А.М. Бутлерова Подгруппа углерода
Подгруппа углерода Основания. 8 класс
Основания. 8 класс Аурум
Аурум Химическая кинетика
Химическая кинетика Дисперсные системы: получение и свойства
Дисперсные системы: получение и свойства Обмоточные провода
Обмоточные провода Химия. 6я группа элементов. 9 класс
Химия. 6я группа элементов. 9 класс Органическая химия. Лекция - Гидроксикислоты
Органическая химия. Лекция - Гидроксикислоты Амин қышқылдар
Амин қышқылдар Минералогия литофильных редких элементов. Бериллий
Минералогия литофильных редких элементов. Бериллий Вклад М.В. Ломоносова в развитие науки химия
Вклад М.В. Ломоносова в развитие науки химия Азотная кислота и ее свойства
Азотная кислота и ее свойства Липолиз. Обмен кетоновых тел
Липолиз. Обмен кетоновых тел Материаловедение. Физические и химические структуры материалов
Материаловедение. Физические и химические структуры материалов Химическая промышленность
Химическая промышленность Химические формулы. 8 класс
Химические формулы. 8 класс Хімічний зв’язок. Ковалентний, йонний, металічний, водневий зв’язки, механізми їх утворення
Хімічний зв’язок. Ковалентний, йонний, металічний, водневий зв’язки, механізми їх утворення Натрий алкилсульфонаттарын алу. №4 лекция
Натрий алкилсульфонаттарын алу. №4 лекция Серебро. Нахождение в природе
Серебро. Нахождение в природе Уран – периодты жүйедегі атомдық номері 92 болатын химиялық элемент
Уран – периодты жүйедегі атомдық номері 92 болатын химиялық элемент Активационный анализ
Активационный анализ Свойства воды
Свойства воды Законы химической термодинамики. Часть 1. Физическая и коллоидная химия
Законы химической термодинамики. Часть 1. Физическая и коллоидная химия Классификация полимеров
Классификация полимеров Кислоты. Определение и классификация
Кислоты. Определение и классификация