Содержание
- 2. Железо. Общая информация. Положение в Периодической системе: VIIIB группа, 4-й период Электронная конфигурация: [Ar]4s23d6 Основные степени
- 3. Железо. Применение Конструкционные материалы (сталь, чугун и другие сплавы; железобетон). >90% от всей выплавки металлов в
- 4. Железо. Получение 4-й по распространенности в земной коре (после O, Si и Al) Основные добывающие страны:
- 5. Хим. свойства Fe0 Левее водорода в ряду напряжений. Похоже по свойствам на Mn. Fe + 2HCl
- 6. http://chemnet.ru/rus/teaching/zagorskii2/lesson0/v011.html http://files.school-collection.edu.ru/dlrstore/deb6e939-f8c8-fea7-fe24-7b2c80013fd7/index.htm
- 7. Хим. свойства Fe+2 Fe(OH)2 – основный гидроксид, в воде нерастворим С растворами кислот реагирует, с р-рами
- 8. Хим. свойства Fe+2 Осадки с катионом Fe2+: 1. FeSO4 + (NH4)2S → FeS↓ (черный) + (NH4)2SO4
- 9. Хим. свойства Fe+3 Fe2O3 и Fe(OH)3 – считаются амфотерными, но на деле ни оксид, ни гидроксид
- 10. Хим. свойства Fe+3 Железо(+3) может быть окислителем: 2FeCl3 + 2NaI → 2FeCl2 + I2↓ + 2NaCl
- 11. Хим. свойства Fe+6 H2FeO4 ("железная кислота") и оксид FeO3 не существуют. Соли FeO42- (ферраты) устойчивы в
- 12. Качественные реакции на Fe3+: Самая неспецифичная: Fe3+ (желтый р-р) + 3OH- → Fe(OH)3↓ (бурый осадок) С
- 13. Качественная реакция на Fe2+: С красной кровяной солью: FeSO4 + K3[Fe(CN)6] → K[FeFe(CN)6]↓ (синий осадок) +
- 14. Железо. Необычные реакции 2FeCl3(тв., безв.) →(300°C, вакуум) Fe2Cl6↑ Имеет молекулярное строение Fe3+ находится в тетраэдрическом окружении
- 15. Железо. Необычные реакции FeCl2 + 2C5H5Na → [Fe(C5H5)2] + 2NaCl Ферроцен Комплекс вида «сэндвич» Устойчив на
- 16. Медь. Общая информация. Положение в Периодической системе: IB группа, 4-й период Электронная конфигурация: [Ar]4s13d10 ("проскок" электрона!)
- 17. Медь. Применение Электропровода и электротехника; припои (латунь - сплав меди с цинком) Конструкционные материалы - водопроводные
- 18. Медь. Получение 25-я по распространенности в земной коре Основные добывающие страны: Чили, Китай, Перу, США. Добывают
- 19. Хим. свойства Cu0 Медь находится правее водорода в ряду напряжений металлов. Не растворяется в щелочах и
- 20. Хим. свойства Cu+1 Аквакомплекс Cu+ в водном растворе неустойчив, диспропорционирует: Cu2O(тв.) + H2SO4(разб.) → Cu↓ +
- 21. Хим. свойства Cu+2 Cu(OH)2 - голубой "объемный" осадок, растворяется в кислотах, не растворяется в щелочах: Cu(OH)2
- 22. Хим. свойства Cu+2 Осадки с катионом Cu2+: 1. CuSO4 + H2S → CuS↓ (черный) + H2SO4
- 23. Медь. Необычные реакции Голубой осадок → синий раствор →(t°C) красный осадок Идёт через стадию образования хелатного
- 24. Медь. Необычные реакции 3CuCl2 + 5Na2SO3 + 3H2O → Cu2SO3*CuSO3*2H2O↓ (темно-красный) + Na2SO4 + 6NaCl +
- 26. Скачать презентацию













![Железо. Необычные реакции FeCl2 + 2C5H5Na → [Fe(C5H5)2] + 2NaCl](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/158768/slide-14.jpg)









 Непредельные углеводороды: алкены, олефины
Непредельные углеводороды: алкены, олефины Основы коррозии и защиты металлов. Виды коррозии металлов
Основы коррозии и защиты металлов. Виды коррозии металлов Реакционная способность твердых тел и способы ее регулирования
Реакционная способность твердых тел и способы ее регулирования Азотистые гетероциклические соединения
Азотистые гетероциклические соединения Водород
Водород Химические профессии на стройках Олимпиады
Химические профессии на стройках Олимпиады Основные классы неорганических веществ
Основные классы неорганических веществ Химическое равновесие. Азот (продолжение). 9 класс
Химическое равновесие. Азот (продолжение). 9 класс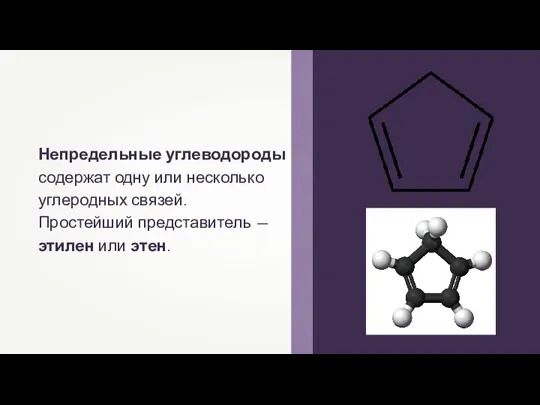 Физические и химические свойства алкенов
Физические и химические свойства алкенов Распространение водорода в природе. Получение в лаболатории
Распространение водорода в природе. Получение в лаболатории Природные источники углеводородов
Природные источники углеводородов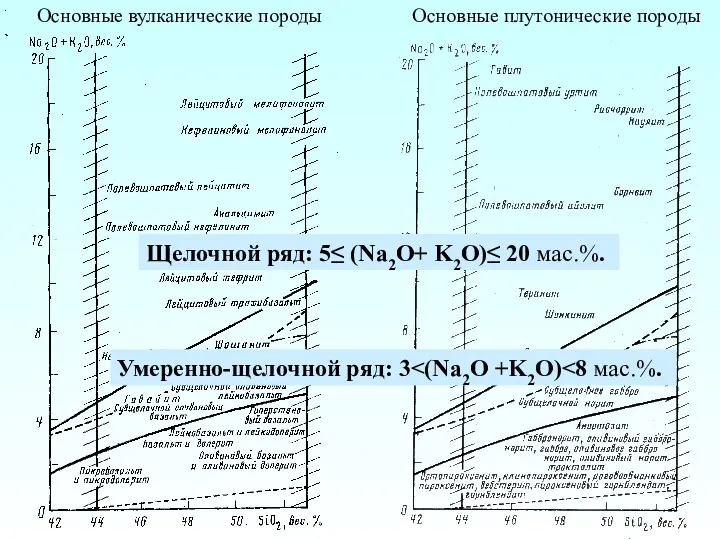 Основные вулканические породы. Основные плутонические породы
Основные вулканические породы. Основные плутонические породы Стронций
Стронций Пластмасса, пластикалық материалдар
Пластмасса, пластикалық материалдар Генетическая связь органических и неорганических соединений
Генетическая связь органических и неорганических соединений Строение атома. Химия. 11 класс
Строение атома. Химия. 11 класс Нефть и ее роль в мировой экономике
Нефть и ее роль в мировой экономике Электролиз: опыты к заданиям ЕГЭ
Электролиз: опыты к заданиям ЕГЭ Тепловой эффект химических реакций
Тепловой эффект химических реакций Алкадиены
Алкадиены Теория электролитической диссоциации
Теория электролитической диссоциации Производные 8-замещенных хинолина
Производные 8-замещенных хинолина Сопряжение электронной плотности, как фактор обеспечения стабильности молекул
Сопряжение электронной плотности, как фактор обеспечения стабильности молекул Реакции ионного обмена
Реакции ионного обмена Технология производства бутилкаучука
Технология производства бутилкаучука Алкины — углеводороды, содержащие тройную связь между атомами углерода
Алкины — углеводороды, содержащие тройную связь между атомами углерода Introduction in bioorganic chemistry. Isomerism and structure of organic compounds
Introduction in bioorganic chemistry. Isomerism and structure of organic compounds Пниктогены - элеметны VA группы
Пниктогены - элеметны VA группы