Слайд 2

Какие углеводороды называются ароматическими?
Ароматические углеводороды (арены) – это углеводороды с
общей формулой СnH2n-6, в молекулах которых имеется хотя бы одно бензольное кольцо.
Слайд 3
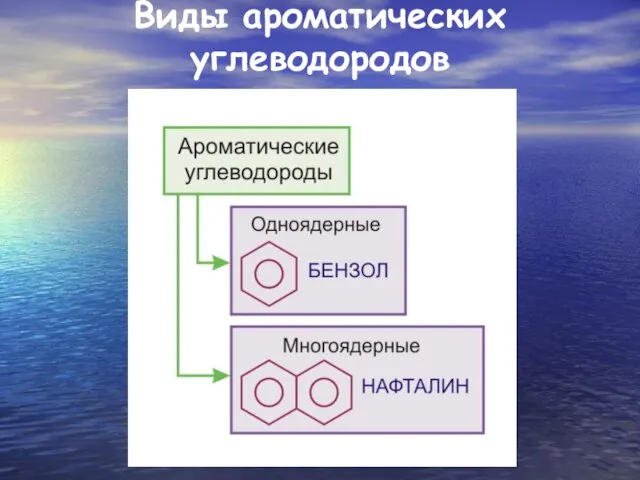
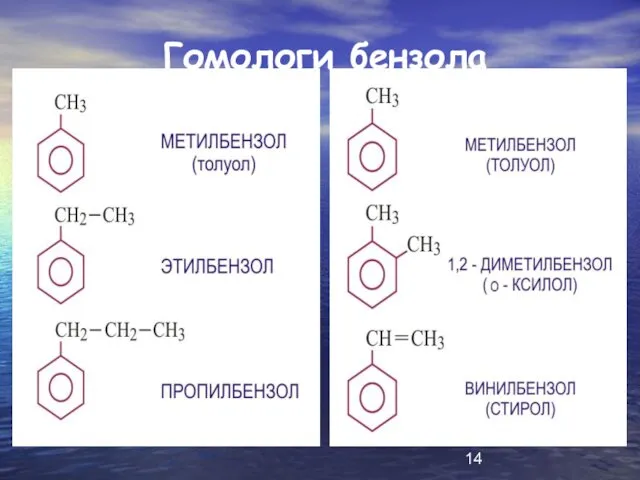
Виды ароматических углеводородов
Слайд 4

Майкл Фарадей
(1791 - 1867)
Английский физик и химик, член Лондонского королевского
общества. Один из основателей количественной электрохимии. В 1823 г. впервые получил жидкие хлор, сероводород, оксид углерода(IV), аммиак, оксид азота(IV). В 1825 г. открыл бензол, изучил его физические и некоторые химические свойства. Положил начало исследованиям каучука. В 1833 - 1836 гг. установил количественные законы электролиза.
Слайд 5

Фридрих Август Кекуле
1829 - 1896
Немецкий химик-органик. Предложил структурную формулу молекулы
бензола. С целью проверки гипотезы о равноценности всех шести атомов водорода в молекуле бензола получил его галоген-, нитро-, амино-, и карбоксипроизводные. Открыл перегруппировку диазоамино- в азоаминобензол, синтезировал трифенилметан и антрахинол.
Слайд 6

Строение молекулы бензола
Слайд 7
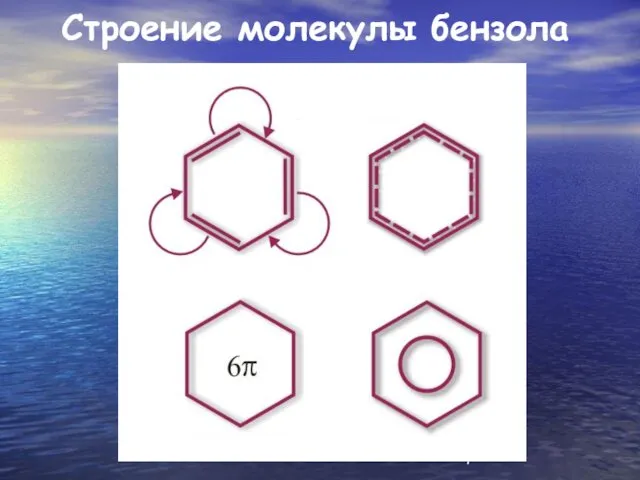
Строение молекулы бензола
Слайд 8

Слайд 9
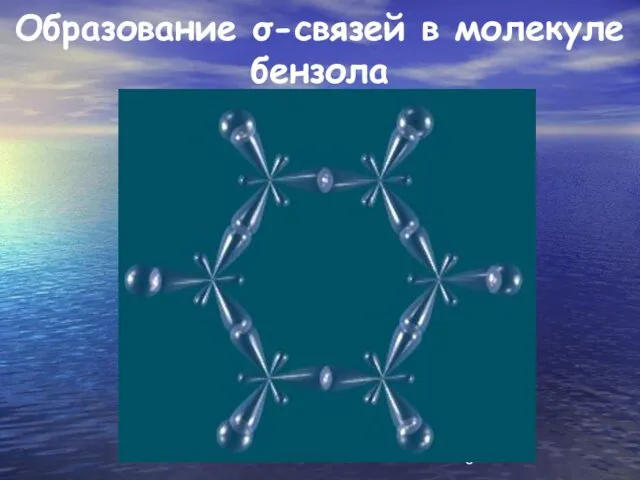
Образование σ-связей в молекуле бензола
Слайд 10
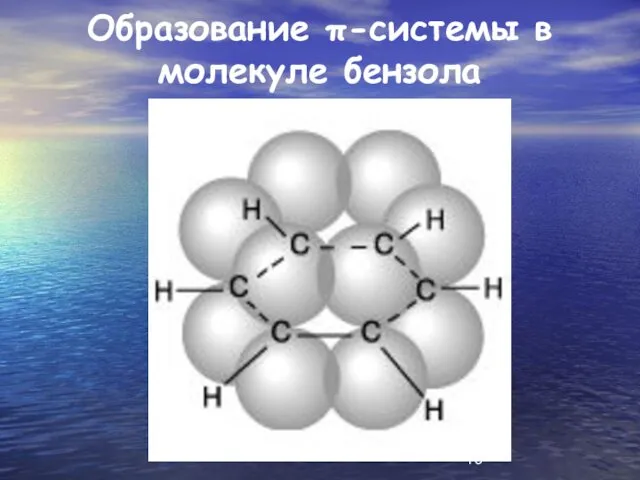
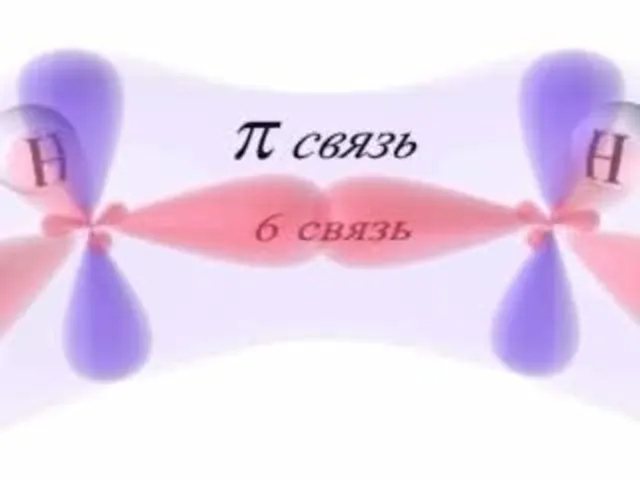
Образование π-системы в молекуле бензола
Слайд 11
Слайд 12

Слайд 13
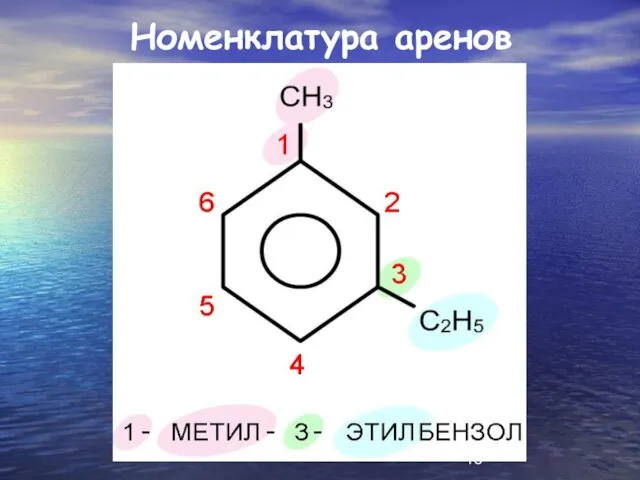
Слайд 14
Слайд 15

Слайд 16

Арены получают главным образом при сухой перегонке каменного угля. При
нагревании каменного угля в ретортах или коксовальных печах без доступа воздуха при 1000 – 1300 0С происходит разложение органических веществ каменного угля с образованием твердых, жидких и газообразных продуктов.
Альтернативным источником получения аренов служит древесина. В самой древесине аренов нет, однако при ее пиролизе они образуются и могут быть выделены.
В странах богатых нефтью арены получают при ее переработке. Нефтяные продукты нагревают при температуре 700 0С, в результате чего из продуктов разложения нефти удается получить 15-18% аренов.
Слайд 17
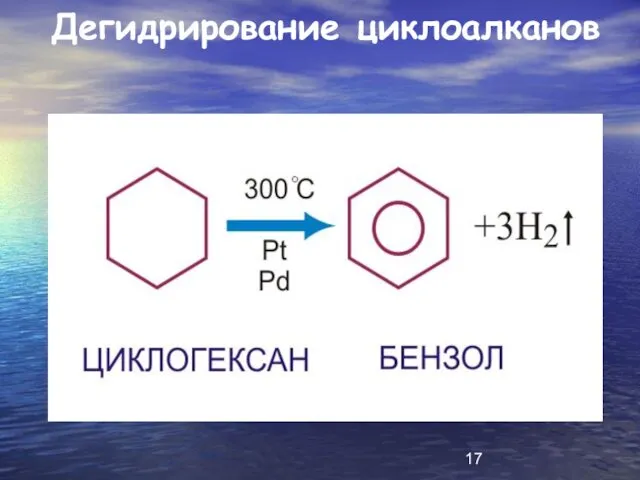
Дегидрирование циклоалканов
Слайд 18
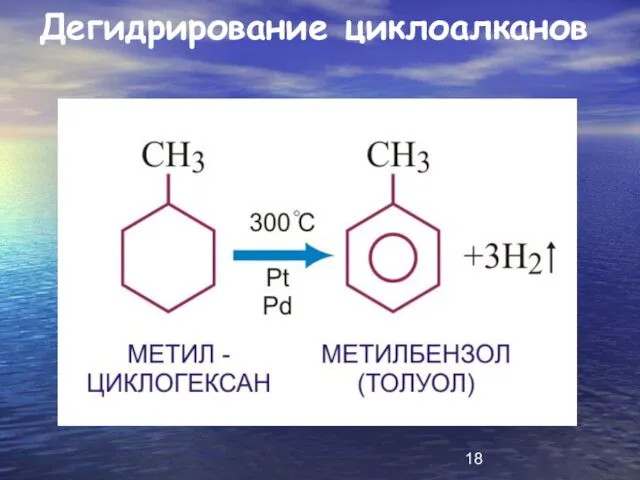
Дегидрирование циклоалканов
Слайд 19
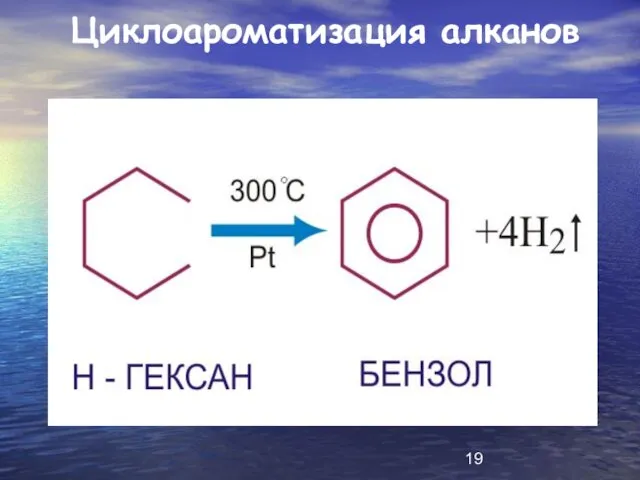
Циклоароматизация алканов
Слайд 20
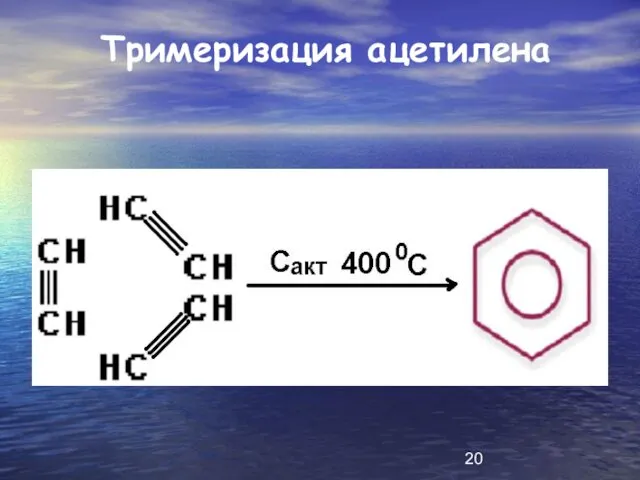
Слайд 21

Николай Дмитриевич Зелинский
1861 – 1953 гг.
Русский химик, академик. Основал большую
школу исследователей в области органического катализа, в которой ему принадлежат классические работы. Важное народнохозяйственное значение имеют исследования Зелинского в области химии нефти. Он разработал методы получения из нефти ценных углеводородов, служащих исходными материалами для синтеза красителей, искусственного каучука, пластмасс, медикаментов и т. д. Провел исследования по химии белка, которые значительно расширили знания о строении белковых тел.
Слайд 22
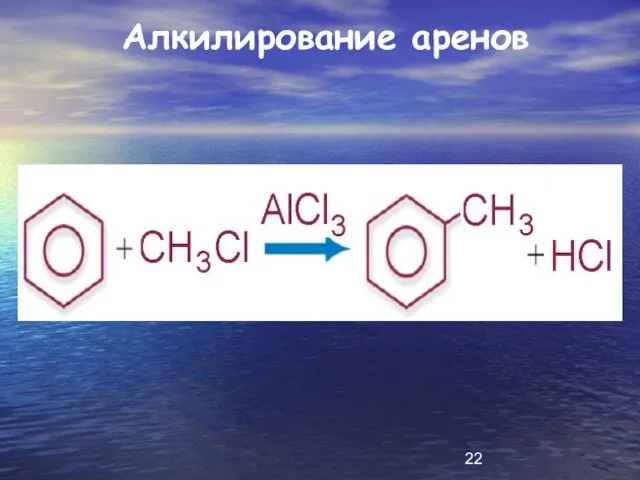
Слайд 23
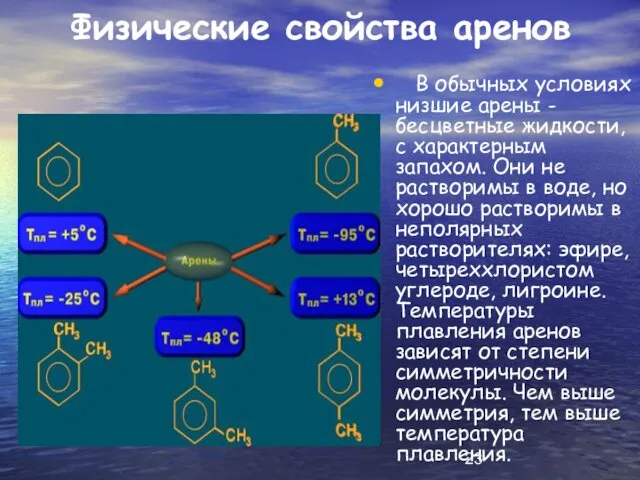
Физические свойства аренов
В обычных условиях низшие арены - бесцветные жидкости,
с характерным запахом. Они не растворимы в воде, но хорошо растворимы в неполярных растворителях: эфире, четыреххлористом углероде, лигроине. Температуры плавления аренов зависят от степени симметричности молекулы. Чем выше симметрия, тем выше температура плавления.
Слайд 24

Слайд 25

Слайд 26

Слайд 27

Слайд 28

Слайд 29

Химические свойства аренов
Слайд 30
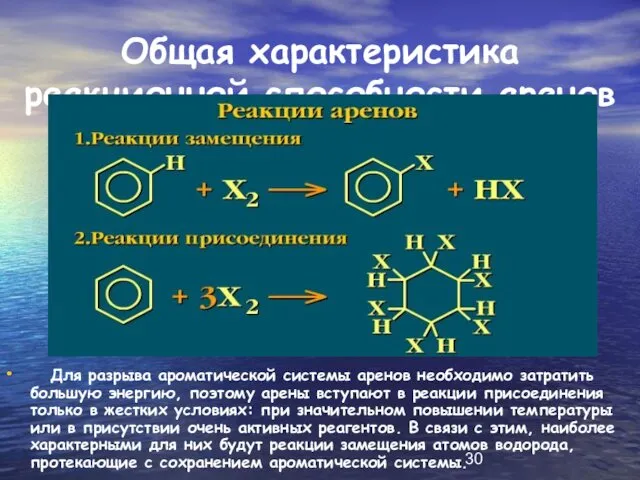
Общая характеристика реакционной способности аренов
Для разрыва ароматической системы аренов необходимо
затратить большую энергию, поэтому арены вступают в реакции присоединения только в жестких условиях: при значительном повышении температуры или в присутствии очень активных реагентов. В связи с этим, наиболее характерными для них будут реакции замещения атомов водорода, протекающие с сохранением ароматической системы.
Слайд 31
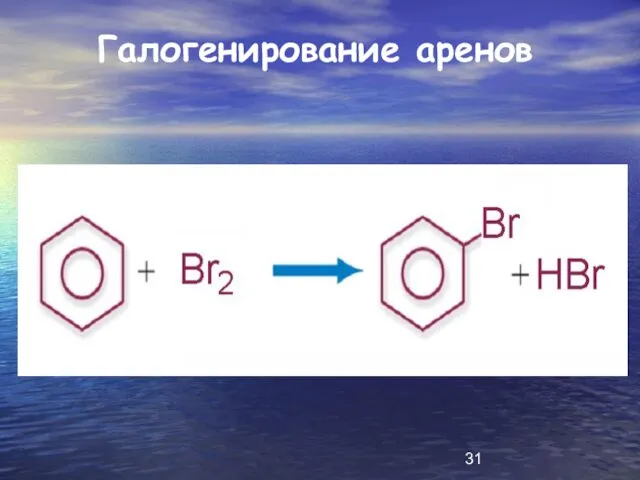
Слайд 32

Слайд 33
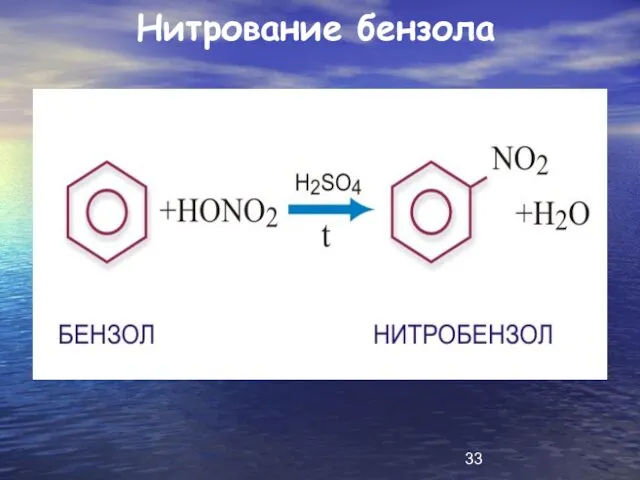
Слайд 34
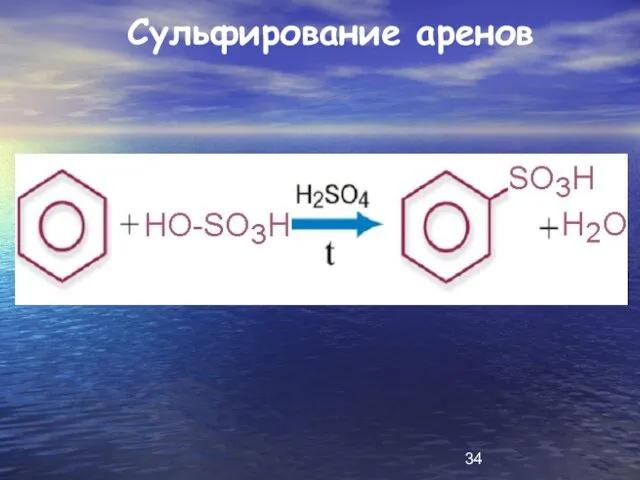
Слайд 35
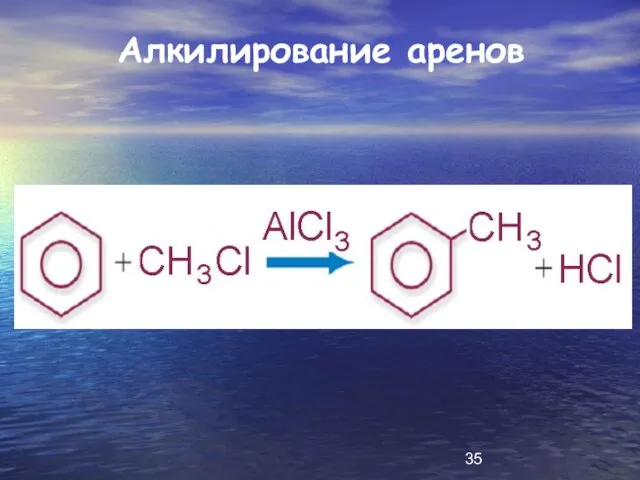
Слайд 36
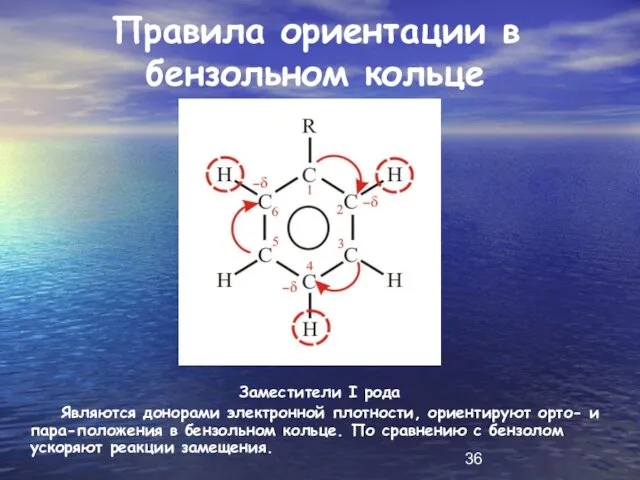
Правила ориентации в бензольном кольце
Заместители I рода
Являются донорами электронной плотности,
ориентируют орто- и пара-положения в бензольном кольце. По сравнению с бензолом ускоряют реакции замещения.
Слайд 37

Правила ориентации в бензольном кольце
Заместители II рода
Являются акцепторами электронной плотности,
ориентируют мета-положение в бензольном кольце. По сравнению с бензолом замедляют реакции замещения.
Слайд 38
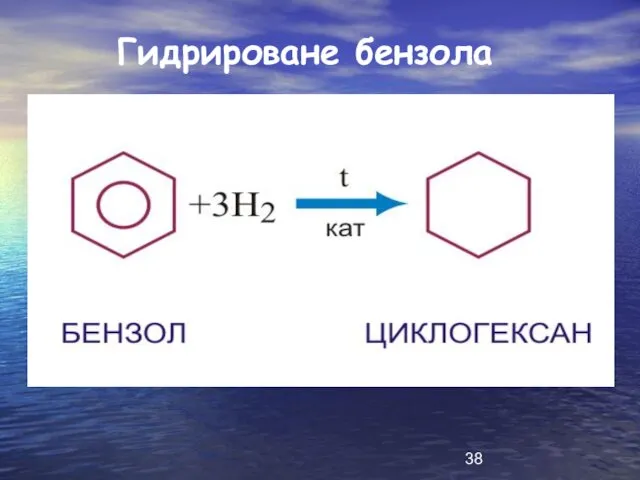
Слайд 39
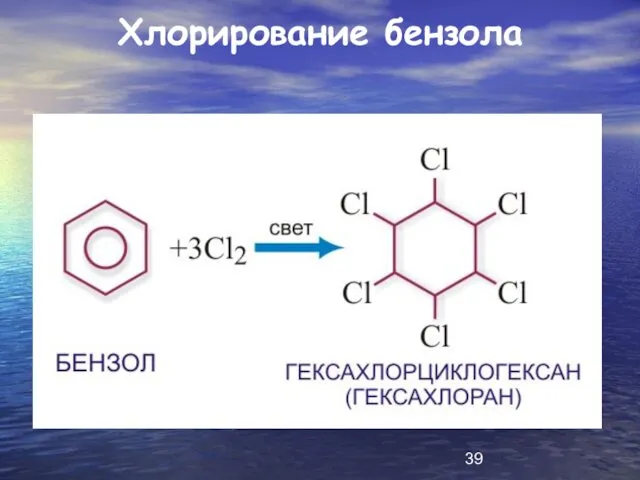
Слайд 40

Слайд 41

Слайд 42
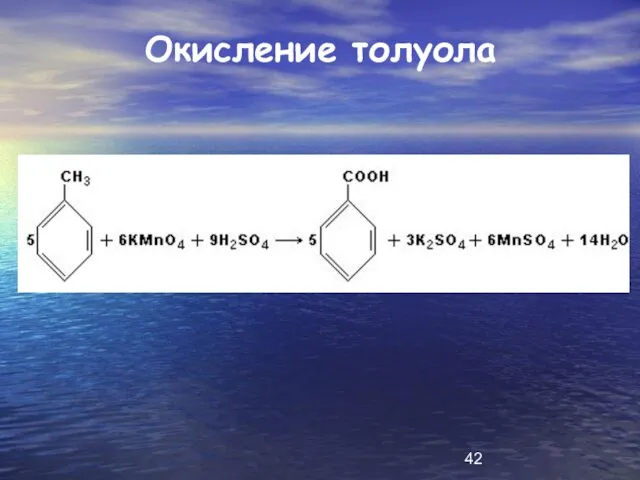
Слайд 43

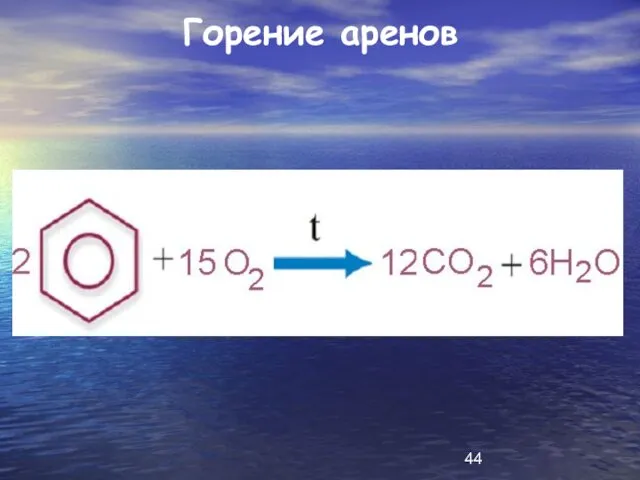
Слайд 44











































 Поверхностные явления. Типы поверхностных явлений
Поверхностные явления. Типы поверхностных явлений Графит
Графит Серная кислота и её свойства
Серная кислота и её свойства Оксиды, их классификация и свойства
Оксиды, их классификация и свойства Алкадиены. Строение алкадиенов
Алкадиены. Строение алкадиенов Курс биохимии. Биохимия крови
Курс биохимии. Биохимия крови Действующие вещества. Лексикон
Действующие вещества. Лексикон Классификация минералов в соответствии с систематикой, утвержденной IMA
Классификация минералов в соответствии с систематикой, утвержденной IMA Алкены. Непредельные углеводороды
Алкены. Непредельные углеводороды Кислород. Промышленный способ (перегонка жидкого воздуха)
Кислород. Промышленный способ (перегонка жидкого воздуха) Атомовиты. Анатомо-физиологические свойства
Атомовиты. Анатомо-физиологические свойства Д.И. Менделеев Мощь и сила науки во множестве фактов, цель – в обобщении этого множества
Д.И. Менделеев Мощь и сила науки во множестве фактов, цель – в обобщении этого множества Гидроочистка нефти и газа
Гидроочистка нефти и газа Поверхностные явления
Поверхностные явления Скорость химических реакций. Химическое равновесие
Скорость химических реакций. Химическое равновесие Центрифугирование в почвоведении
Центрифугирование в почвоведении Классификация химических реакций (11 класс)
Классификация химических реакций (11 класс) Особливості горіння дисперсних систем
Особливості горіння дисперсних систем Первая группа периодической системы Менделеева. Щелочные металлы
Первая группа периодической системы Менделеева. Щелочные металлы Оптические свойства салических породообразующих минералов (лекция 8)
Оптические свойства салических породообразующих минералов (лекция 8) Альдегиды и кетоны
Альдегиды и кетоны Углеводы. Молекулярные формулы
Углеводы. Молекулярные формулы Трансмиссионные масла
Трансмиссионные масла Атомно-молекулярное учение. (Лекция 1)
Атомно-молекулярное учение. (Лекция 1) Закон постоянства состава
Закон постоянства состава Путешествие на остров Соединений химических элементов. Урок-игра
Путешествие на остров Соединений химических элементов. Урок-игра Кобальт. Химический элемент
Кобальт. Химический элемент 20230306_oni_byli_pervymi
20230306_oni_byli_pervymi