Содержание
- 2. Процессы, протекающие на границе электрод-раствор, называются электродными и занимают центральное место во всей электрохимии. В зависимости
- 3. Электродный потенциал возникает в биосистемах, как и в любых системах, имеющих контакт двух фаз. Это относится
- 4. Это электрохимические устройства, разделенные мембраной и чувствительные (селективные) к определенным ионам. В них возникает мембранный потенциал
- 5. 2) Мембранные потенциалы характеризуются не только разностью концентраций электролита по обе стороны мембраны, но и разностью
- 6. 3.1. Двойной электрический слой (ДЭС). Уравнение Нернста Рассмотрим процессы, происходящие при помещении любого металла в раствор
- 7. Рассмотрим границу раздела фаз металлического Zn с раствором ZnSO4 Химические потенциалы ионов цинка в металле оказываются
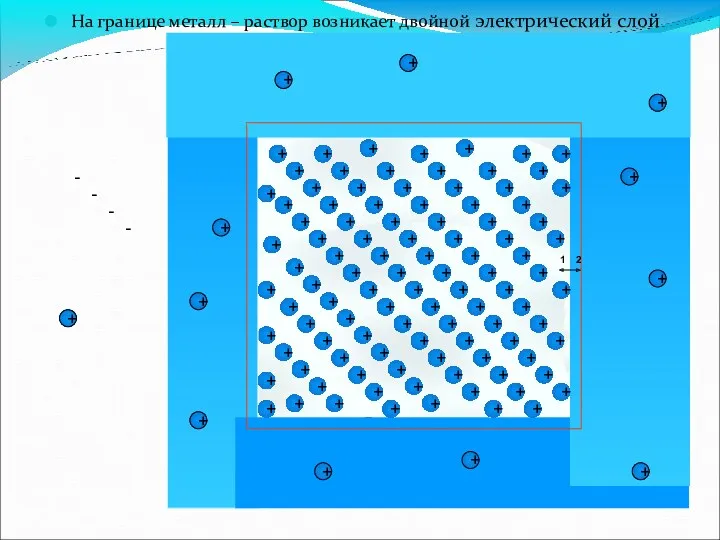
- 8. На границе любых двух фаз самопроизвольно возникает двойной электрический слой и, следовательно, появляется скачок потенциала
- 9. - - - - - - На границе металл – раствор возникает двойной электрический слой +
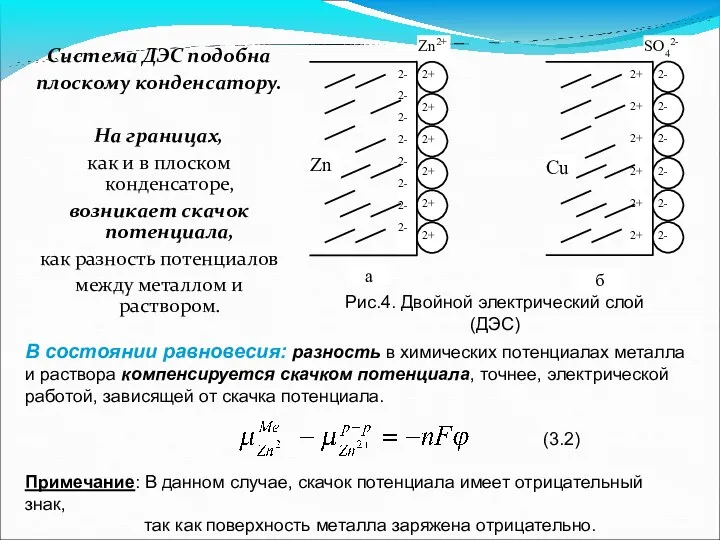
- 10. Система ДЭС подобна плоскому конденсатору. На границах, как и в плоском конденсаторе, возникает скачок потенциала, как
- 11. Уравнение Нернста Выразим из уравнения (3.2) скачок потенциала : выражение является постоянной величиной и обозначается: Тогда
- 12. На границе металлической меди и раствора CuSO4 реализуется другой случай возникновения ДЭС: (3.4) В результате: Ионы
- 13. Строго говоря, равновесие между заряженными частицами в двух фазах должно определяться равенством НЕ химических, а электрохимических
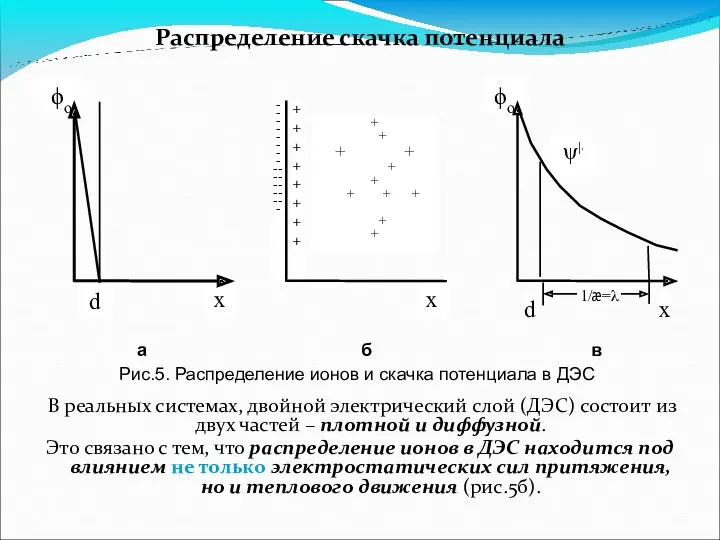
- 14. Распределение скачка потенциала В реальных системах, двойной электрический слой (ДЭС) состоит из двух частей – плотной
- 15. Если считать ДЭС плоским конденсатором, то распределение скачка потенциала, в зависимости от расстояния, является линейным (рис.5а).
- 16. 3.2. Электродвижущая сила (ЭДС) гальванического элемента Основа работы гальванических элементов: Самопроизвольные процессы образования ДЭС Возникновения скачка
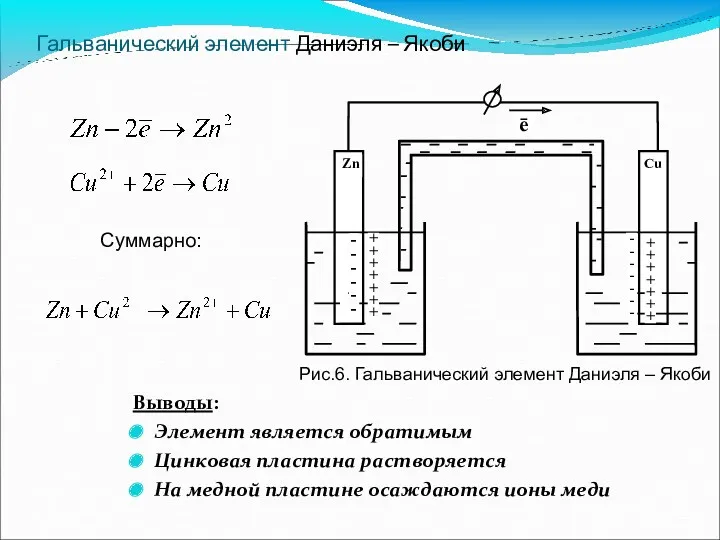
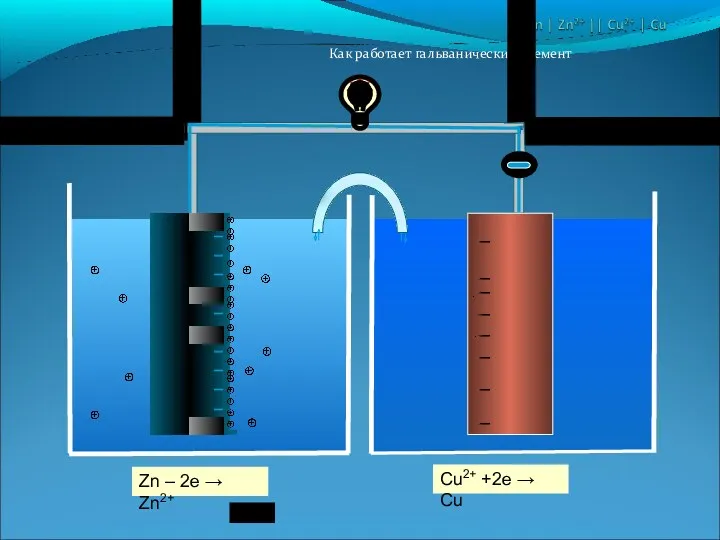
- 17. Гальванический элемент Даниэля – Якоби Выводы: Элемент является обратимым Цинковая пластина растворяется На медной пластине осаждаются
- 18. Как работает гальванический элемент ____________ _ _ _ _ _ _ _ _ Cu2+ +2e →
- 19. Основные элементы электрохимической (гальванической) цепи: металлические электроды (проводники I рода) растворы или расплавы электролитов (проводники II
- 20. Форма записи гальванических цепей Записывают металл отрицательного электрода. Одной вертикальной чертой обозначают границы фаз между металлом
- 21. Электродвижущая сила - основная характеристика элемента. Электродвижущая сила элемента (ЭДС) - это алгебраическая сумма всех скачков
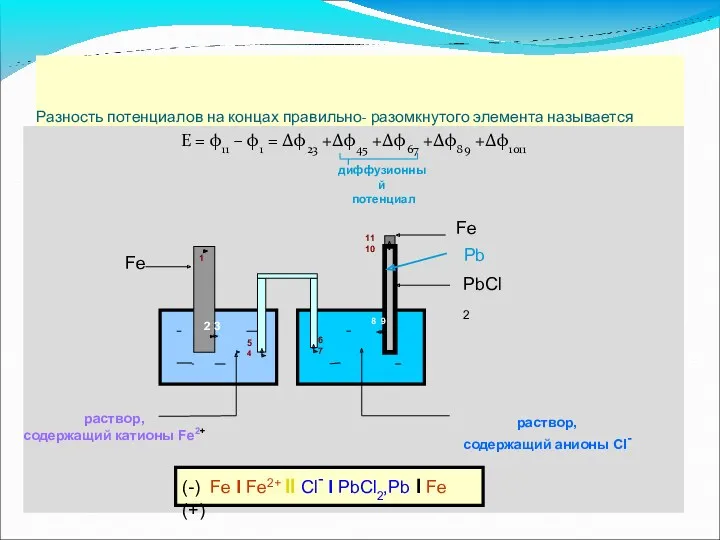
- 22. Разность потенциалов на концах правильно- разомкнутого элемента называется электродвижущей силой этого элемента Е = φ11 –
- 23. + - + - + - + - + - + - Fe раствор FeCl3 Fe3+
- 24. Величину диффузионного потенциала можно снизить заполнением электролитического ключа насыщенным раствором KCl. При этом одна граница раздела
- 25. 3.3. Потенциалы электродов. Система знаков Для практических расчетов достаточно знать НЕ абсолютные величины потенциалов, а лишь
- 26. Химическую реакцию, протекающую в элементе, составленном из измеряемого и водородного электродов, принято записывать так, чтобы: на
- 27. Если реакция в элементе протекает в противоположном направлении, то потенциал электрода – отрицателен. Реакция с участием
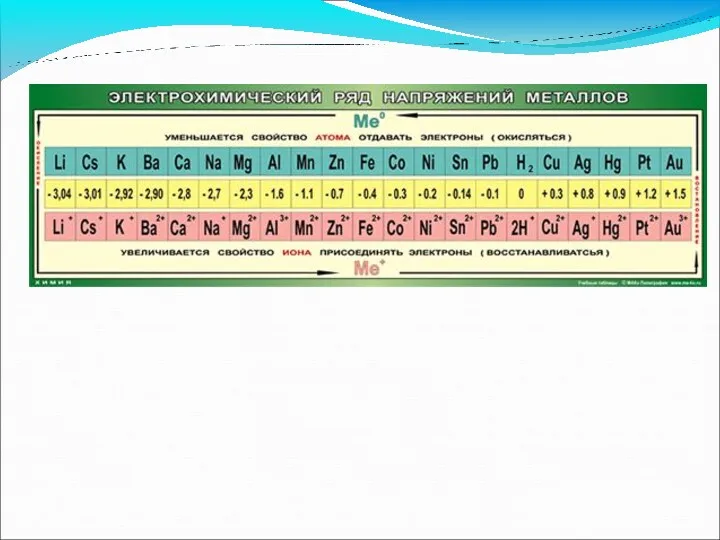
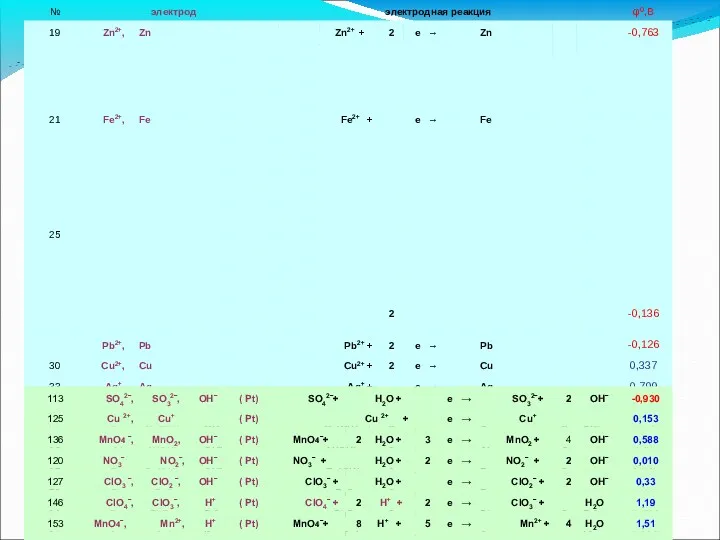
- 28. Ряд напряжений стандартных потенциалов Ряд напряжений – значения стандартных потенциалов, расположенные в порядке их возрастания. Ряд
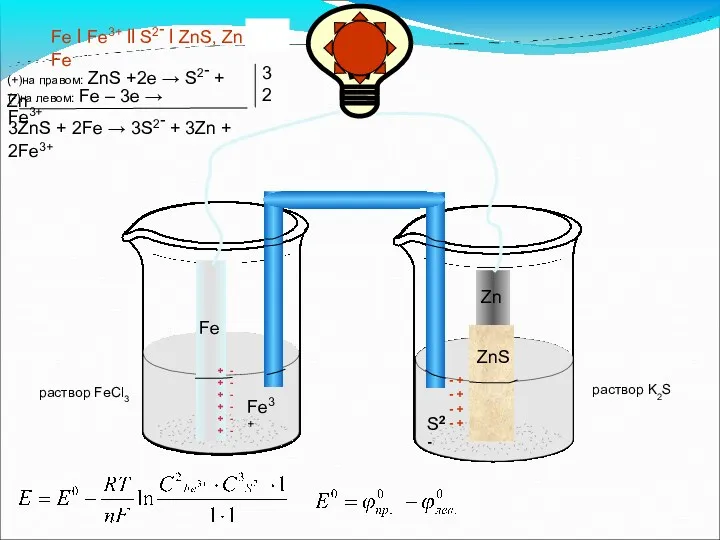
- 31. В общем случае, ЭДС элемента рассчитывают по уравнению Нернста для элемента: (3.6) где и - активности
- 32. 3.4. Термодинамика гальванического элемента. Измерение ЭДС. Компенсационный метод измерения ЭДС позволяет: проводить измерение при минимальном прохождении
- 33. Примечание: Измерение ЭДС вольтметром с низким уровнем внутреннего сопротивления вызывает значительный ток, протекающий через прибор; При
- 34. Термодинамические функции Методы измерение ЭДС позволяют определить: максимальную работу тепловой эффект реакции константу равновесия изменение энтропии
- 35. Изменение энергии Гиббса: Изменение энтропии: (3.9) где -температурный коэффициент ЭДС Уравнение Гиббса – Гельмгольца: Используется для
- 36. Уравнение изотермы Вант – Гоффа: При стандартных условиях, имеет вид: (3.12) Константа равновесия химической реакции: С
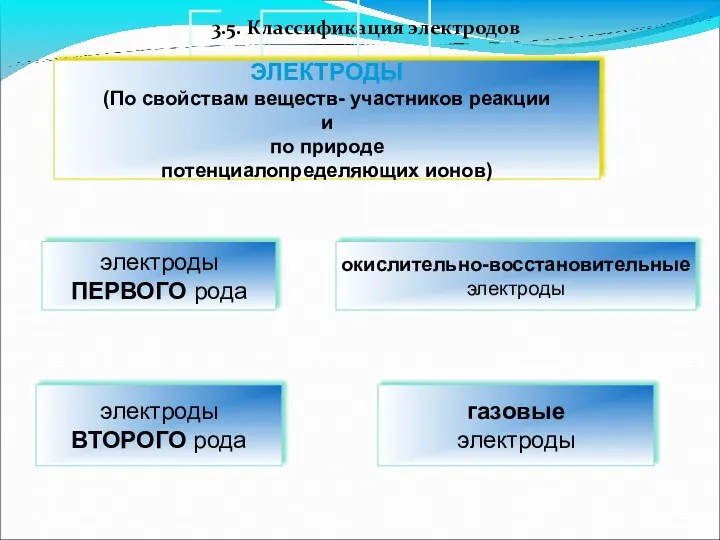
- 37. 3.5. Классификация электродов
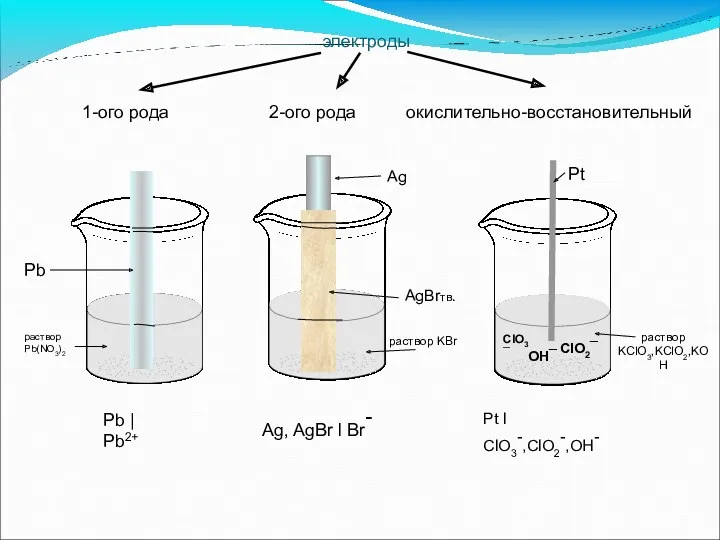
- 38. электроды 1-ого рода 2-ого рода окислительно-восстановительный Pb | Pb2+ Pb раствор Pb(NO3)2 Ag AgBrтв. раствор KBr
- 39. Электроды первого рода: Определение: Электроды, потенциал которых определяется концентрацией катионов или анионов, называются электродами первого рода.
- 40. 2. Электроды второго рода: Определение: Электроды, представляющие собой систему, в которой металл покрыт слоем труднорастворимой соли
- 41. Обратимость электродов второго рода Пример: Обратимость хлорсеребряного электрода, по отношению к ионам серебра, определяется электродным равновесием:
- 42. В таком случае, потенциал электрода примет вид: или (3.15) Уравнение отражает обратимость электрода к анионам. При
- 43. Хлорсеребряный электрод-электрод сравнения В насыщенном растворе KCl при температуре 25оС потенциал хлорсеребряного электрода φ = 0,22
- 44. Электроды 2 рода Условная запись: Ag, AgCl│Cl- Электродная реакция: AgCl↓ + ē ↔ Ago + Cl-
- 46. 3.Окислительно-восстановительные (Ox-Red) электроды: На любом электроде протекает окислительно-восстановительная полуреакция: В реакции участвует одно и то же
- 47. Если металл является инертным, то такие электродные системы называются окислительно-восстановительными электродами. Примечание: Инертные металлы не участвует
- 48. Пример: Если поместить платиновую пластинку в раствор, содержащий ионы и ; То ионы , обладая окислительной
- 49. Потенциал окислительно-восстановительного электрода рассчитывается по уравнению Нернста: (3.16) где - число зарядов, участвующих в электродной реакции.
- 50. Газовые электроды Среди окислительно-восстановительных электродов выделяют газовые электроды. Газовыми электродами называют системы инертных металлов ( ,
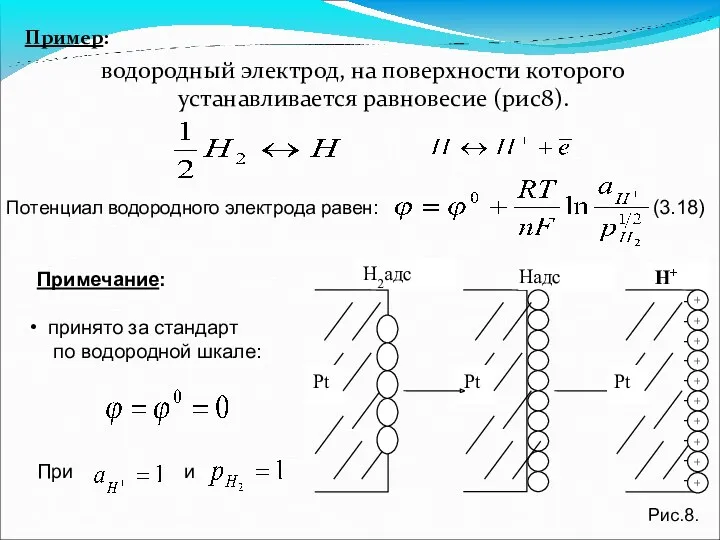
- 51. Пример: водородный электрод, на поверхности которого устанавливается равновесие (рис8). Потенциал водородного электрода равен: (3.18) Примечание: принято
- 52. Таким образом, потенциал водородного электрода: (3.19) Переходя к десятичным логарифмам при Т=298К получаем: (3.20) если ,
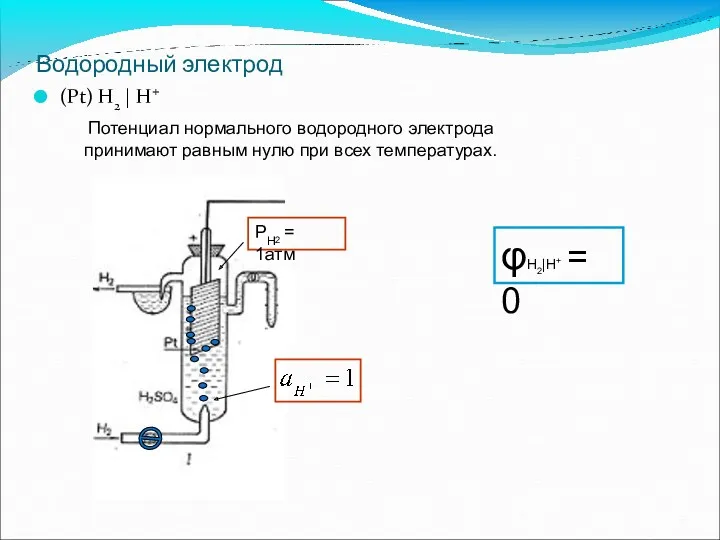
- 53. Водородный электрод (Pt) H2 | H+ Потенциал нормального водородного электрода принимают равным нулю при всех температурах.
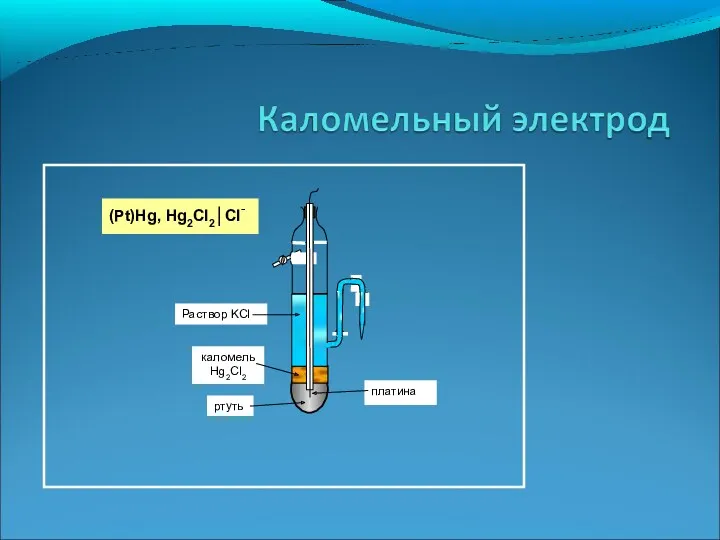
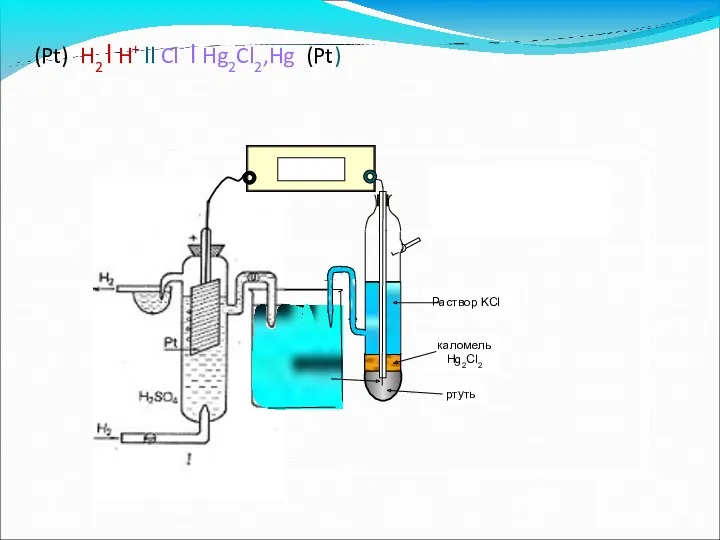
- 54. (Pt) H2 l H+ ll Cl- l Hg2Cl2,Hg (Pt)
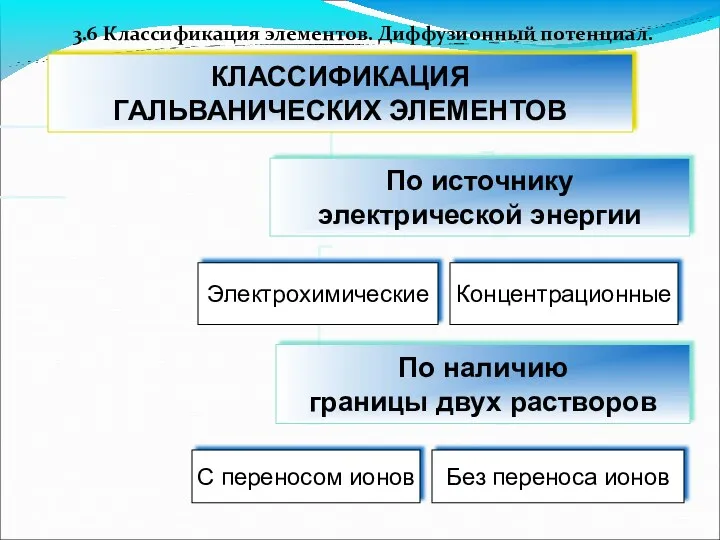
- 55. 3.6 Классификация элементов. Диффузионный потенциал.
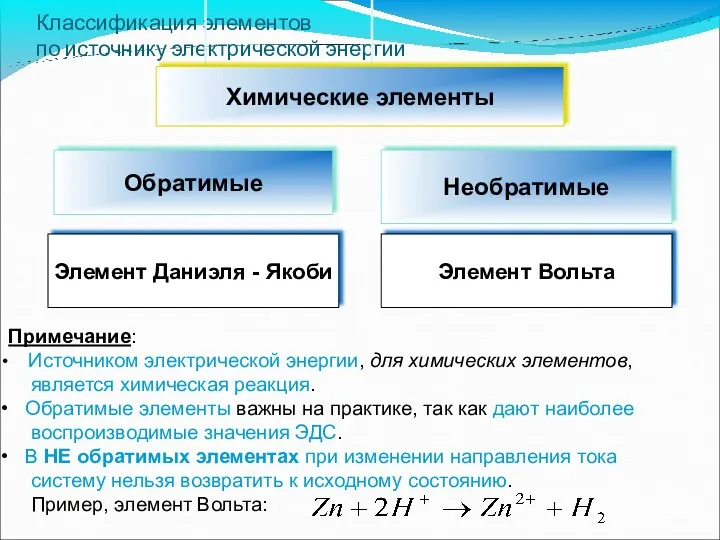
- 56. Классификация элементов по источнику электрической энергии Примечание: Источником электрической энергии, для химических элементов, является химическая реакция.
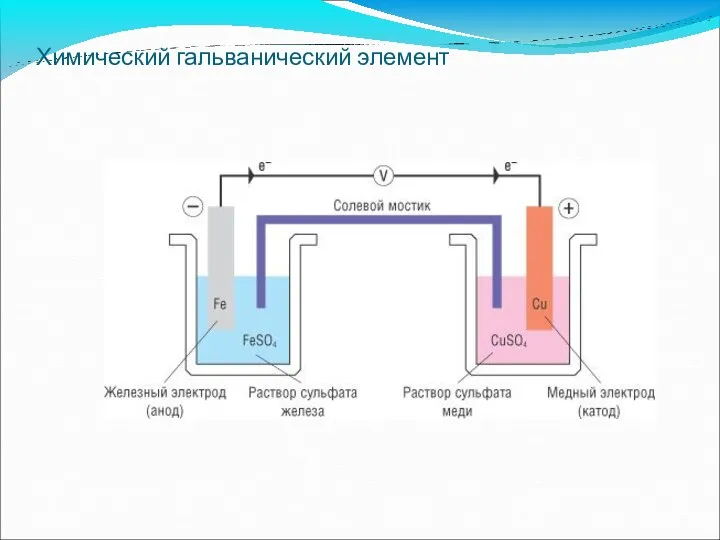
- 57. Химический гальванический элемент
- 58. Концентрационные элементы - элементы, в которых источником электрической энергии служат процессы выравнивания концентраций растворов. Пример: Если
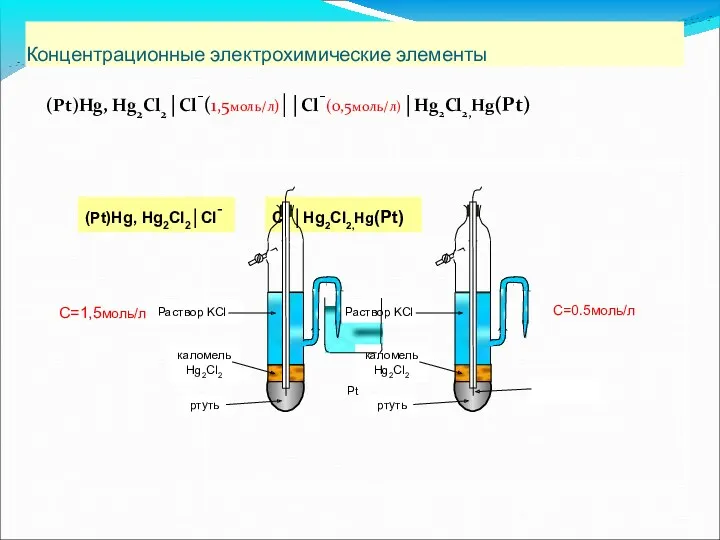
- 59. Концентрационные электрохимические элементы (Pt)Hg, Hg2Cl2│Cl-(1,5моль/л)|│Cl-(0,5моль/л)│Hg2Cl2,Hg(Pt) ртуть Раствор KCl каломель Hg2Cl2 (Pt)Hg, Hg2Cl2│Cl- Pt C=0.5моль/л С=1,5моль/л
- 60. На границе двух растворов возникает диффузионный потенциал. Ионы, обладающие большей подвижностью, диффундируют раньше. В результате, на
- 61. Если , то более разбавленный раствор зарядится положительно, а жидкостная граница со стороны более концентрированного раствора
- 62. Примечание: На границах раздела растворов различных электролитов расчет диффузионного потенциала более сложен. Если электролиты имеют общий
- 63. Элементами с переносом ионов называются гальванические элементы, имеющие жидкостную границу. Элементами без переноса ионов называются гальванические
- 64. Пример: Гальванический элемент без переноса ионов Рассмотрим элемент, составленный: из водородного и хлорсеребряного электродов, погруженных в
- 65. Сухие элементы Анодом в сухом элементе служит цинковая оболочка 1, а катодом - графитовый стержень 2,
- 66. Ионообменные электроды
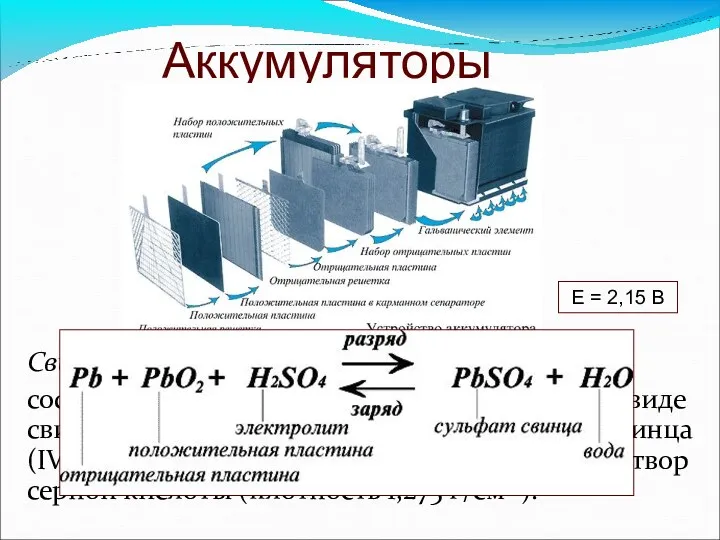
- 67. Аккумуляторы Свинцовый аккумулятор: состоит из свинцовых анодов и катодов в виде свинцовой решетки, заполненной оксидом свинца(IV).
- 68. Топливные элементы В топливном элементе протекает реакция окисления топлива или продуктов его переработки (водорода, оксида углерода,
- 69. По словам инженеров компании Canon, на 0,6 кубический сантиметр топливного элемента приходится один Вт·ч. То есть,
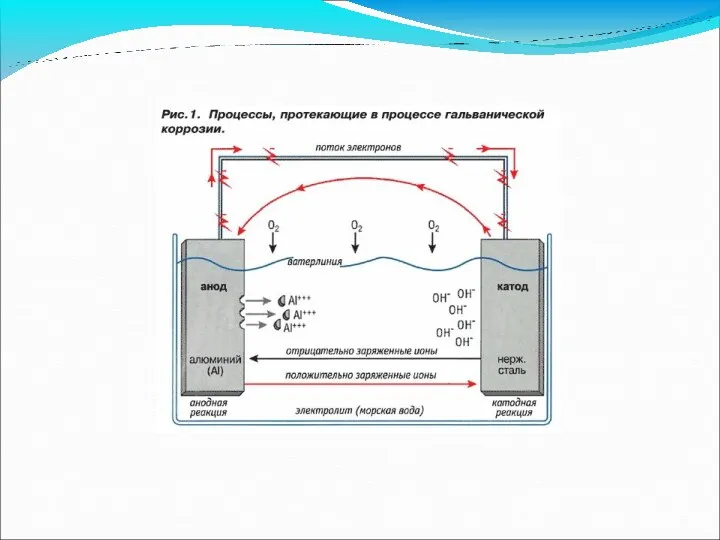
- 70. + + + + - - - - Zn| раствор электролита |Cu При электрохимической коррозии: более
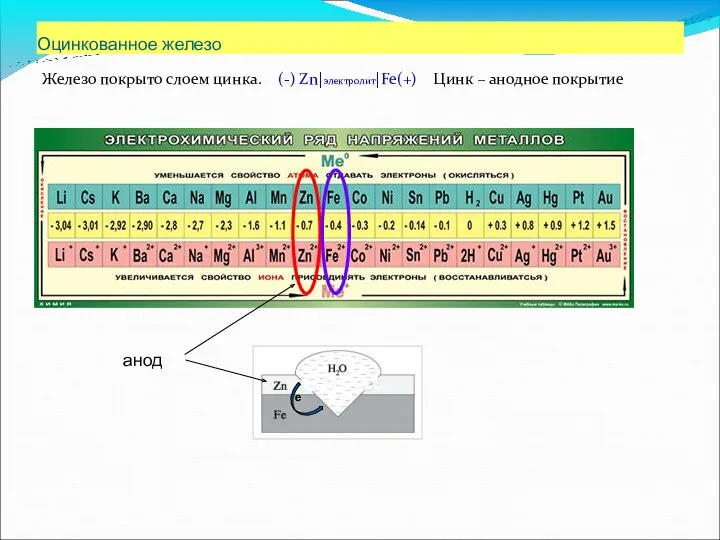
- 71. Оцинкованное железо Железо покрыто слоем цинка. (-) Zn|электролит|Fe(+) Цинк – анодное покрытие анод е
- 74. Скачать презентацию

















































 Органическая химия
Органическая химия Растворение. Растворимость веществ в воде. Классификация растворов
Растворение. Растворимость веществ в воде. Классификация растворов Железо и его соединения
Железо и его соединения Хімічні властивості алканів
Хімічні властивості алканів Щелочные породы среднего состава
Щелочные породы среднего состава Применение уксусной кислоты
Применение уксусной кислоты Металлы. Металлы главной подгруппы
Металлы. Металлы главной подгруппы Алюміній. Загальна характеристика, властивості. Алюміній оксид, алюміній гідроксид, їх амфотерність
Алюміній. Загальна характеристика, властивості. Алюміній оксид, алюміній гідроксид, їх амфотерність Чипсы: вред или польза
Чипсы: вред или польза Подготовка проб к анализу в лаборатории. Продолжение. Лекция 5
Подготовка проб к анализу в лаборатории. Продолжение. Лекция 5 Определение качественного состава минеральных вод
Определение качественного состава минеральных вод Металлы – простые вещества
Металлы – простые вещества Гальванический элемент Даниэля-Якоби. Потенцометрия. Стеклянный электрод
Гальванический элемент Даниэля-Якоби. Потенцометрия. Стеклянный электрод Теплота сгорания топлива
Теплота сгорания топлива 20230316_otkrytyy_urok_v_8_kl_geneticheskaya_svyaz.docx
20230316_otkrytyy_urok_v_8_kl_geneticheskaya_svyaz.docx Электролитическая диссоциация
Электролитическая диссоциация Характеристика неметаллов. Галогены
Характеристика неметаллов. Галогены Оксиды серы. Сернистая кислота
Оксиды серы. Сернистая кислота Получение галогенов. Биологическое значение и применение галогенов и их соединений
Получение галогенов. Биологическое значение и применение галогенов и их соединений Природные источники углеводородов, их переработка, применение и экологические проблемы. 10 класс
Природные источники углеводородов, их переработка, применение и экологические проблемы. 10 класс Степень окисления
Степень окисления Анализ жидких средств для мытья посуды
Анализ жидких средств для мытья посуды Классификация химических реакций, протекающих с изменением состава веществ
Классификация химических реакций, протекающих с изменением состава веществ Аммиак. 9 класс
Аммиак. 9 класс Поверхностные явления
Поверхностные явления Тайна мыльного пузыря
Тайна мыльного пузыря Нуклеиновые кислоты, их структурные компоненты
Нуклеиновые кислоты, их структурные компоненты Современные проблемы химической технологии вяжущих материалов
Современные проблемы химической технологии вяжущих материалов