Слайд 2

“...Да! Это была собака, огромная, черная, как смоль. Но такой собаки
еще никто из нас, смертных, не видывал. Из ее отверстой пасти вырывалось пламя, глаза метали искры, по морде и загривку переливался мерцающий огонь. Ни в чьем воспаленном мозгу не могло возникнуть видение более страшное, более омерзительное, чем это адское существо, выскочившее на нас из тумана... Страшный пес, величиной с молодую львицу. Его огромная пасть все еще светилась голубоватым пламенем, глубоко сидящие дикие глаза были обведены огненными кругами. Я дотронулся до этой светящейся головы и, отняв руку, увидел, что мои пальцы тоже засветились в темноте. Фосфор, – сказал я”.
Слайд 3

Слайд 4

Гамбургский алхимик
Хеннинг Бранд
1669 год
Слайд 5

Содержание
Строение атома фосфора
Аллотропные модификации фосфора
Нахождение в природе
Химические свойства фосфора
Получение фосфора
Фосфин
Оксид фосфора
(Оксид фосфора (VОксид фосфора (V)
Ортофосфорная кислота
Соли фосфорной кислоты
Слайд 6

Строение атома фосфора
Элемент VA группы имеет электронную формулу 1s22s22p63s23p3.
Фосфор –
неметалл.
Наиболее характерные степени окисления: +5, +3, 0, -3.
Оксиды Э2О5 и Э2О3 имеют кислотные свойства.
Летучее водородное соединение – фосфин PH3.
Слайд 7
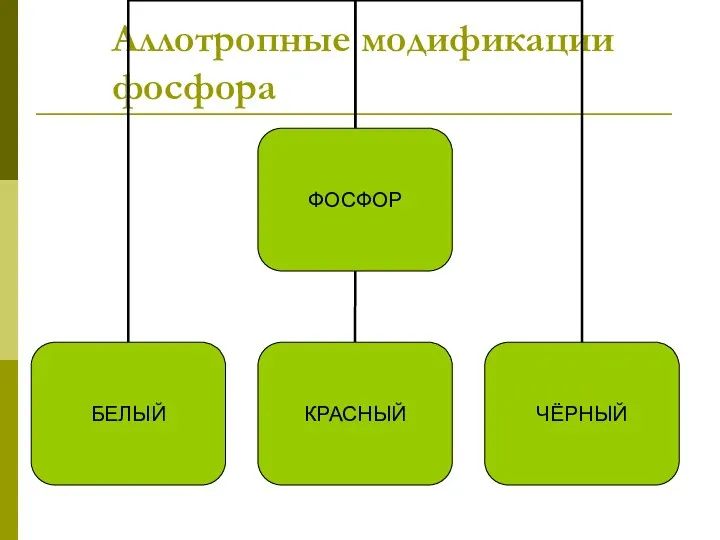
Аллотропные модификации фосфора
Слайд 8

Нахождение в природе
Организм человека- 1,5 кг фосфора:
в костях - 1,4кг,
в
мышцах - 130г,
в нервной ткани - 13 г.
Суточное потребление фосфора – около 2 г.
В природе:
важнейшие минералы: апатит и фосфорит Ca3(PO4)2. наиболее распространен фторапатит 3Ca3(PO4)2· CaF2.
Слайд 9

Химические свойства фосфора
2P + 3Ca → Ca3P2
4P + 3O2(недостат)
→ 2P2O3 (P4O6)
4P + 5O2(избыток) → 2P2O5 (P4O10)
4P + 6Cl2(недостат) → 4PCl3
2P + 5Cl2(избыток) → 2PCl5
2P + 3S → P2S3
2P + 5S → P2S5
2P + 5H2SO4(к) → 5SO2↑ + 2H3PO4 + 2H2O
P + 5HNO3(к) → 5NO2↑ + H3PO4 + H2O
3P + 5HNO3(разб) + 2H2O → 5NO↑ + 3H3PO4
Слайд 10
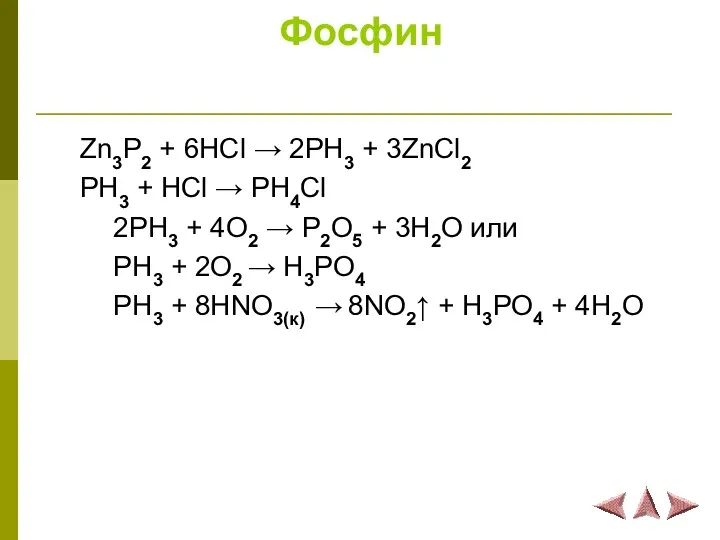
Фосфин
Zn3P2 + 6HCl → 2PH3 + 3ZnCl2
PH3 + HCl → PH4Cl
2PH3 + 4O2 → P2O5 + 3H2O или
PH3 + 2O2 → H3PO4
PH3 + 8HNO3(к) → 8NO2↑ + H3PO4 + 4H2O
Слайд 11

Оксид фосфора (V)
4Р + 5О2 → 2Р2О5
P2O5 + H2O → 2HPO3
P2O5 + 3H2O → 2H3PO4
P2O5 + 3CaO → Ca3(PO4)2
P2O5 +3Ca(OH)2 → Ca3(PO4)2 + 3H2O
Слайд 12
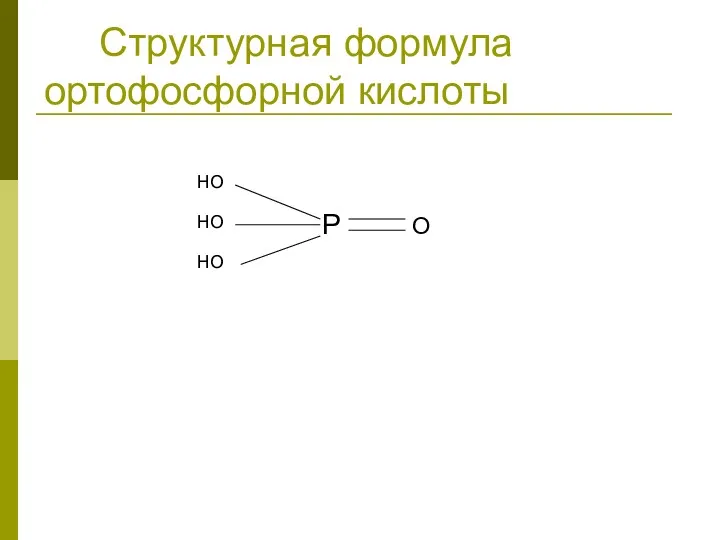
Структурная формула ортофосфорной кислоты
P
O
HO
HO
HO
Слайд 13

Химические свойства ортофосфорной кислоты
1.С металлами, стоящими в ряду напряжения
металлов до
водорода:
3Mg + 2H3PO4 → Mg3(PO4)2 + 3H2↑
2.С основными оксидами:
3CaO + 2H3PO4 → Сa3(PO4)2 + 3H2O
3.С основаниями:
H3PO4 + NH3 → (NH4)2HPO4
Слайд 14
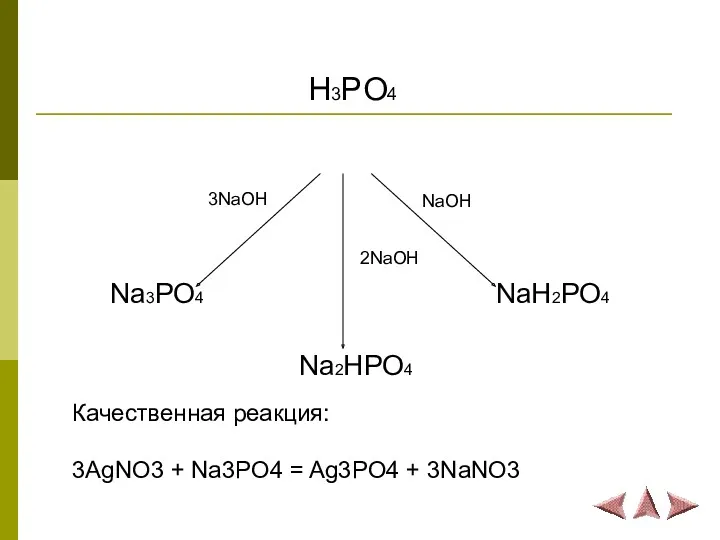
H3PO4
Na3PO4
Na2HPO4
NaH2PO4
3NaOH
2NaOH
NaOH
Качественная реакция:
3AgNO3 + Na3PO4 = Ag3PO4 + 3NaNO3
Слайд 15

Получить следующие соли:
Гидрофосфат кальция
Дигидрофосфат натрия
Фосфат серебра














 Общая характеристика неметаллов
Общая характеристика неметаллов Химия и повседневная жизнь человека
Химия и повседневная жизнь человека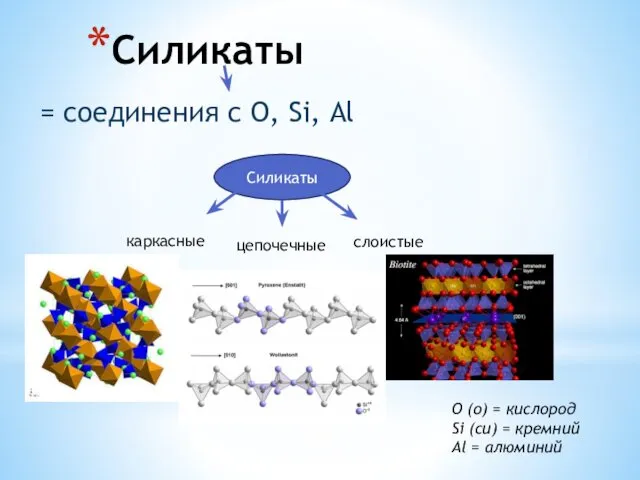 Силикаты. Слюды. Тальк. Фосфаты. Апатит. Крокоит
Силикаты. Слюды. Тальк. Фосфаты. Апатит. Крокоит Аморфные сплавы
Аморфные сплавы Электролиз. Классификация
Электролиз. Классификация Химическая термодинамика. Экзаменационные вопросы
Химическая термодинамика. Экзаменационные вопросы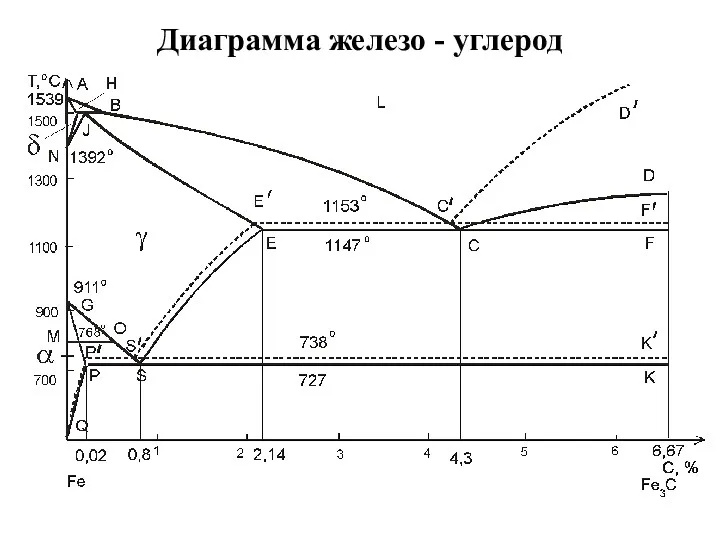 Диаграмма железо - углерод
Диаграмма железо - углерод Хром. Химиялық қасиеттері
Хром. Химиялық қасиеттері Анализ 3% раствора водорода пероксида
Анализ 3% раствора водорода пероксида Alkynes
Alkynes Металлическая связь
Металлическая связь Аминокислоты алифатического ряда и их производные
Аминокислоты алифатического ряда и их производные Комплексные соединения
Комплексные соединения Історія відкриття періодичної системи хімічних елементів
Історія відкриття періодичної системи хімічних елементів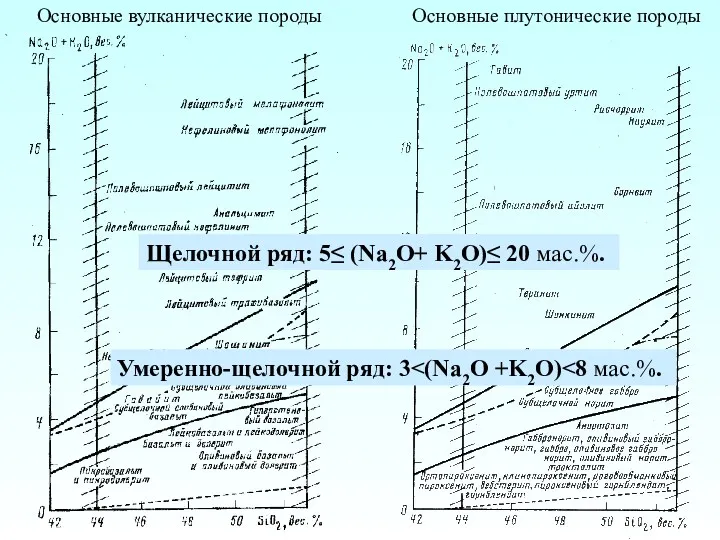 Основные вулканические породы. Основные плутонические породы
Основные вулканические породы. Основные плутонические породы Утворення асимілятів та їхнє перетворення
Утворення асимілятів та їхнє перетворення Технология промышленных газов
Технология промышленных газов Кислотно-основное титрование
Кислотно-основное титрование Химические свойства алкенов
Химические свойства алкенов Алкалоидтар. Алкалоидтар туралы түсінік. Жіктелуі
Алкалоидтар. Алкалоидтар туралы түсінік. Жіктелуі Элементы пятой-А группы. Азот и фосфор
Элементы пятой-А группы. Азот и фосфор Анілін. Фізичні властивості
Анілін. Фізичні властивості Тағамдық қоспалар. Тағамдық бояулар. Антиоксиданттар. Эмульгаторлар
Тағамдық қоспалар. Тағамдық бояулар. Антиоксиданттар. Эмульгаторлар Анализ анионов. Анализ смеси солей
Анализ анионов. Анализ смеси солей Жиры. История открытия, строение, классификация, свойства
Жиры. История открытия, строение, классификация, свойства Активные формы кислорода. Антиоксиданты их физиологическая роль
Активные формы кислорода. Антиоксиданты их физиологическая роль Д.И. Менделеев Мощь и сила науки во множестве фактов, цель – в обобщении этого множества
Д.И. Менделеев Мощь и сила науки во множестве фактов, цель – в обобщении этого множества 20230419_oksidy
20230419_oksidy