Содержание
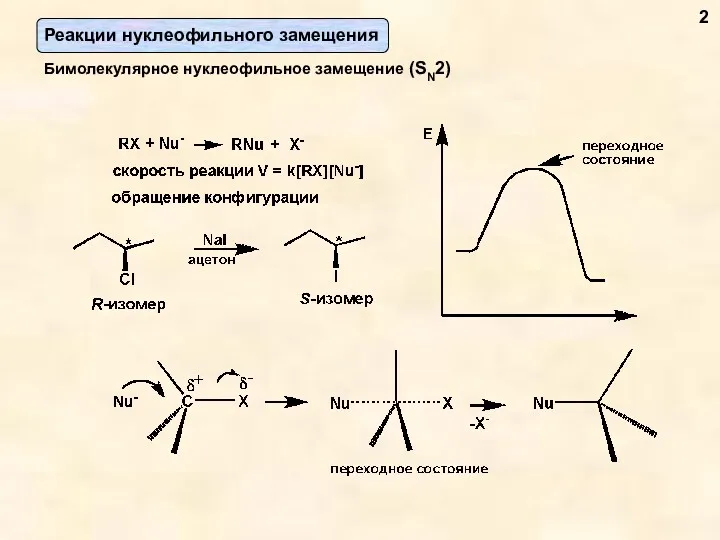
- 2. Бимолекулярное нуклеофильное замещение (SN2) 2
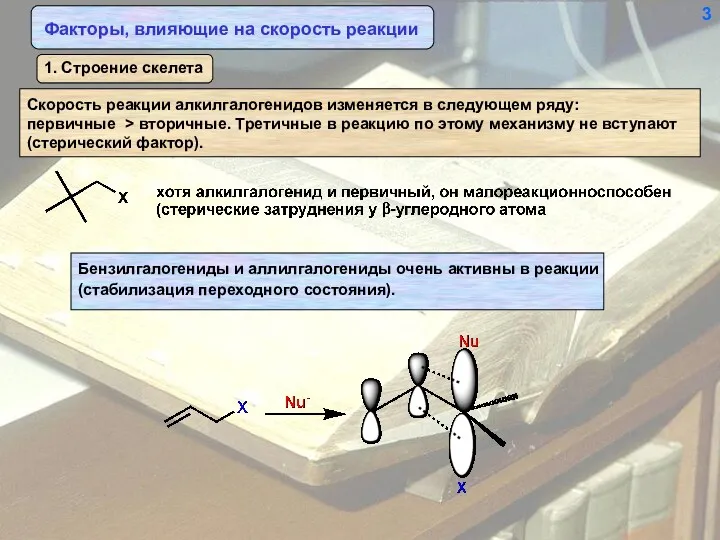
- 3. 3
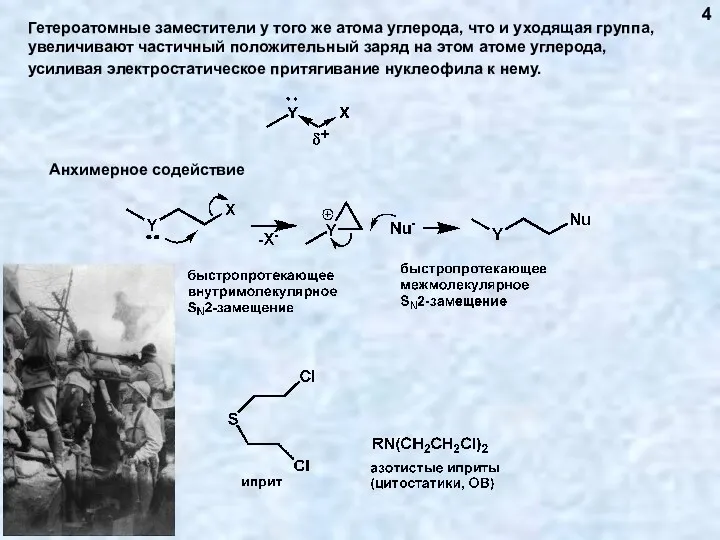
- 4. Гетероатомные заместители у того же атома углерода, что и уходящая группа, увеличивают частичный положительный заряд на
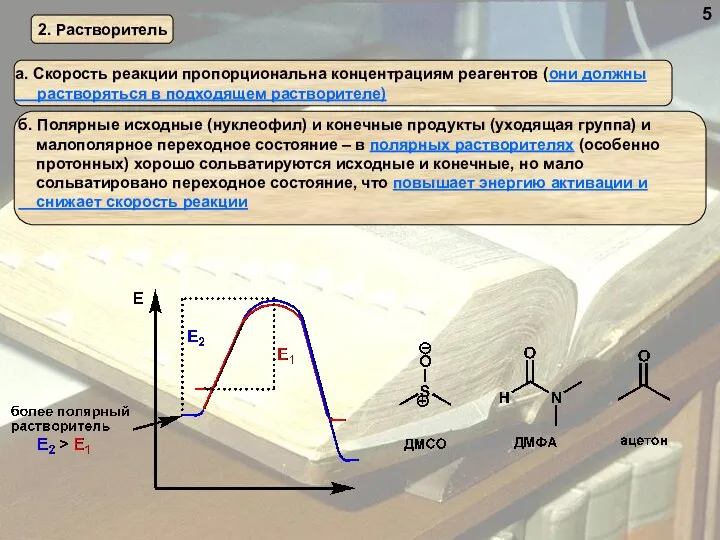
- 5. 5
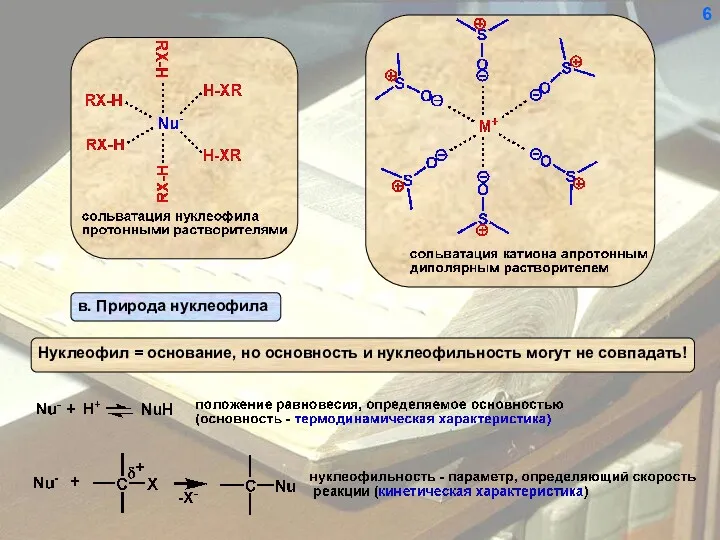
- 6. 6
- 7. 7
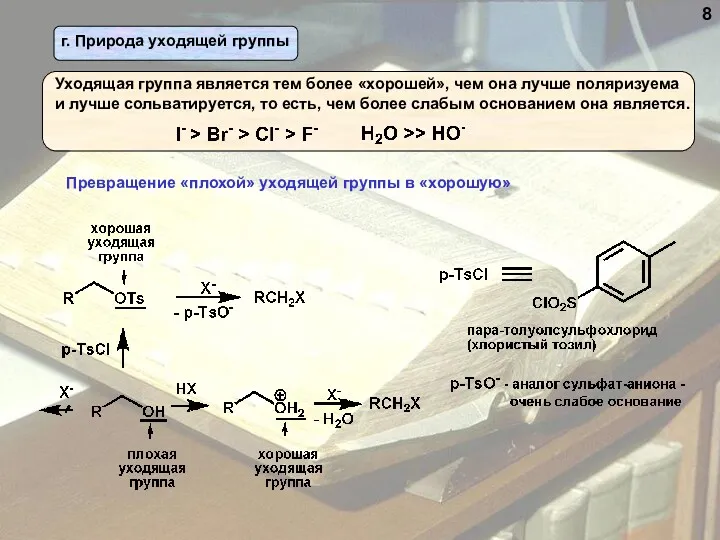
- 8. Превращение «плохой» уходящей группы в «хорошую» 8
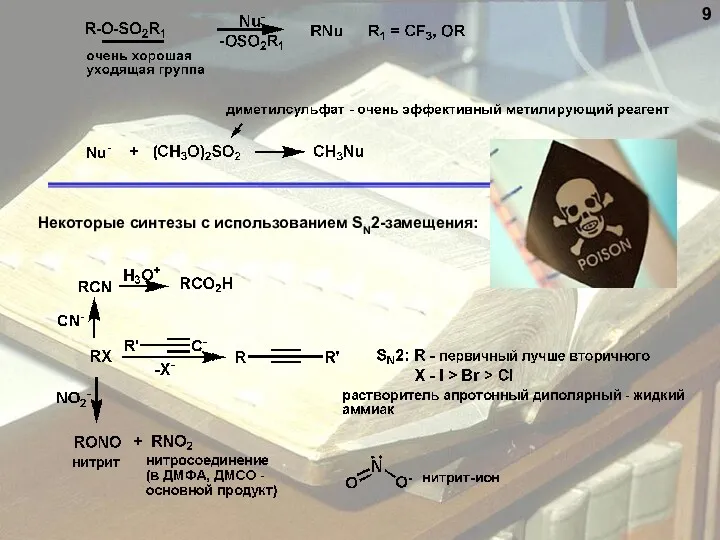
- 9. 9
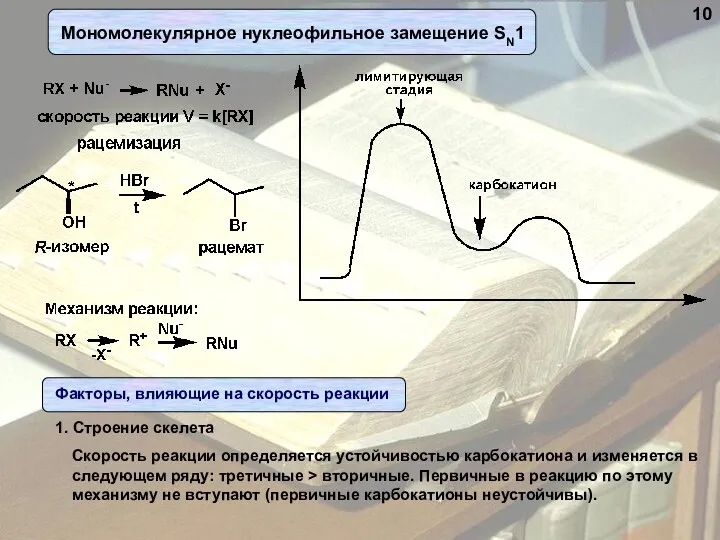
- 10. Мономолекулярное нуклеофильное замещение SN1 10
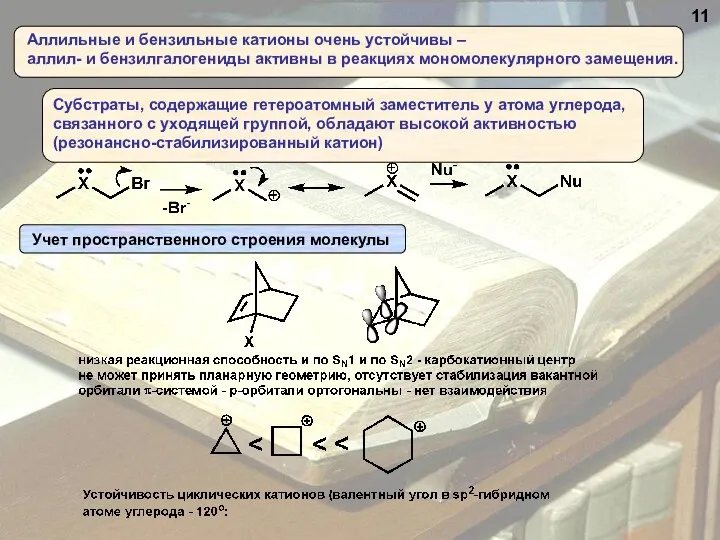
- 11. 11
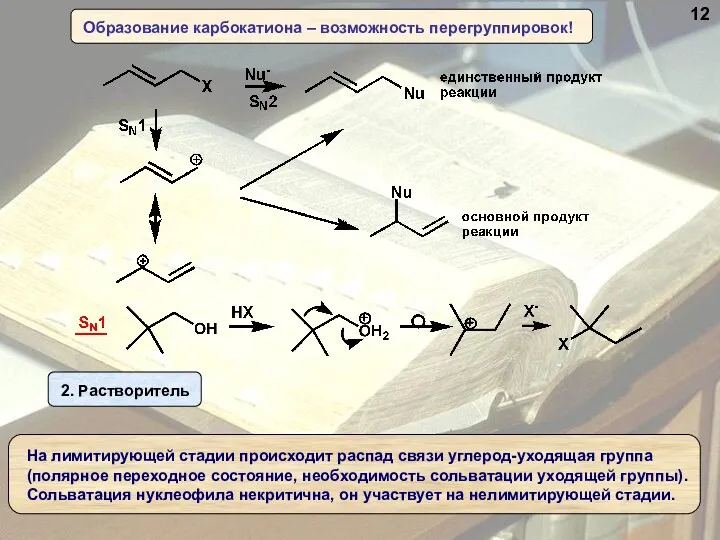
- 12. Образование карбокатиона – возможность перегруппировок! 12
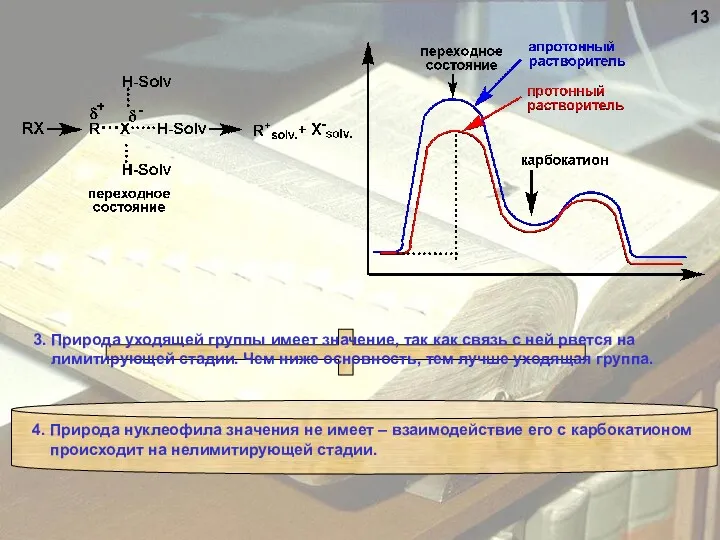
- 13. 13
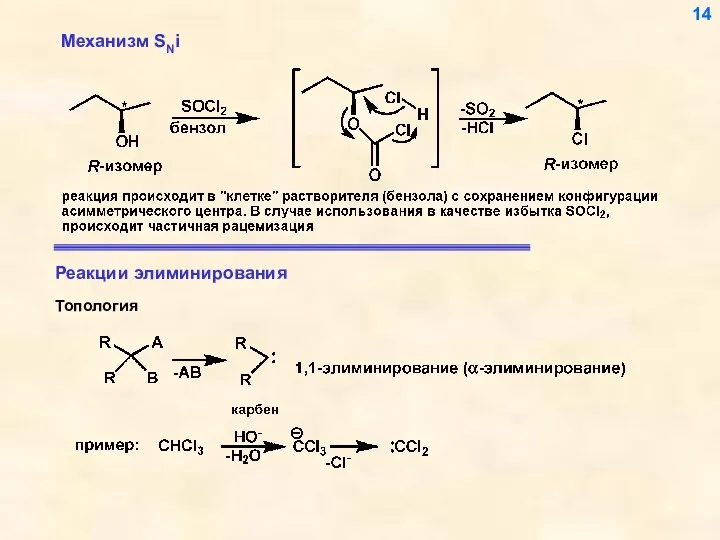
- 14. Механизм SNi Топология 14
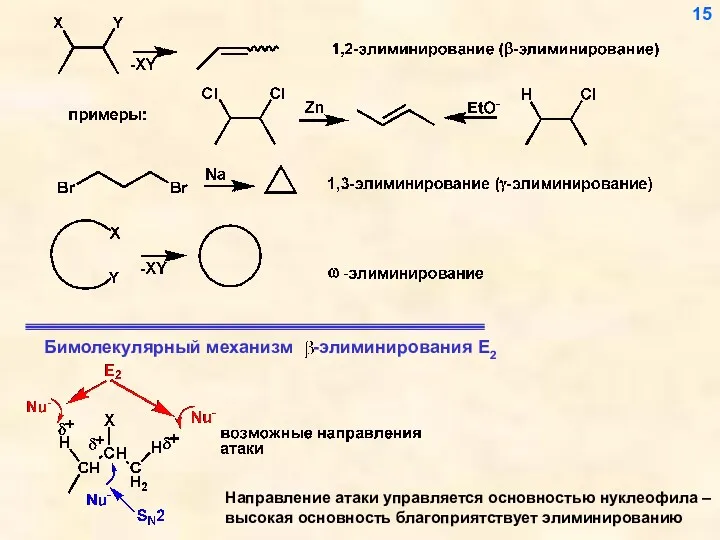
- 15. Направление атаки управляется основностью нуклеофила – высокая основность благоприятствует элиминированию 15
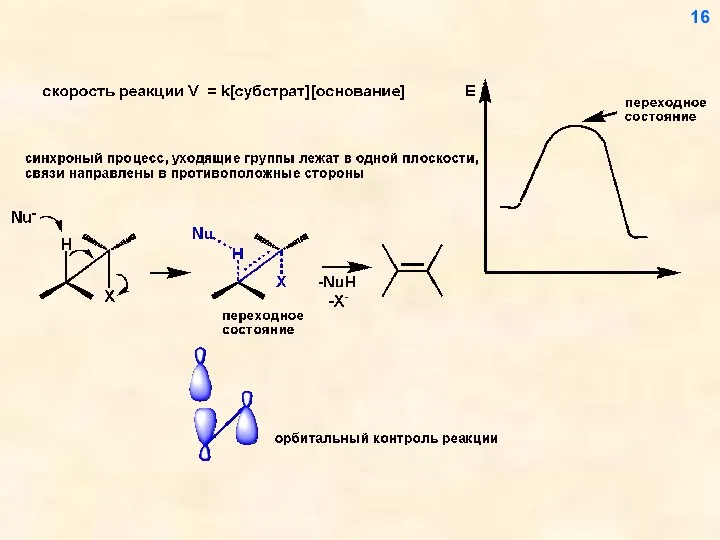
- 16. 16
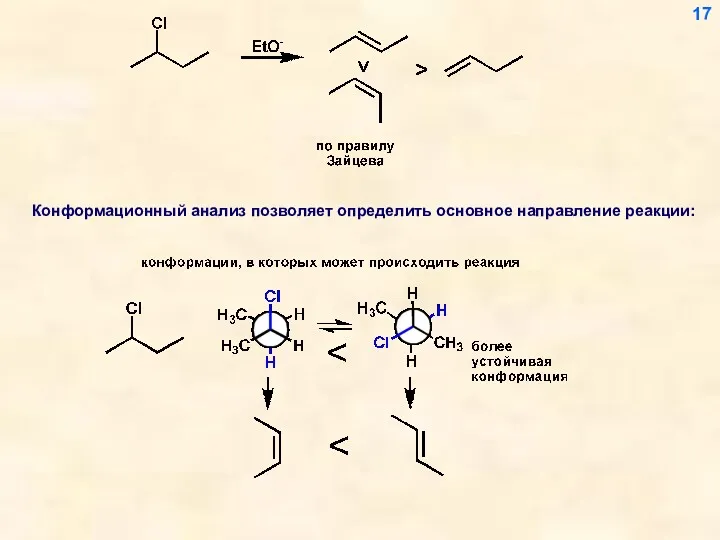
- 17. Конформационный анализ позволяет определить основное направление реакции: 17
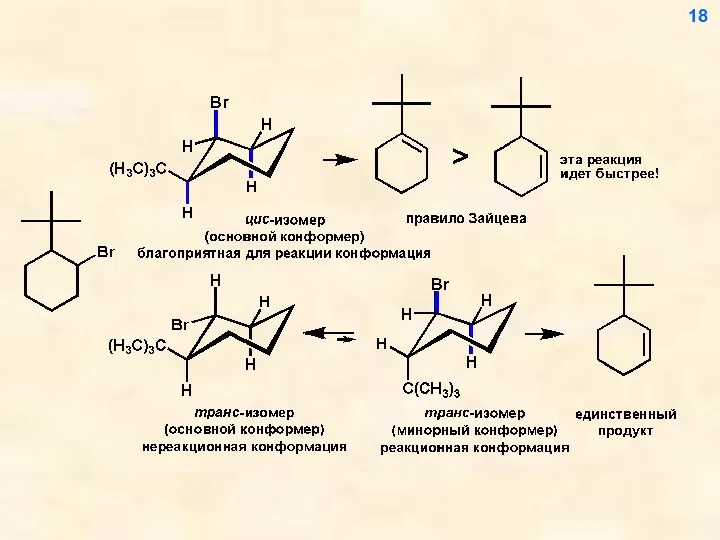
- 18. 18
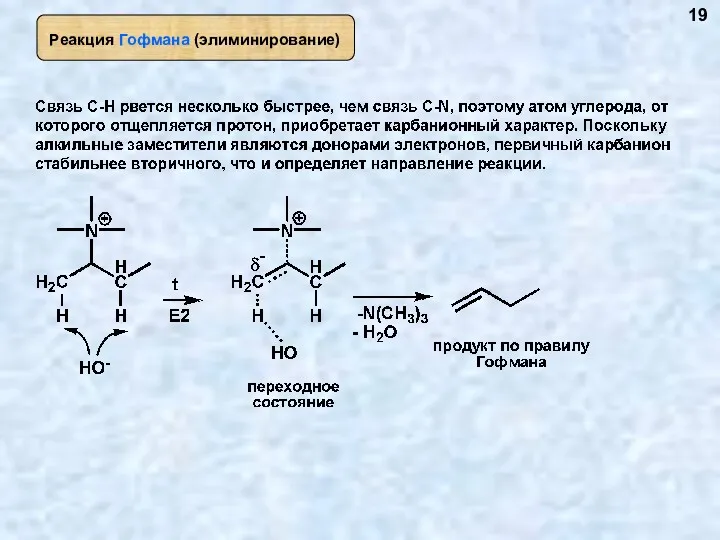
- 19. 19
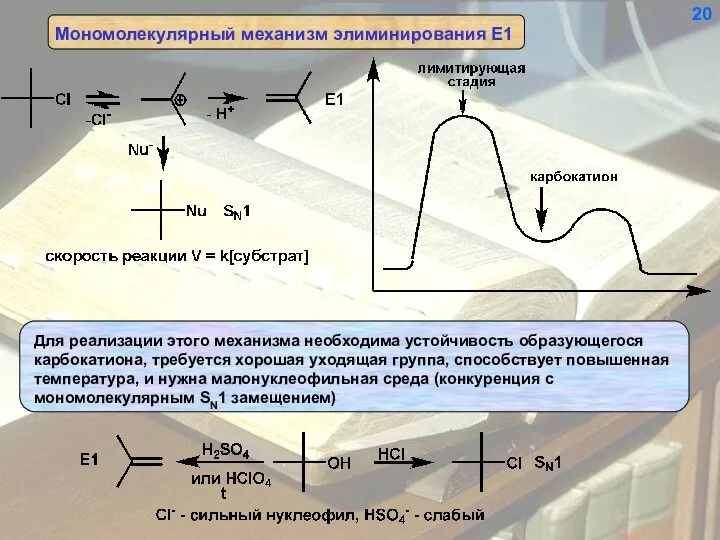
- 20. 20
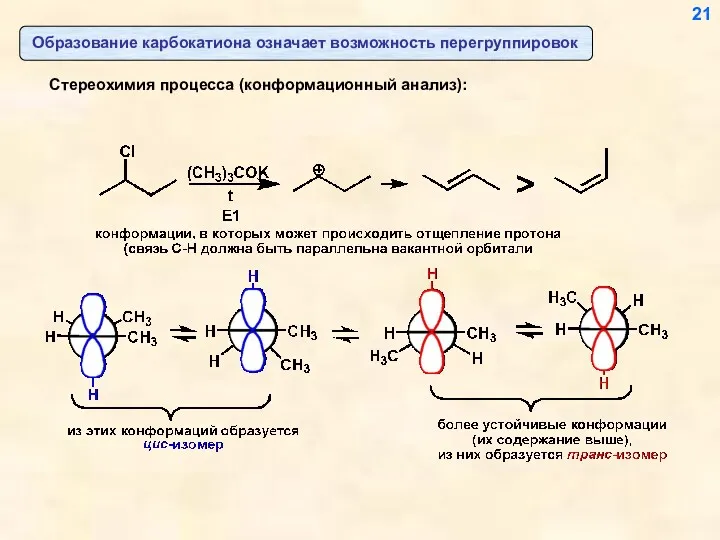
- 21. Образование карбокатиона означает возможность перегруппировок Стереохимия процесса (конформационный анализ): 21
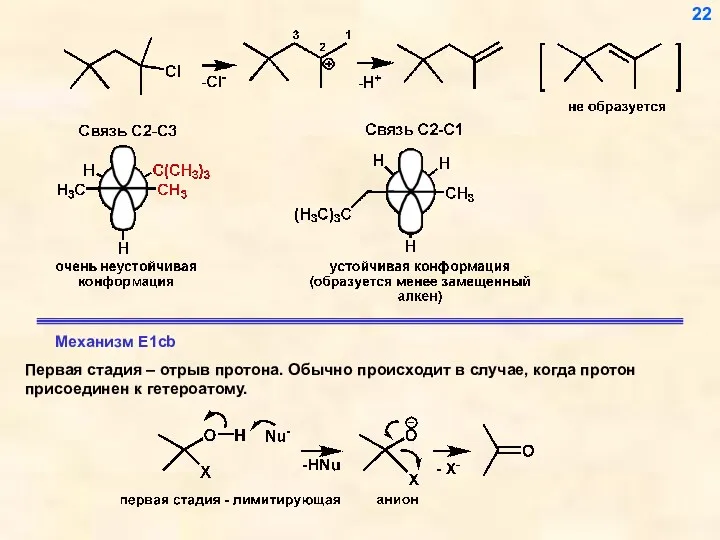
- 22. Первая стадия – отрыв протона. Обычно происходит в случае, когда протон присоединен к гетероатому. 22
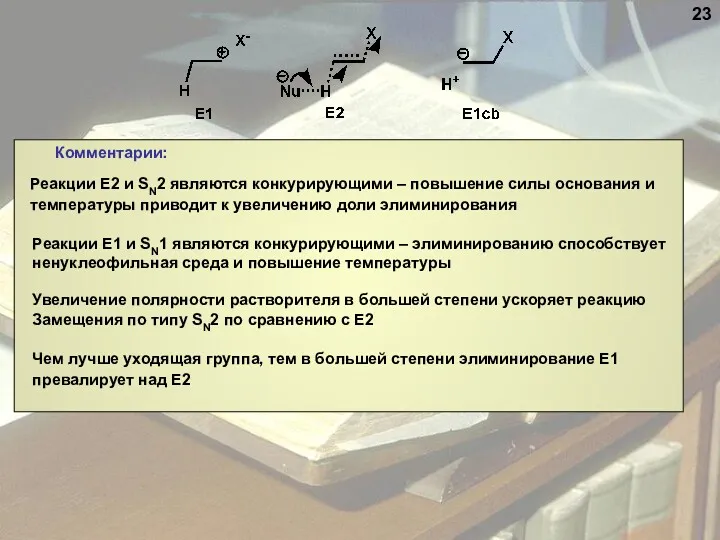
- 23. Комментарии: Реакции Е2 и SN2 являются конкурирующими – повышение силы основания и температуры приводит к увеличению
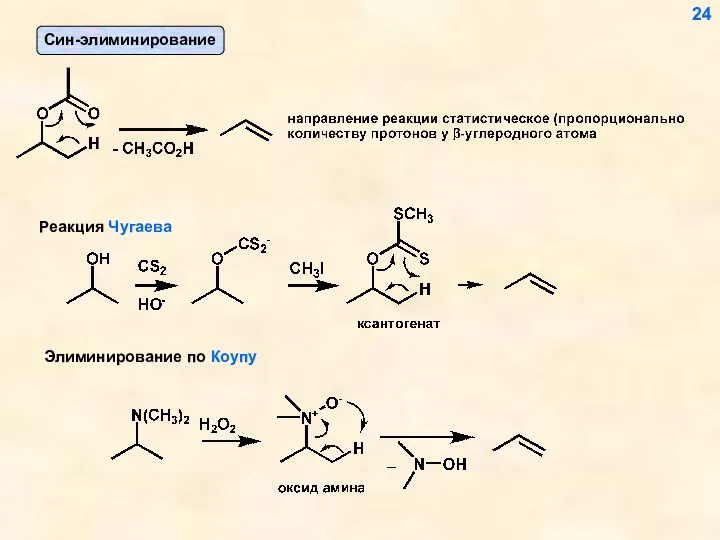
- 24. 24
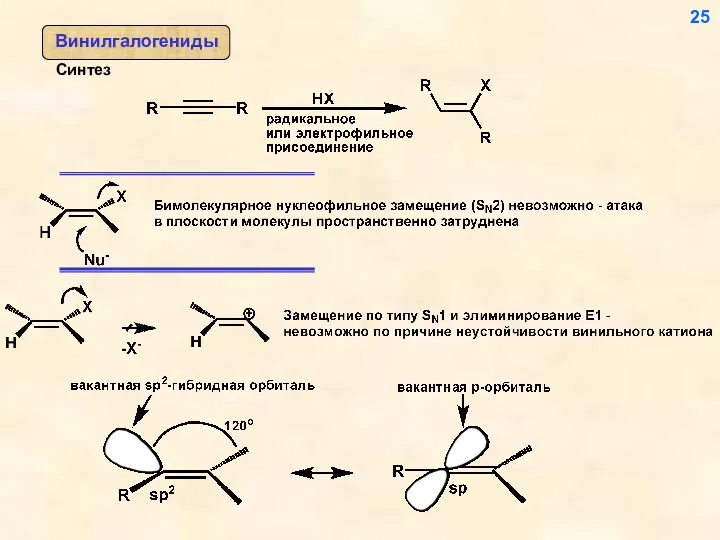
- 25. 25
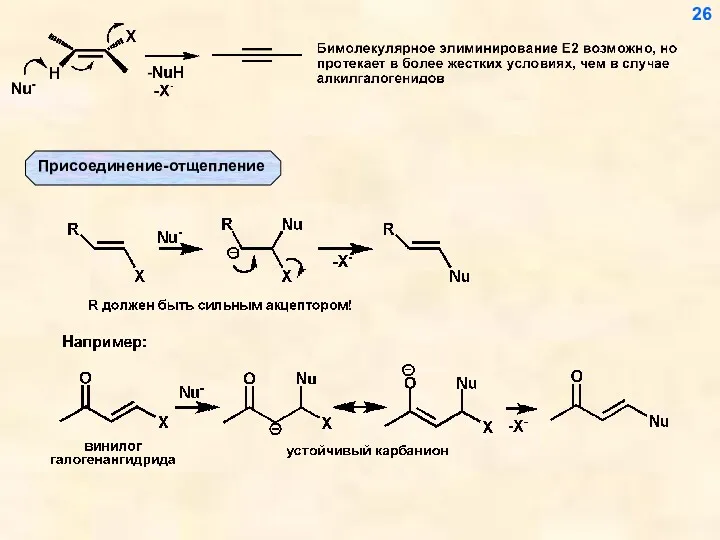
- 26. 26
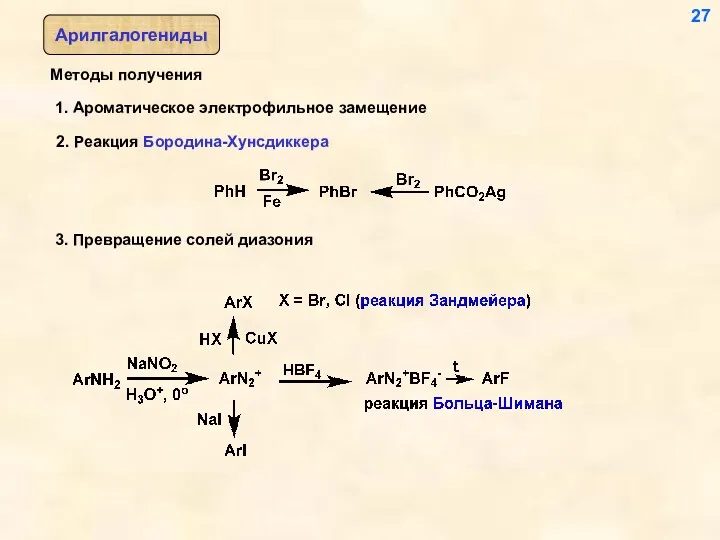
- 27. Методы получения 1. Ароматическое электрофильное замещение 27
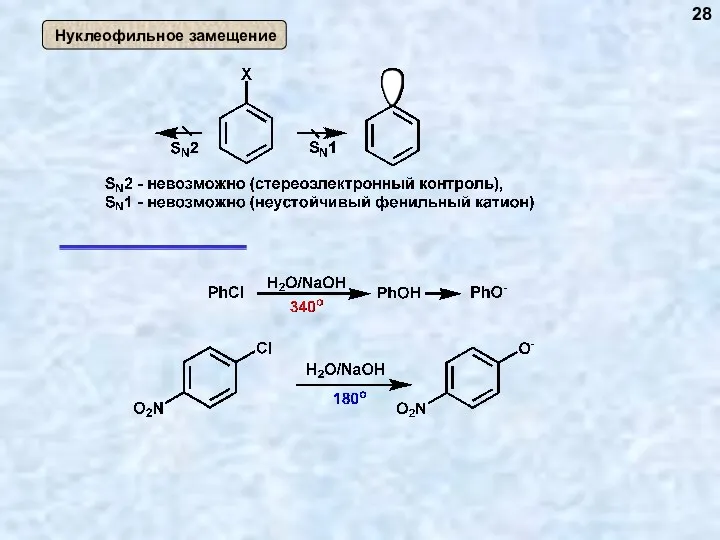
- 28. 28
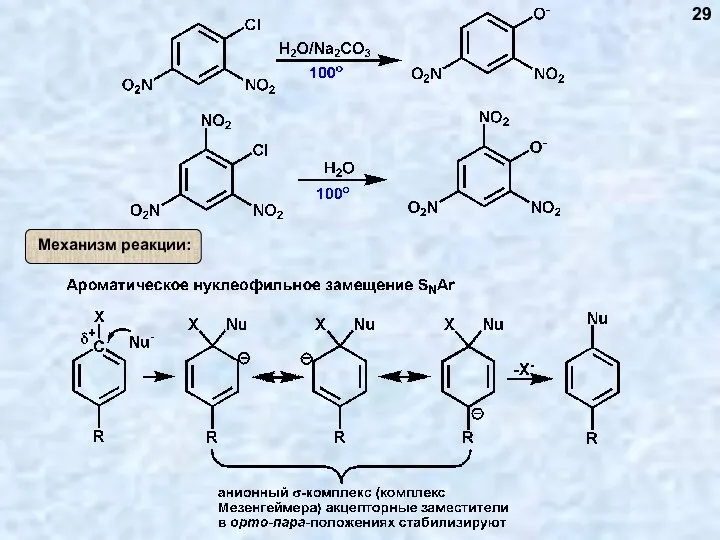
- 29. 29
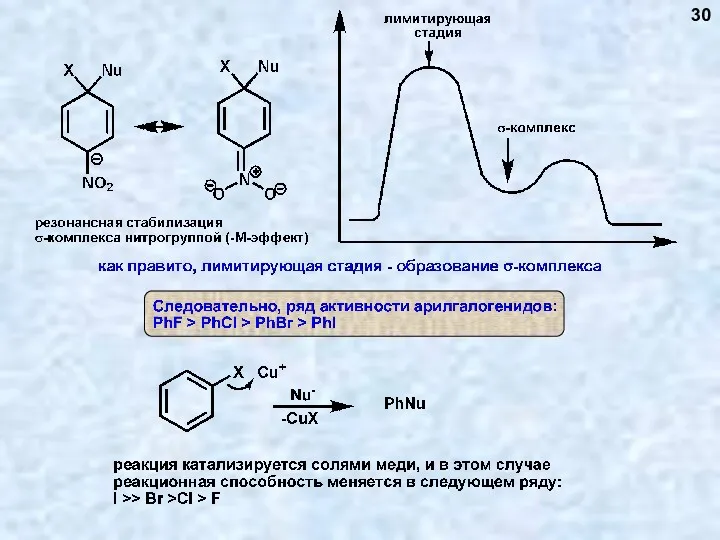
- 30. 30
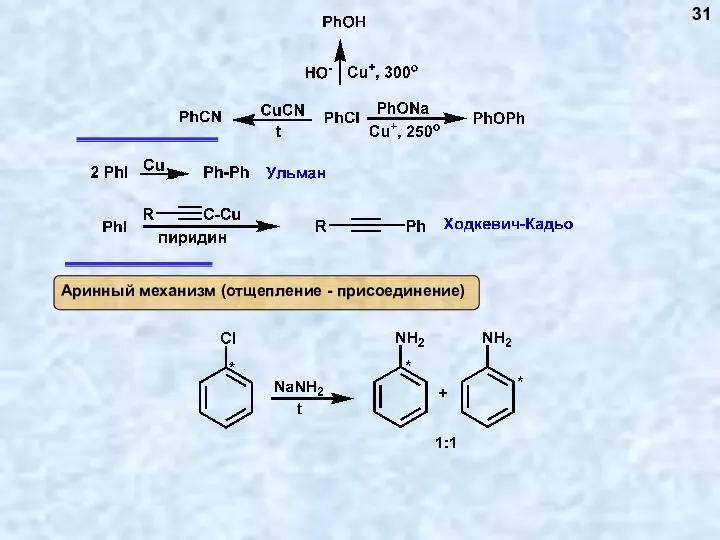
- 31. 31
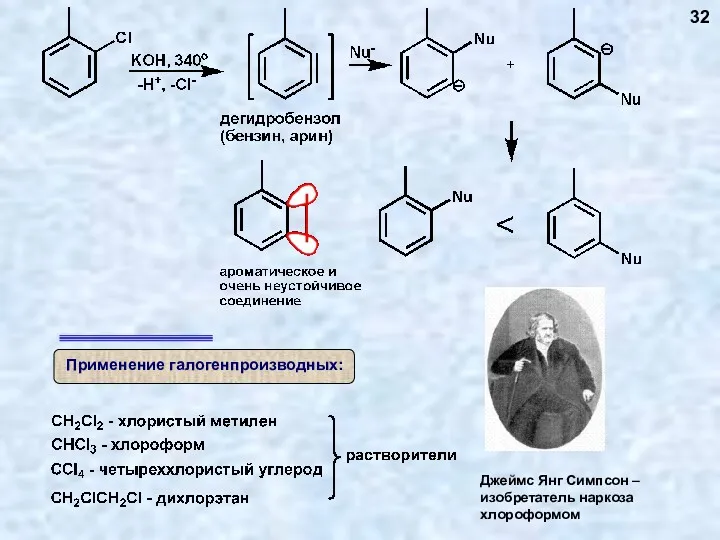
- 32. 32
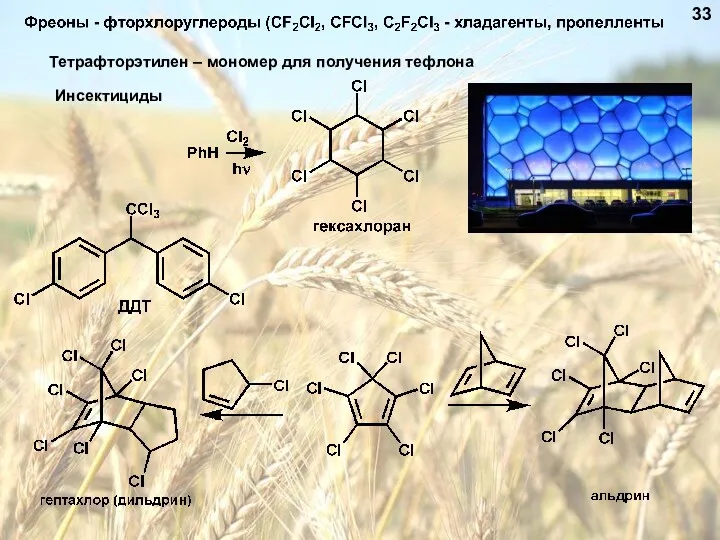
- 33. Тетрафторэтилен – мономер для получения тефлона Инсектициды 33
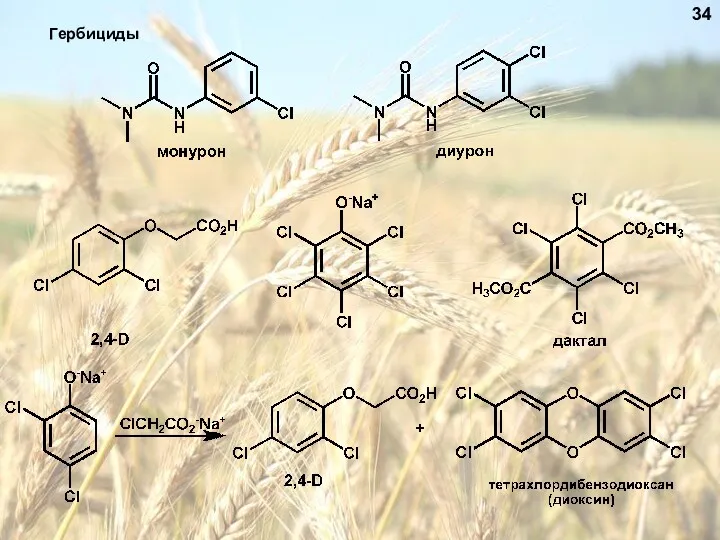
- 34. Гербициды 34
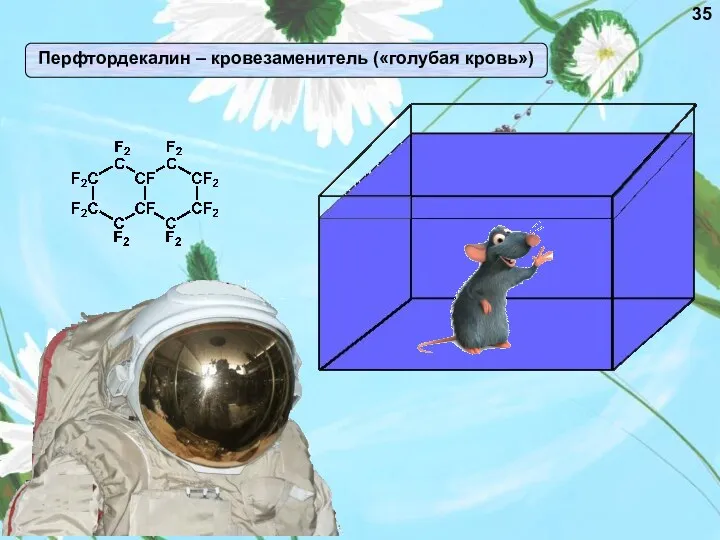
- 35. 35
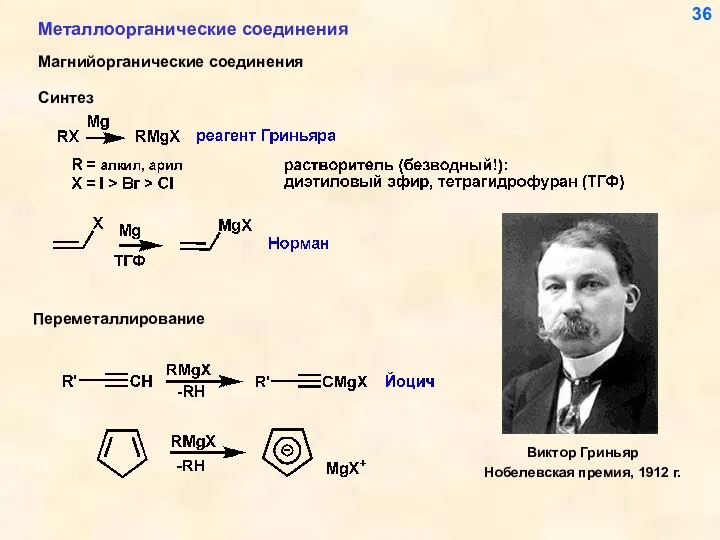
- 36. Металлоорганические соединения Магнийорганические соединения 36
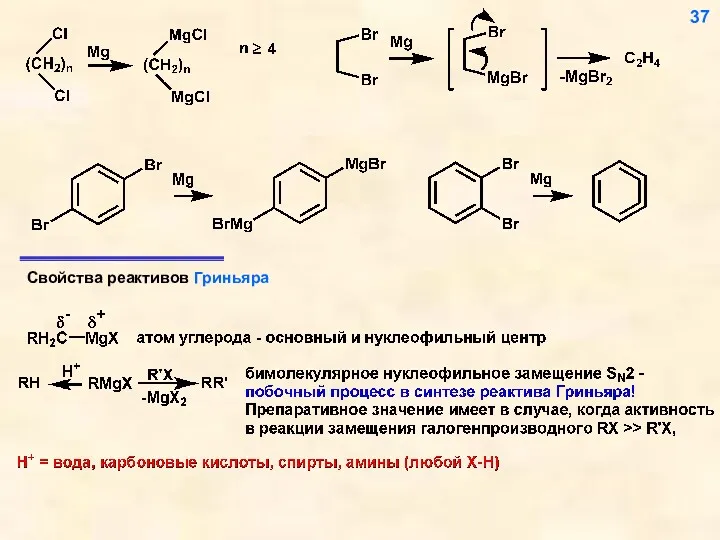
- 37. 37
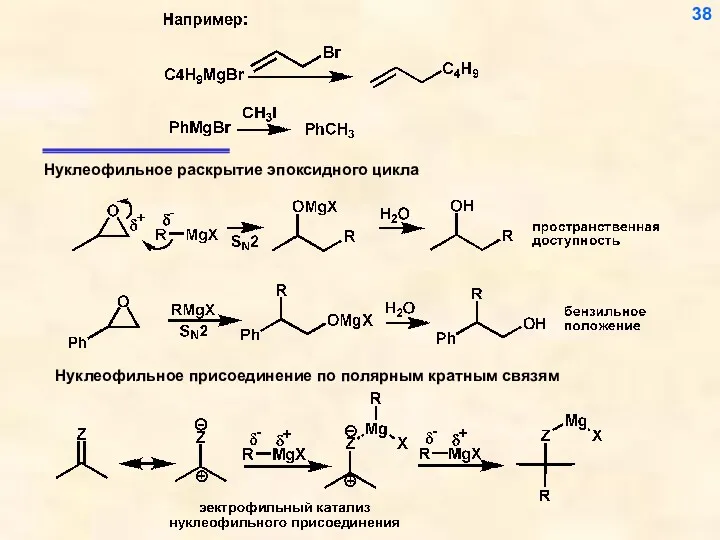
- 38. 38
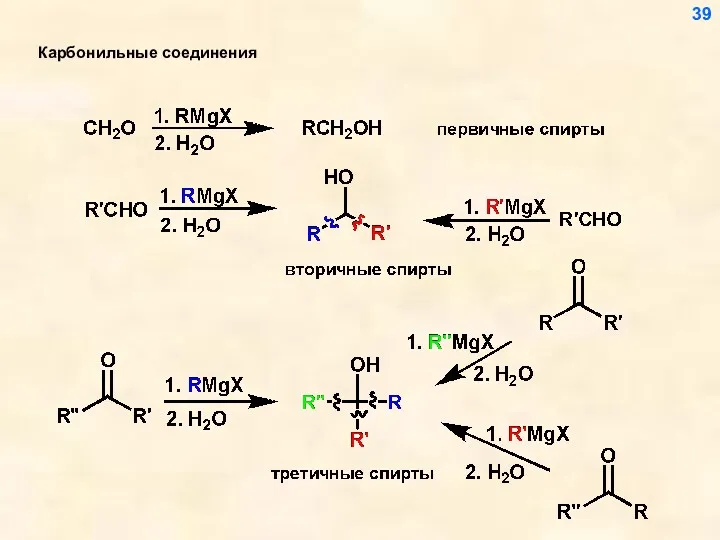
- 39. Карбонильные соединения 39
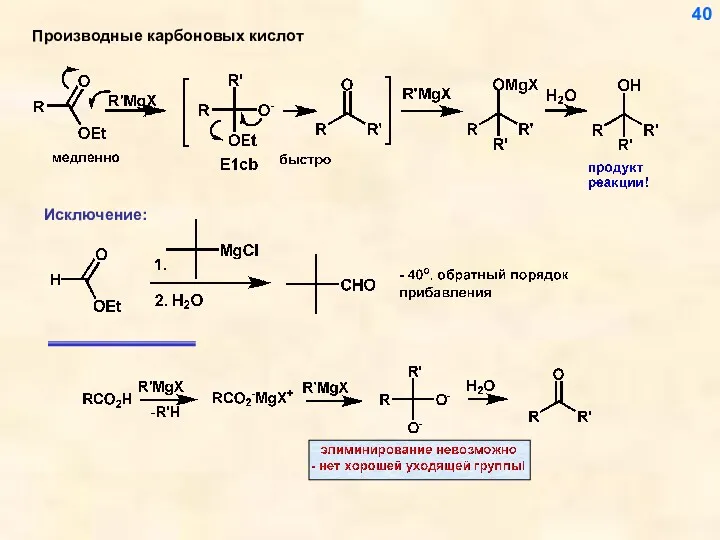
- 40. 40
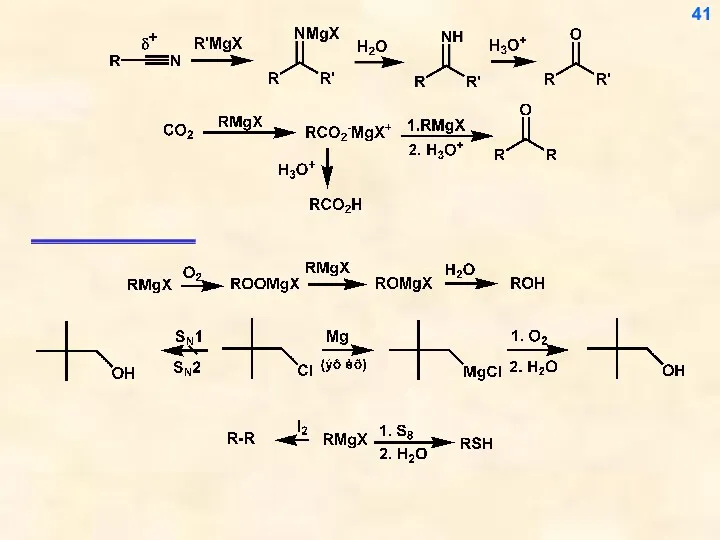
- 41. 41
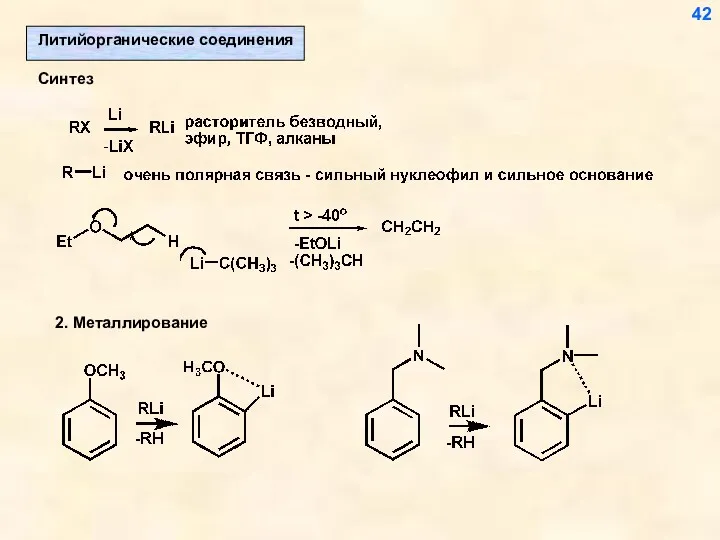
- 42. Синтез 42
- 44. Скачать презентацию

 Effect of anodizing parameters on growth of selfordering TiO2
Effect of anodizing parameters on growth of selfordering TiO2 Мұнайды өңдеудің химиялық процестерінің теориялық негіздері
Мұнайды өңдеудің химиялық процестерінің теориялық негіздері Аминокислоты
Аминокислоты Открытие Периодического закона
Открытие Периодического закона Химические свойства алкенов. Получение
Химические свойства алкенов. Получение Видалення забруднень органічного походження з поверхні тканини
Видалення забруднень органічного походження з поверхні тканини Строение атома, изотопы
Строение атома, изотопы 20230306_vodorod_ego_fizicheskie_svoystva
20230306_vodorod_ego_fizicheskie_svoystva Токсическое действие диоксинов и диоксиноподоных соединений
Токсическое действие диоксинов и диоксиноподоных соединений Analytical methods in modern research. Chromatography
Analytical methods in modern research. Chromatography Аномальные свойства воды – основа жизни на Земле
Аномальные свойства воды – основа жизни на Земле Алюміній. Загальна характеристика, властивості. Алюміній оксид, алюміній гідроксид, їх амфотерність
Алюміній. Загальна характеристика, властивості. Алюміній оксид, алюміній гідроксид, їх амфотерність Металлогеническая периодизация истории Земли. Геолого-металлогенические ранги
Металлогеническая периодизация истории Земли. Геолого-металлогенические ранги Железо, его физические и химические свойства
Железо, его физические и химические свойства Неомыляемые липиды. Изопреноиды
Неомыляемые липиды. Изопреноиды Тепловой эффект химических реакций
Тепловой эффект химических реакций Спирти. Феноли. Етери
Спирти. Феноли. Етери Химия переходных элементов IV – V группы
Химия переходных элементов IV – V группы Инструментальные методы исследования органических веществ
Инструментальные методы исследования органических веществ Зародження періодичної системи елементів Менделєєва
Зародження періодичної системи елементів Менделєєва Свойства воды
Свойства воды Коллигативные свойства растворов
Коллигативные свойства растворов Валентность и степень окисления
Валентность и степень окисления Спирты, фенолы, тиолы
Спирты, фенолы, тиолы Каталитический риформинг бензинов
Каталитический риформинг бензинов Вплив хімічних сполук на довкілля
Вплив хімічних сполук на довкілля Понятия про синтетические лекарственные средства
Понятия про синтетические лекарственные средства Волшебница - вода
Волшебница - вода