Слайд 2

Цели урока
Сформировать представления о металлах как восстановителях
Выяснить причину разной активности металлов
Выделить
основные свойства металлов
Слайд 3

Слайд 4

Слайд 5

Слайд 6

Слайд 7

Ме - восстановители
Атомы Ме имеют сравнительно большие радиусы.
⇨ ē
значительно удалены от ядра и слабо с ним связаны
У наиболее активных Ме на внешнем энергетическом уровне находятся 1-3 ē.
⮋
Ме легко отдают внешние ē и являются
восстановителями
Слайд 8

1. Взаимодействие с неМе
+ О2
0 0 +1 -2
4Li + O2
= 2Li2O
4 ē
0 0 +2 -2
2Ca + O2 = 2CaO
4 ē
0 0 +2 -2
2Cu + O2 = 2CuO
4 ē
Слайд 9

1. Взаимодействие с неМе
+ Cl2
0 0 +2 -1
Cu +
Cl2 = CuCl2
2 ē
0 0 +3 -1
2Fe + 3Cl2 = 2FeCl3
6 ē
+ S
0 0 +2 -2
Cu + S = CuS
2 ē
0 0 +2 -2
Hg + S = HgS
2 ē
Слайд 10

2. Взаимодействие с водой
Щелочные и щелочноземельные Ме ?
? Щелочи
0 +1
+1 0
2Na + 2H2O = 2NaOH + H2↑
2 ē
Менее активные Ме (раскаленные) ? оксид
3Fe + 4H2O = Fe3O4 + 4H2↑
Ag, Au, Pt, Hg, Cu с водой не взаимодействуют
Слайд 11

Бекетов
Николай Николаевич
Слайд 12

3. Взаимодействие с кислотами
0 +1 +2 0
Mg + H2SO4 =
MgSO4 + H2↑
2 ē
0 +1 +2 0
Zn + H2SO4 = ZnSO4 + H2↑
2 ē
Cu + H2SO4 =
Вывод: Ме, стоящие в ряду напряжений левее водорода, вытесняют его из растворов кислот, а стоящие правее – не вытесняют водород из растворов кислот
Слайд 13

Исключения
H2SO4 (конц.) и HNO3 (любой конц-ии) реагируют с металлами по-особому, при
этом Н2 не образуется
Слайд 14

4. Взаимодействие с солями
0 +2 +2 0
Zn + CuSO4 =
ZnSO4 + Cu
2 ē
Cu + ZnSO4 =
Вывод: Каждый металл вытесняет из растворов солей другие металлы, находящиеся правее него в ряду напряжений, и сам может быть вытеснен металлами, расположенными левее
Слайд 15

Упражнение 1
Расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
а) Al
+ O2 = Al2O3
б) Zn + S =ZnS
Слайд 16

Ответы
0 0 +3 -2
а) 4Al + 3O2 = 2Al2O3
в-ль
о-ль
Al0 - 3ē → Al+3 4 окисление
O20 + 4ē → 2O-2 3 восстановление
0 0 +2 -2
б) Zn + S =ZnS
в-ль о-ль
Zn0 - 2ē → Zn+2 2 1 окисление
S0 + 2ē → S-2 2 1 восстановление
Слайд 17

Упражнение 2
Допишите практически осуществимые реакции:
а) Fe + HCl →
б) Ag +
H3PO4 →
в) Al + HCl →
г) Zn + Pb(NO3)2 →
д) Fe + MgCl2 →
Слайд 18

Ответы
а) 2Fe + 6HCl → 2FeCl3 + 3H2↑
б) Ag + H3PO4
→
в) 2Al + 3H2SO4 → Al2(SO4)3 + 3H2↑
г) Zn + Pb(NO3)2 → Zn(NO3)2 + Pb
д) Fe + MgCl2 →
Слайд 19

Домашнее задание
Выучить общие химические свойства металлов.
Задача. Смесь медных и магниевых опилок
массой 1,5 г обработали избытком соляной кислоты. В результате выделился газ объемом 560 мл (н.у.). Определите массовую долю меди в смеси.


















 Месторождения берилла и топаза
Месторождения берилла и топаза Химический эквивалент. Формульные единицы
Химический эквивалент. Формульные единицы Metode electrochimice. Generalităţi
Metode electrochimice. Generalităţi Соединения железа
Соединения железа Соединения кальция. Жесткость воды и способы её устранения
Соединения кальция. Жесткость воды и способы её устранения Электролитическая диссоциация. 9 класс
Электролитическая диссоциация. 9 класс Методика преподавания химии
Методика преподавания химии Высшие жирные кислоты. Липиды
Высшие жирные кислоты. Липиды Электронные конфигурации атомов
Электронные конфигурации атомов Метод молекулярных орбиталей
Метод молекулярных орбиталей Натуральные, искуственные и синтетические материалы
Натуральные, искуственные и синтетические материалы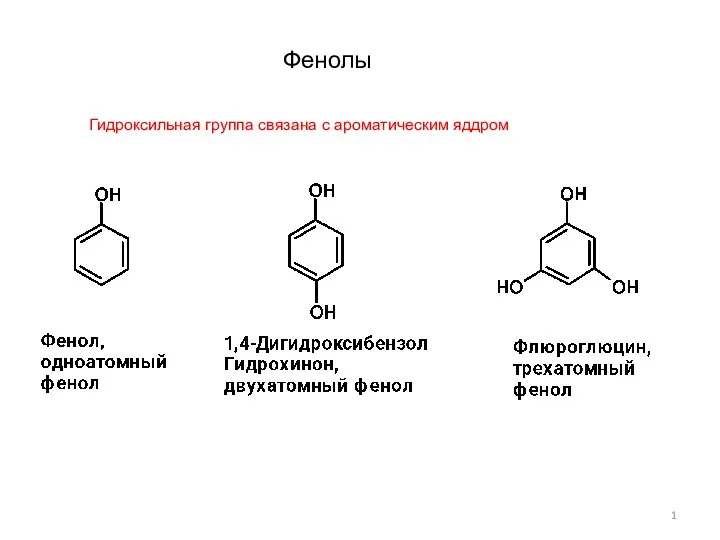 Фенолы-1
Фенолы-1 Группа веществ, изолируемых из биологического материала дистилляцией
Группа веществ, изолируемых из биологического материала дистилляцией Введение. Предмет и содержание фармацевтической химии, её связи с другими науками
Введение. Предмет и содержание фармацевтической химии, её связи с другими науками Естери. Класифікація та номенклатура естерів
Естери. Класифікація та номенклатура естерів Электронное строение элементов главной подгруппы III группы
Электронное строение элементов главной подгруппы III группы Сложные эфиры
Сложные эфиры Основні класи неорганічних сполук
Основні класи неорганічних сполук Насичені одноатомні спирти, їх фізичні та хімічні властивості. Одержання етанолу
Насичені одноатомні спирти, їх фізичні та хімічні властивості. Одержання етанолу Производство полимеров
Производство полимеров Элементтер-органогендер. өмір металдары. Көміртек – органикалық қосылыстардың негізін құраушы
Элементтер-органогендер. өмір металдары. Көміртек – органикалық қосылыстардың негізін құраушы Гетероциклические соединения
Гетероциклические соединения Свойства воды. Оценка качества
Свойства воды. Оценка качества Відносна молекулярна маса речовини, її обчислення за хімічною формулою
Відносна молекулярна маса речовини, її обчислення за хімічною формулою ОВР – окислительно-восстановительные реакции. Тема 4
ОВР – окислительно-восстановительные реакции. Тема 4 Solutions and solubilities
Solutions and solubilities Аминокислоты. Пептиды. Белки
Аминокислоты. Пептиды. Белки Генетическая связь между основными классами неорганических веществ
Генетическая связь между основными классами неорганических веществ