Содержание
- 2. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев
- 3. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев ТОРИЙ Открыт в 1828 г. Берцелиусом. Стабильных изотопов не имеет. Известно
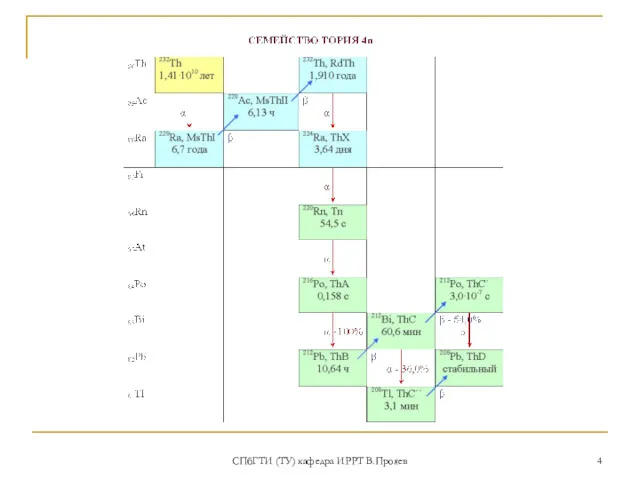
- 4. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев
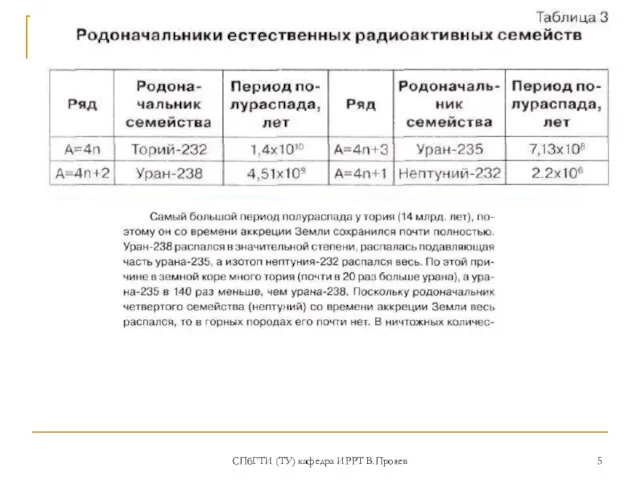
- 5. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев
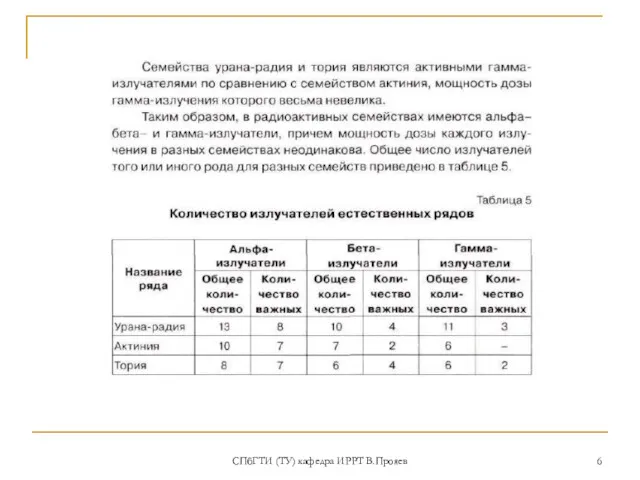
- 6. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев
- 7. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев
- 8. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев ОБЩАЯ характеристика химических свойств тория Конфигурация внешних. электронных оболочек атома тория
- 9. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев
- 10. НРБ 99/2009 5.3.4. Эффективная удельная активность (Аэфф) природных радионуклидов в строительных материалах (щебень, гравий, песок, бутовый
- 11. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев СВОЙСТВА металлического тория Торий—металл серебристого цвета, легко подвергающийся механической обработке. Порошкообразный
- 12. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев
- 13. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев ОКИСЛЫ тория. Торий в растворе Главный оксид – диоксид тория ThO2.
- 14. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев
- 15. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев НЕРАСТВОРИМЫЕ соединения тория (1)
- 16. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев НЕРАСТВОРИМЫЕ соединения тория (2) гидроокись тория Th(OH)xAya- (x+ay=4), начинает осаждаться при
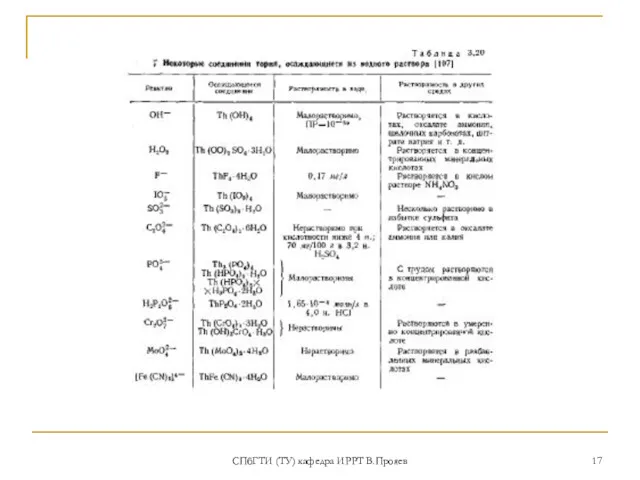
- 17. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев
- 18. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев НЕРАСТВОРИМЫЕ соединения тория (3) фторид тория ThF4 4H2O, гексафториат калия К2ThF6.
- 19. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев РАСТВОРИМЫЕ соединения тория РАСТВОРИМЫЕ СОЕДИНЕНИЯ: перхлораты, хлориды, нитраты, сульфаты, хлораты, броматы.
- 20. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев МЕТОДЫ определения тория Используются гравиметрические, объемные, колориметрические и радиометрические методы. Стандартным
- 21. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев ПРИМЕНЕНИЕ тория 1. Торий как потенциальное ядерное горючее - ТОРИЕВЫЙ ТОПЛИВНЫЙ
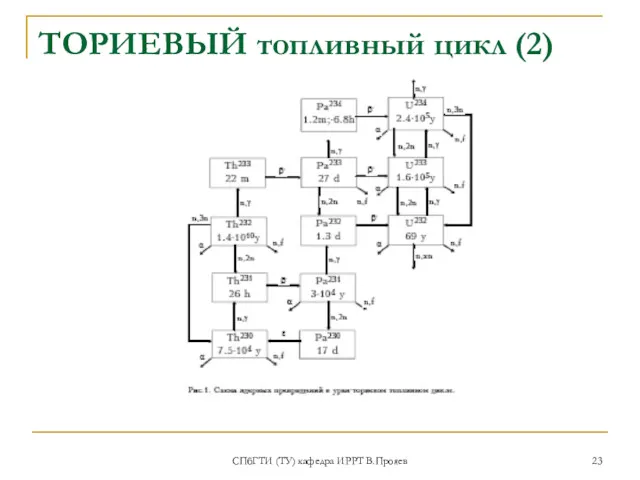
- 22. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев ТОРИЕВЫЙ топливный цикл (1) Интерес к торию, как топливу для ядерных
- 23. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев ТОРИЕВЫЙ топливный цикл (2)
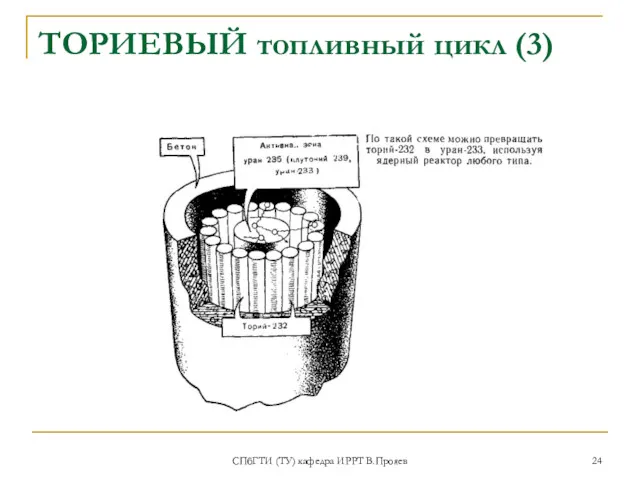
- 24. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев ТОРИЕВЫЙ топливный цикл (3)
- 25. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев ТОРИЕВЫЙ топливный цикл (4) преимущества отработавшие твэлы не нуждаются в радиохимической
- 26. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев
- 27. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев ТОРИЕВЫЙ топливный цикл (4) недостатки ториевый цикл, в целом, дороже уранового.
- 28. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев ПРОТАКТИНИЙ (1/2) 1.Ра – один из немногих элементов, существование которых предсказано
- 29. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев ПРОТАКТИНИЙ (2/2) 4.Ра – один из немногих элементов, которые пока намного
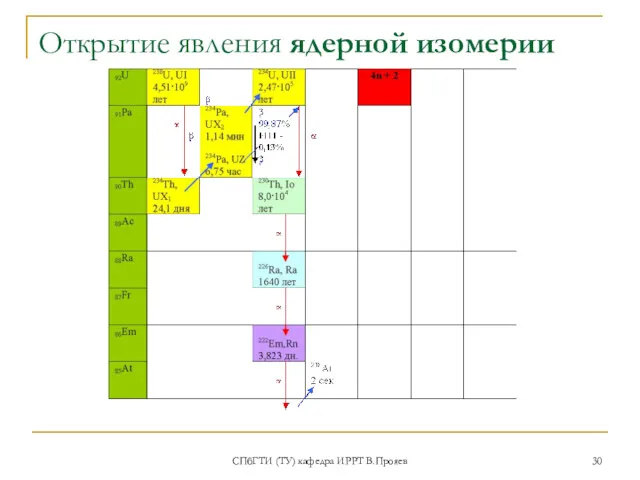
- 30. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев Открытие явления ядерной изомерии
- 31. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев
- 32. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев Радиоактивные свойства некоторых изотопов протактиния:
- 33. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев ОБЩАЯ характеристика химических свойств протактиния Конфигурация внешних электронных оболочек атома 5s25p65d105f26s26p66d17s2,
- 34. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев Двойственность химических свойств Pa С одной стороны Ра, является аналогом Nb
- 35. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев СВОЙСТВА металлического протактиния Протактиний — блестящий металл светло-серого цвета, покрывающийся на
- 36. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев
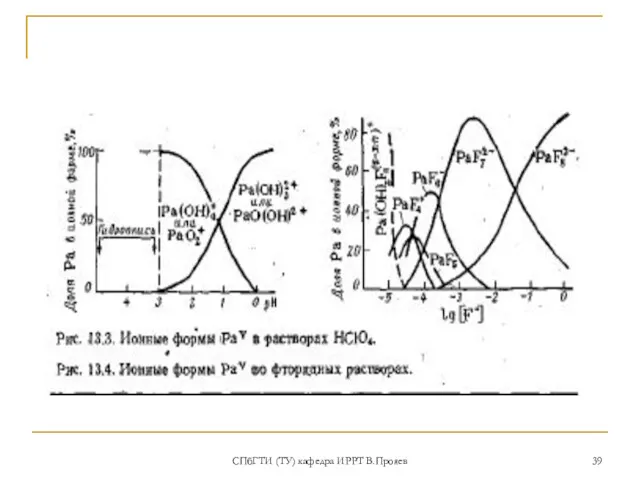
- 37. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев Ра в степени окисления +5 (1) Получено большое число различных соединений
- 38. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев Ра в степени окисления +5 (2) Принято считать, что линейные диоксикатионы
- 39. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев
- 40. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев Ра в степени окисления +4 Протактиний в степени окисления +4 относительно
- 41. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев Ра в степени окисления +4 Ра (IV) менее склонен к гидролизу,
- 42. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев МЕТОДЫ выделения протактиния Основными методами выделения протактиния являются: соосаждение, экстракция и
- 43. СПбГТИ (ТУ) кафедра ИРРТ В.Прояев МЕТОДЫ определения протактиния Применение протактиния Наиболее простым методом количественного определения протактиния
- 45. Скачать презентацию


































 Соединения химических элементов. 8 класс
Соединения химических элементов. 8 класс Обчислення за хімічними рівняннями відносного виходу продукту реакції
Обчислення за хімічними рівняннями відносного виходу продукту реакції Галогены. Положение в периодической системе. Химические свойства
Галогены. Положение в периодической системе. Химические свойства Аммиак. Физические и химические свойства. Получение, применение
Аммиак. Физические и химические свойства. Получение, применение Комплексні сполуки. Комплексоутворення в біологічних системах
Комплексні сполуки. Комплексоутворення в біологічних системах Химические свойства солей
Химические свойства солей Уравнения химических реакций. Алгоритм расстановки коэффициентов
Уравнения химических реакций. Алгоритм расстановки коэффициентов Зелёные камни
Зелёные камни Вчення про розчини. Рівновага в розчинах електролітів
Вчення про розчини. Рівновага в розчинах електролітів Гидролиз солей (11 класс)
Гидролиз солей (11 класс) Технология переработки полимеров
Технология переработки полимеров Карбоновые кислоты. Свойства карбоновых кислот
Карбоновые кислоты. Свойства карбоновых кислот Спирты (алканолы)
Спирты (алканолы) 5511c750430548bfa1da4ba840324bb2
5511c750430548bfa1da4ba840324bb2 Introduction to Periodic Table
Introduction to Periodic Table Ауыр металлдар
Ауыр металлдар Розв’язування розрахункових хімічних задач. Методичні рекомендації для вчителів хімії та школярів
Розв’язування розрахункових хімічних задач. Методичні рекомендації для вчителів хімії та школярів Learning Objectives
Learning Objectives Предельные углеводороды
Предельные углеводороды Сучасні методи органічного синтезу. Ізогіпсичні перетворення функціональних груп. Реакції приєднання. Гідроборування
Сучасні методи органічного синтезу. Ізогіпсичні перетворення функціональних груп. Реакції приєднання. Гідроборування Элементы подгруппы углерода
Элементы подгруппы углерода Ионная связь
Ионная связь Кристаллические решетки. (8 класс)
Кристаллические решетки. (8 класс) Спирты. Понятие о спиртах
Спирты. Понятие о спиртах Химические реакции
Химические реакции Розв’язання експериментальних задач. Практична робота №2
Розв’язання експериментальних задач. Практична робота №2 Актиноиды. Физические и химические свойства
Актиноиды. Физические и химические свойства Пластмассы
Пластмассы