Содержание
- 2. План лекции: Классификация неорганических веществ. Способы получения, номенклатура, физические и химические свойства основных, кислотных и амфотерных
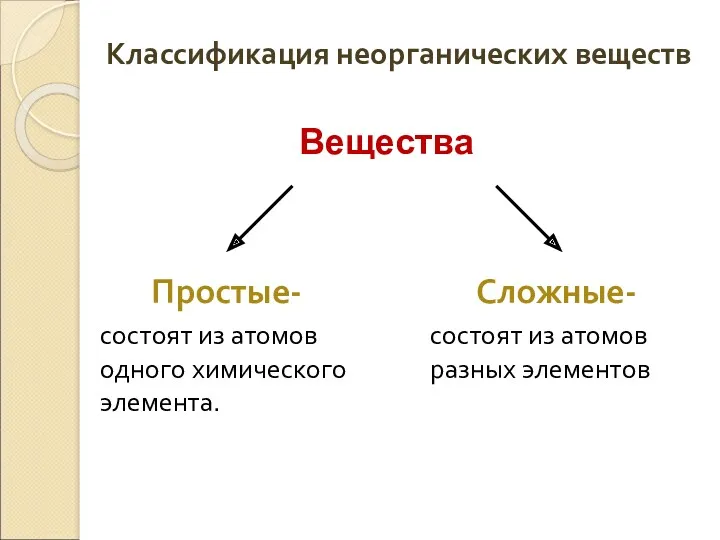
- 3. Классификация неорганических веществ Простые- состоят из атомов одного химического элемента. Сложные- состоят из атомов разных элементов
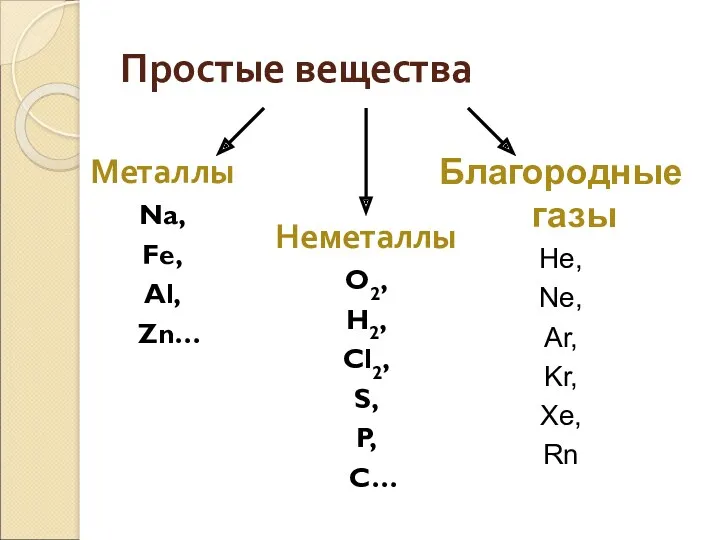
- 4. Благородные газы He, Ne, Ar, Kr, Xe, Rn Простые вещества Металлы Na, Fe, Al, Zn… Неметаллы
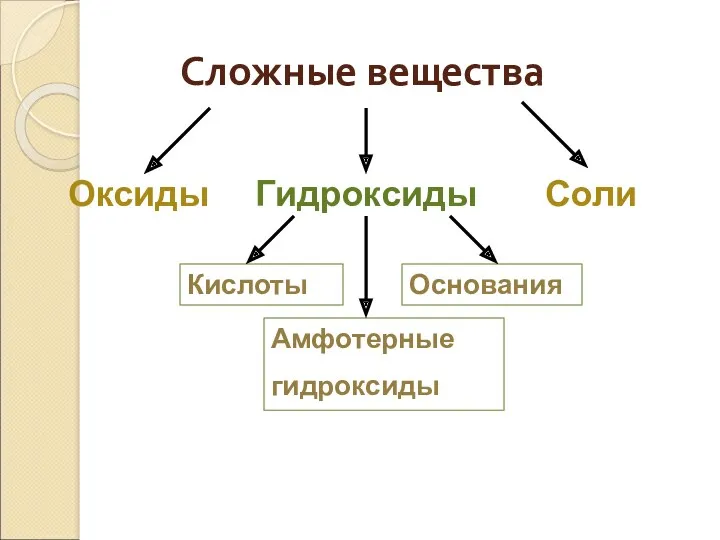
- 5. Сложные вещества Оксиды Гидроксиды Соли Кислоты Основания Амфотерные гидроксиды
- 6. Свойства оксидов и гидроксидов в периоде изменяются от основных через амфотерные к кислотным, т.к. увеличивается положительная
- 7. Оксиды Оксиды – это сложные вещества, состоящие из двух химических элементов, один из которых – кислород
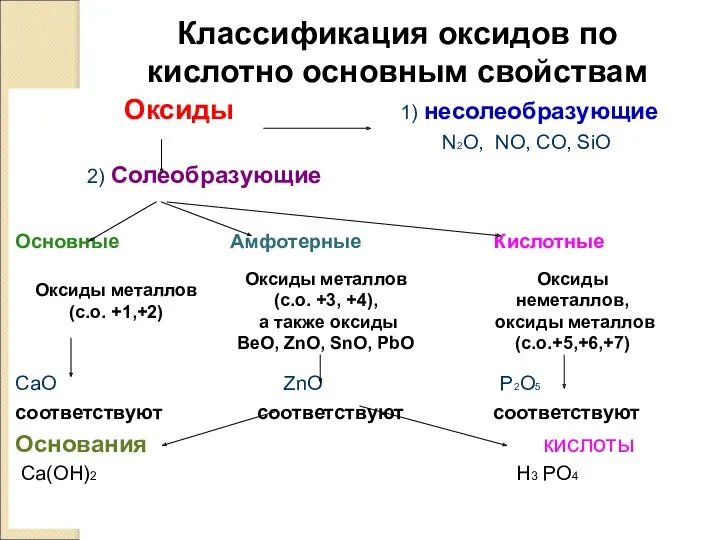
- 8. Классификация оксидов по кислотно основным свойствам Оксиды 1) несолеобразующие N2O, NO, CO, SiO 2) Солеобразующие Основные
- 9. Несолеобразующие оксиды — оксиды, не проявляющие ни кислотных, ни основных, ни амфотерных свойств и не образующие
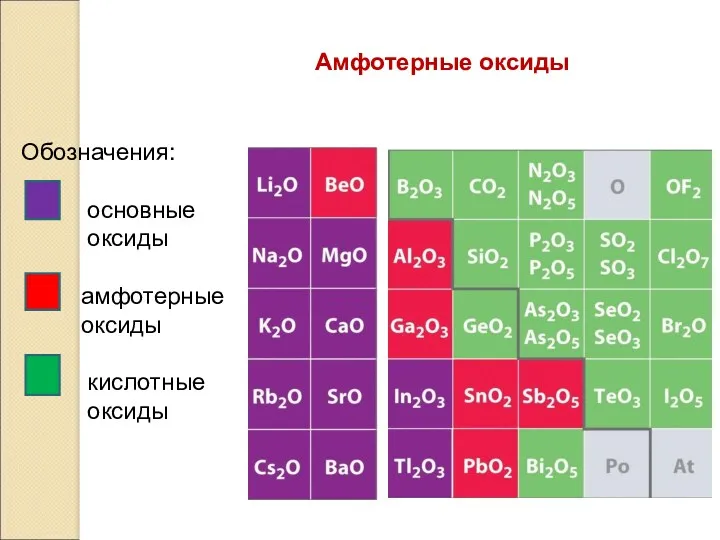
- 10. Амфотерные оксиды Амфотерными называются оксиды, которые в зависимости от условий проявляют основные или кислотные свойства. Примеры:
- 11. Al2O3 (оксид алюминия) очень твердые прозрачные кристаллы. Температура плавления – 2053 °C, температура кипения – 3000
- 12. Какие элементы периодической системы образуют амфотерные соединения? Металлы Неметаллы, исключая элементы побочных подгрупп Элементы, образующие амфотерные
- 13. Амфотерные оксиды Обозначения: основные оксиды амфотерные оксиды кислотные оксиды
- 14. Гидроксиды Гидроксиды – это неорганические соединения, содержащие в составе гидроксильную группу (-ОН ) Общая формула: Э(ОН)n
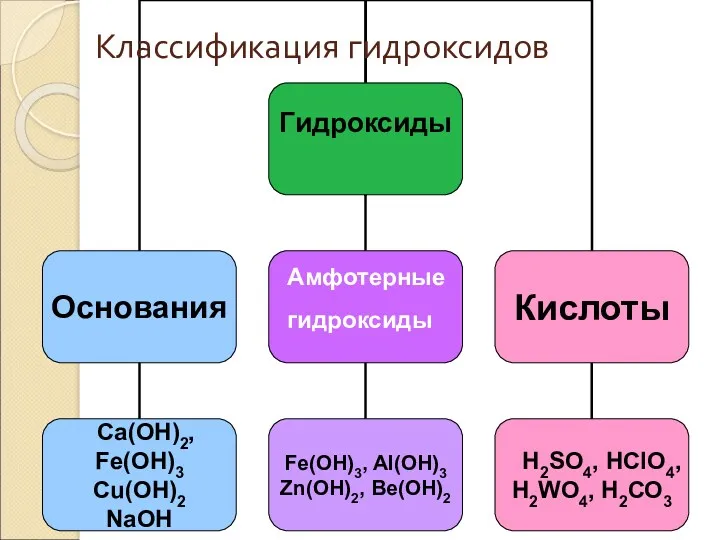
- 15. Амфотерные гидроксиды Классификация гидроксидов
- 16. Основания Основания – это сложные вещества, состоящие из ионов металлов и связанных с ними одного или
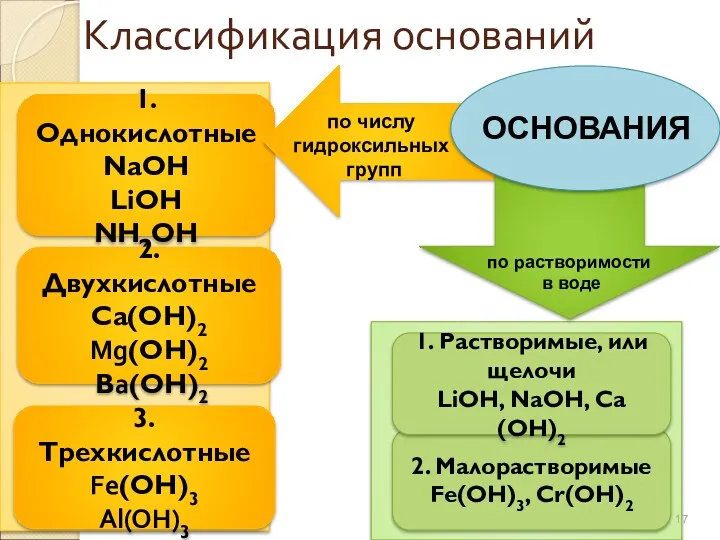
- 17. Классификация оснований 1. Однокислотные NaОН LiОН NН4ОН 2. Двухкислотные Са(ОН)2 Mg(ОН)2 Вa(ОН)2 3. Трехкислотные Fe(ОН)3 Al(OH)3
- 18. Кислоты Кислоты – это сложные вещества, молекулы которых состоят из атомов водорода и кислотных остатков.
- 19. Классификация кислот
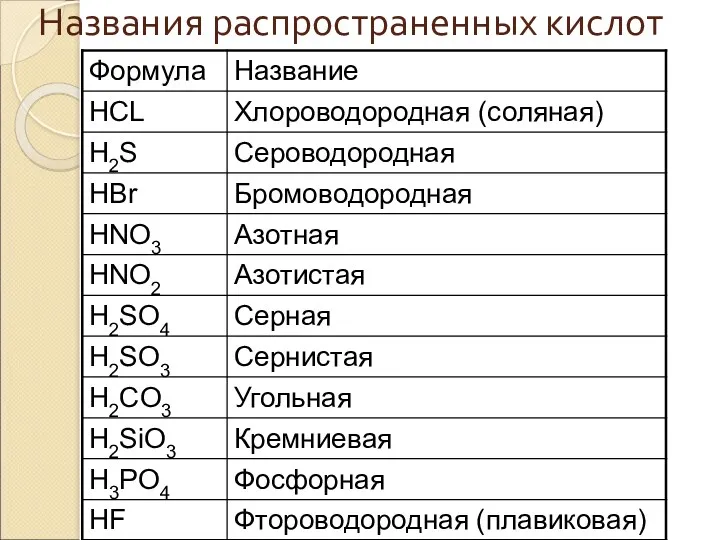
- 20. Названия распространенных кислот
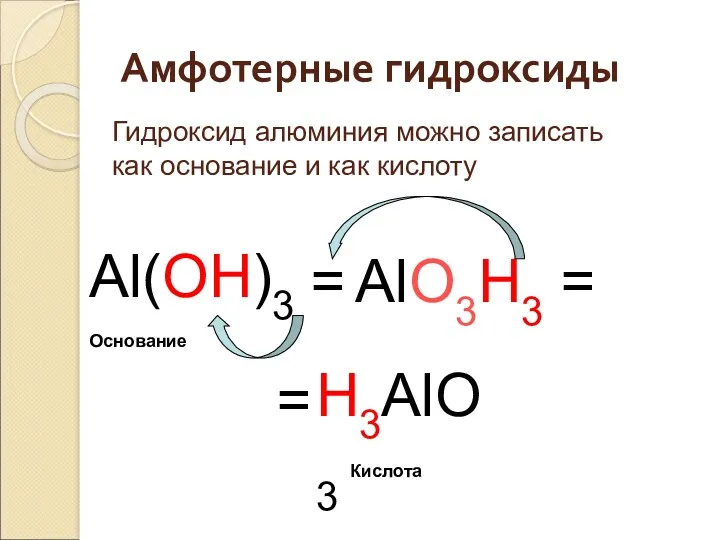
- 21. Амфотерными называются гидроксиды , которые в зависимости от условий могут быть как донорами катионов водорода и
- 22. Амфотерные гидроксиды Al(OH)3 = H3AlO3 AlO3H3 = = Кислота Основание Гидроксид алюминия можно записать как основание
- 23. Некоторые гидроксиды с кислотно-основными свойствами:
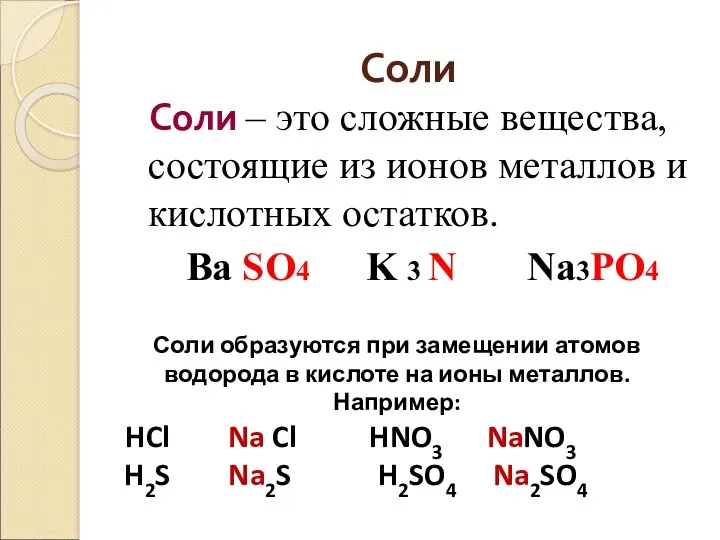
- 24. Соли Соли – это сложные вещества, состоящие из ионов металлов и кислотных остатков. Ba SO4 K
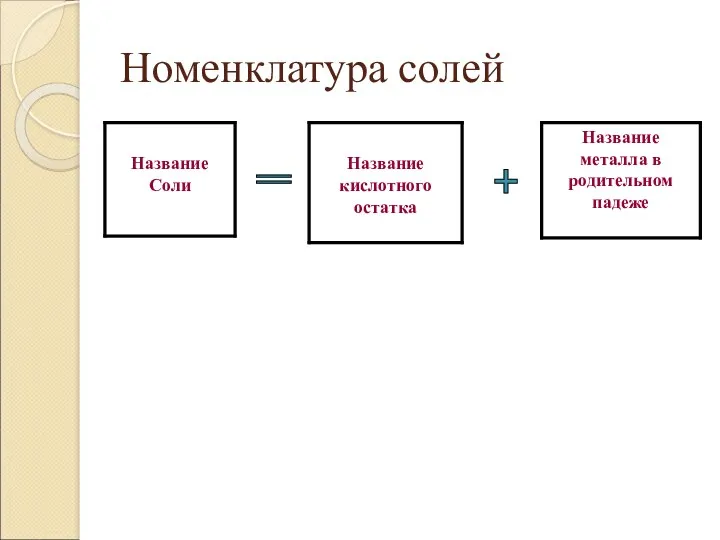
- 25. Номенклатура солей + =
- 26. Названия солей бескислородных кислот называем неметалл ( латинское название) с суффиксом – ид (в им. падеже);
- 27. Названия солей кислородсодержащих кислот Называем ион кислотного остатка (в именительном падеже); с суффиксами: -ат для высшей
- 28. Номенклатура солей F – Cl – Br – I – S 2- SO3 2- SO4 2-
- 29. Алгоритм составления формулы соли бескислородной кислоты Первое действие: записываем степени окисления элементов, находим наименьшее общее кратное
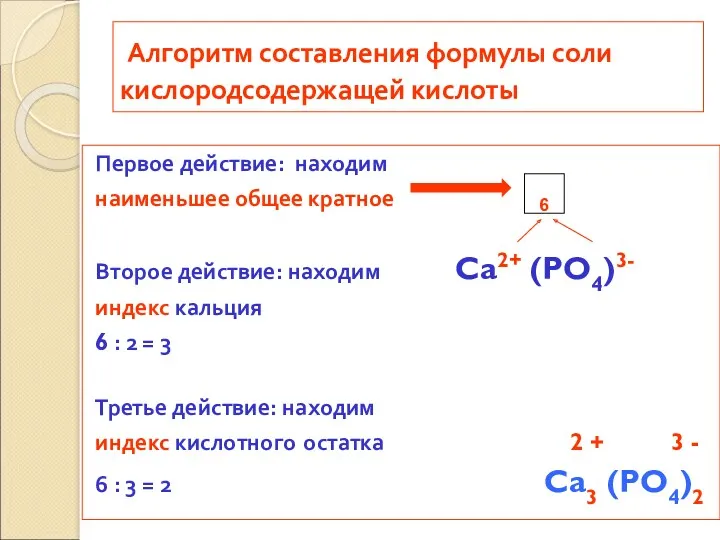
- 30. Алгоритм составления формулы соли кислородсодержащей кислоты Первое действие: находим наименьшее общее кратное Второе действие: находим Ca2+
- 31. Типы солей Нормальные (средние) -это соли, в которых все атомы водорода соответствующей кислоты замещены на атомы
- 32. Бытовые (тривиальные) названия некоторых солей
- 33. Генетическая связь Связь между классами неорганических соединений, основанная на получении веществ одного класса из веществ другого
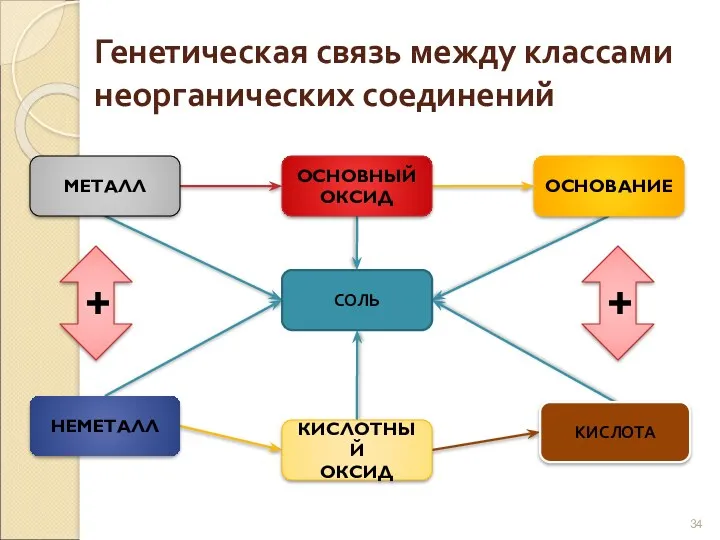
- 34. Генетическая связь между классами неорганических соединений МЕТАЛЛ ОСНОВНЫЙ ОКСИД ОСНОВАНИЕ СОЛЬ НЕМЕТАЛЛ КИСЛОТНЫЙ ОКСИД КИСЛОТА +
- 35. Генетическая связь отражается в генетических рядах. В состав любого генетического ряда входят вещества различных классов неорганических
- 37. Скачать презентацию





















 Кислородсодержащие соединения серы
Кислородсодержащие соединения серы Химическая связь
Химическая связь Взаємодія кисню із складними речовинами
Взаємодія кисню із складними речовинами Предельные одноатомные спирты
Предельные одноатомные спирты Химическая промышленность России
Химическая промышленность России Физико-химические процессы в системе свинец - сталь - кислород, для энергетических ядерных реакторов
Физико-химические процессы в системе свинец - сталь - кислород, для энергетических ядерных реакторов Откуда берутся кристаллы
Откуда берутся кристаллы Непредельные углеводороды. Алкены
Непредельные углеводороды. Алкены Выращивание кристалла медного купороса
Выращивание кристалла медного купороса Нуклеопротеины
Нуклеопротеины Введение в общеобразовательную научную дисциплину Химия
Введение в общеобразовательную научную дисциплину Химия Периодический закон и периодическая система химических элементов Д.И. Менделеева
Периодический закон и периодическая система химических элементов Д.И. Менделеева Атомный и ионный радиусы. Принципы шаровых упаковок
Атомный и ионный радиусы. Принципы шаровых упаковок Карбоновые кислоты
Карбоновые кислоты Диффузия вокруг нас
Диффузия вокруг нас Функциональные производные карбоновых кислот
Функциональные производные карбоновых кислот Валентность химических элементов (8 класс)
Валентность химических элементов (8 класс) Электроотрицательность химических элементов. Виды химической связи
Электроотрицательность химических элементов. Виды химической связи Масс-Спектроскопия
Масс-Спектроскопия Установка изомеризации пентан гексановой фракции
Установка изомеризации пентан гексановой фракции Аналітична хімія. Лекція 1
Аналітична хімія. Лекція 1 Теории кислот и оснований
Теории кислот и оснований Особенности лантаноидов и актиноидов
Особенности лантаноидов и актиноидов Правила техники безопасности. Приемы обращения с лабораторным оборудованием. Урок №2. Практическая работа №1
Правила техники безопасности. Приемы обращения с лабораторным оборудованием. Урок №2. Практическая работа №1 Окислительно-восстановительные процессы
Окислительно-восстановительные процессы Карбонильные соединения
Карбонильные соединения Химия в быту
Химия в быту Теория электролитической диссоциации
Теория электролитической диссоциации