Содержание
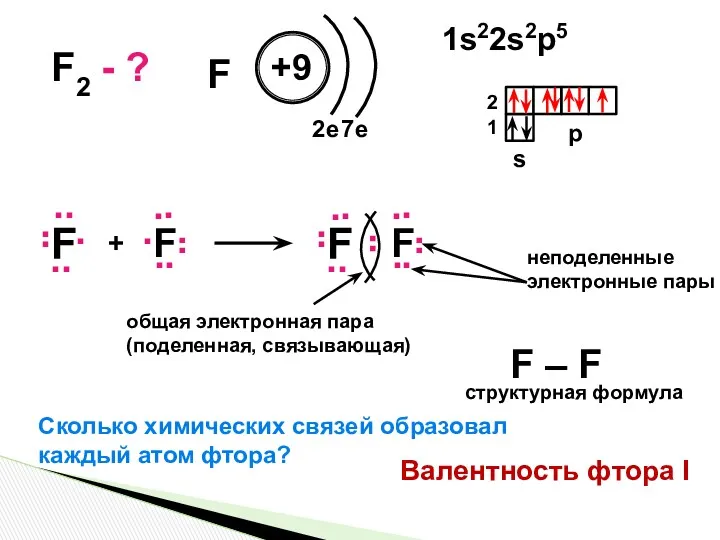
- 2. F2 - ? общая электронная пара (поделенная, связывающая) неподеленные электронные пары F – F структурная формула
- 3. Химическая связь, возникающая при образовании общих электронных пар, называется ковалентной (атомной) связью. Валентность – это число
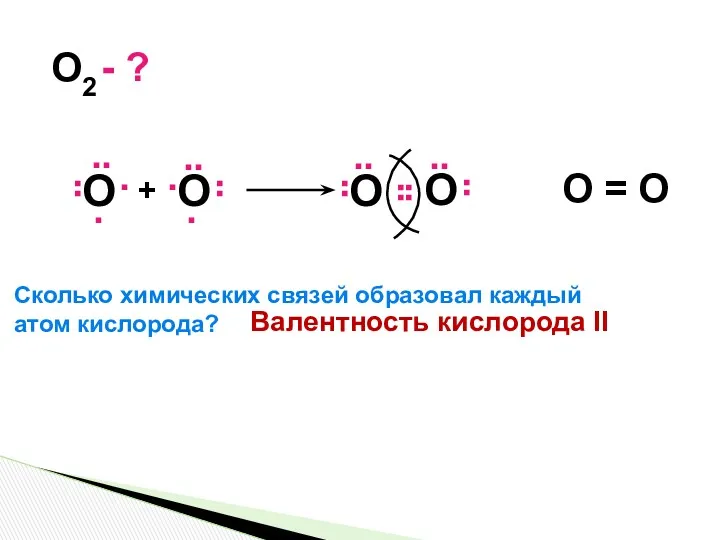
- 4. O2 - ? O O = O Сколько химических связей образовал каждый атом кислорода? Валентность кислорода
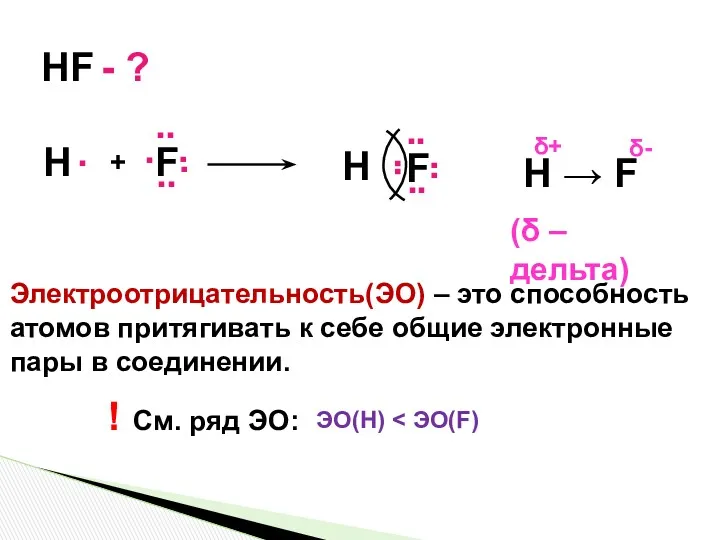
- 5. HF - ? H → F Электроотрицательность(ЭО) – это способность атомов притягивать к себе общие электронные
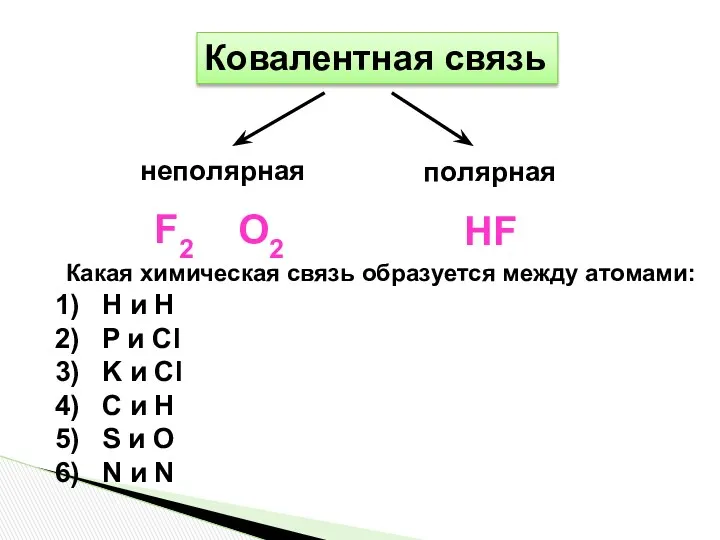
- 6. Ковалентная связь неполярная полярная O2 F2 HF Какая химическая связь образуется между атомами: H и H
- 7. Домашнее задание: § 56(до стр. 196) Стр.196 № 4 б, 3) Запишите схемы образования ковалентной связи,
- 9. Скачать презентацию


 Молекулярные свойства жидкостей
Молекулярные свойства жидкостей Р-элементы IV А группы. Углерод и кремний
Р-элементы IV А группы. Углерод и кремний Металлы и сплавы
Металлы и сплавы Реакции ионного обмена
Реакции ионного обмена Натуральный и синтетический каучуки. Резина
Натуральный и синтетический каучуки. Резина Степень окисления
Степень окисления Физические и химические явления
Физические и химические явления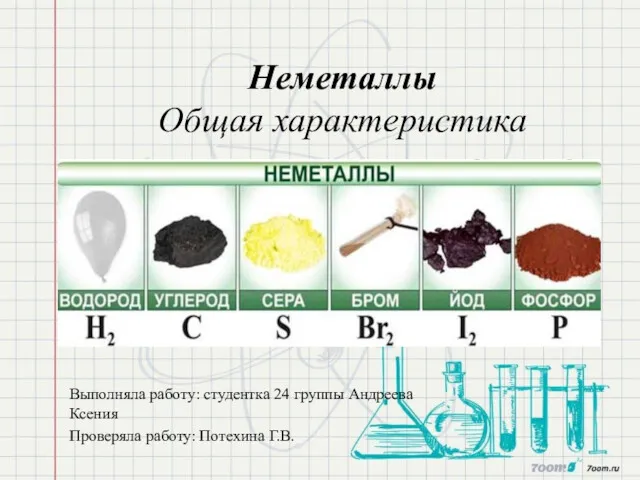 Неметаллы. Общая характеристика
Неметаллы. Общая характеристика Алкадиены: гомологический ряд, общая формула, номенклатура. Сопряжённые, изолированные, кумулированные
Алкадиены: гомологический ряд, общая формула, номенклатура. Сопряжённые, изолированные, кумулированные Изменения, происходящие с белками в процессах технологической переработки сырья
Изменения, происходящие с белками в процессах технологической переработки сырья Молекулы и атомы. Броуновское движение
Молекулы и атомы. Броуновское движение Новое направление в бизнесе компании – катализаторы синтеза метанола
Новое направление в бизнесе компании – катализаторы синтеза метанола Химическое равновесие в гомогенных системах. Ионное произведение воды. 12 класс
Химическое равновесие в гомогенных системах. Ионное произведение воды. 12 класс Химическая идентификация
Химическая идентификация Координационные соединения
Координационные соединения Цикли трикарбонових кислот
Цикли трикарбонових кислот Фазовые диаграммы
Фазовые диаграммы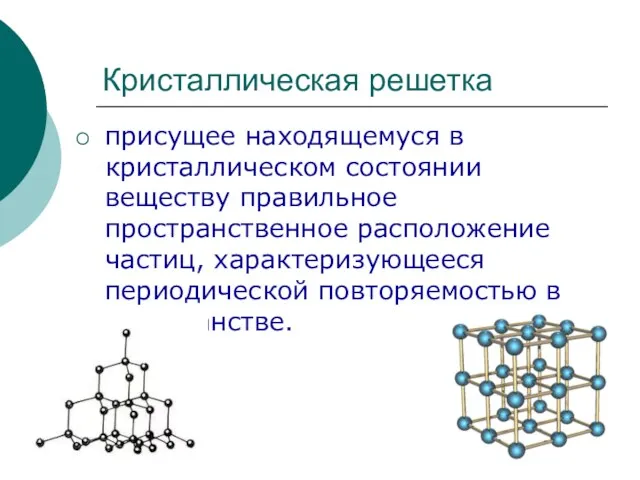 Кристаллическая решетка
Кристаллическая решетка Классификация химических элементов. Периодический закон Д.И. Менделеева
Классификация химических элементов. Периодический закон Д.И. Менделеева Соли. Определение солей
Соли. Определение солей Химические свойства оснований, кислот и солей в свете теории электролитической диссоциации
Химические свойства оснований, кислот и солей в свете теории электролитической диссоциации Введение в количественный анализ
Введение в количественный анализ Химия атмосферы. Химические процессы в тропосфере
Химия атмосферы. Химические процессы в тропосфере Основания
Основания Бериллий. Строение элемента. Физические и химические свойства. Способы получения. Применение. Интересные факты. Опыты
Бериллий. Строение элемента. Физические и химические свойства. Способы получения. Применение. Интересные факты. Опыты Промышленные типы месторождений железа
Промышленные типы месторождений железа Алюминий. 9 класс
Алюминий. 9 класс Технология производства хлорбензола
Технология производства хлорбензола