Слайд 2

Литература
Ахметов Н.С. Общая и неорганическая химия
Угай Я.А. Общая и неорганическая
химия
Зайцев О.С. Общая химия
Коровин Н.В. Общая химия
Глинка Н.Л. Общая химия
Хомченко И.Г. Общая химия
Слайд 3

Ресурсы Internet
www.xumuk.ru
www.nehudlit.ru
www.interneturok.ru
Слайд 4

Слайд 5
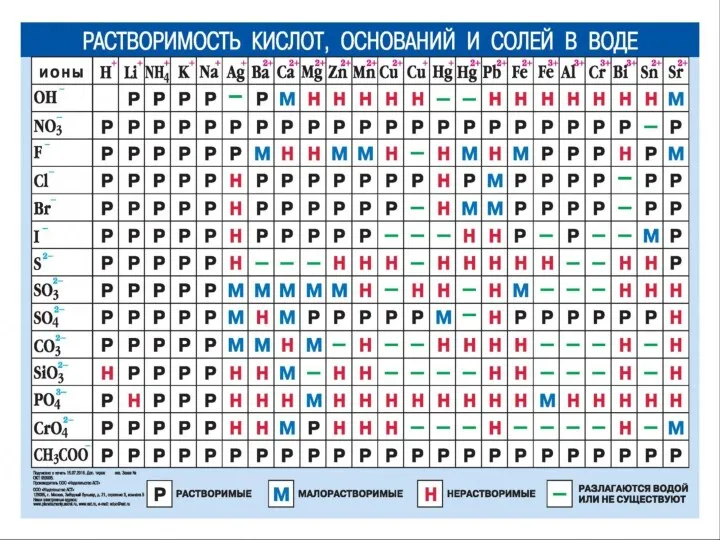
Слайд 6
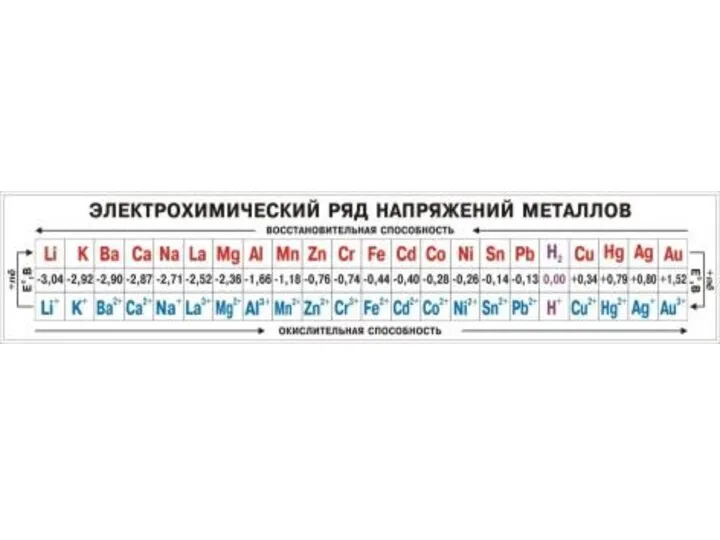
Слайд 7

Основные химические понятия и законы
Слайд 8

Слайд 9

Химия – наука о превращениях веществ, связанных с изменением электронного окружения
атомных ядер.
Вещество – это конкретный вид материи, обладающий определенными физическими и химическими свойствами, состав которого может быть выражен химической формулой.
Простое вещество состоит из атомов одного и того же химического элемента.
Химические соединения состоят из атомов нескольких элементов.
Слайд 10

Химический элемент представляет собой вид атомов с одинаковым положительным зарядом ядра.
В
настоящее время известно 117 химических элементов, из которых 92 встречаются в природе.
Атомы – мельчайшие химические частицы, являющиеся пределом химического разложения любого вещества.
Атом – это наименьшая частица химического элемента, сохраняющая все его химические свойства.
Слайд 11

Массы атомов химических элементов чрезвычайно малы: ~ 10-27 – 10-25 кг.
В химии пользуются относительными значениями масс атомов (Ar, где r – «относительный», от англ. relative).
Слайд 12

Относительная атомная масса – это масса атома, выраженная в атомных единицах
массы. За атомную единицу массы принята 1/12 часть массы атома нуклида :
1 а.е.м. =
Относительная атомная масса – величина безразмерная.
Слайд 13

Абсолютное большинство различных веществ состоит из молекул.
Молекула – наименьшая частица вещества,
способная существовать самостоятельно и сохраняющая основные химические свойства вещества.
Относительная молекулярная масса Mr вещества – это масса его молекулы, выраженная в а.е.м. (символ Mr – безразмерная величина). Например, Mr(H2SО4) = 98
Слайд 14

Единицей измерения количества вещества (n) является моль.
Моль – количество вещества, содержащее
столько структурных элементарных единиц (атомов, молекул, ионов, электронов и т.д.), сколько содержится атомов в 0,012 кг изотопа углерода 12С.
Число атомов NА в 0,012 кг углерода, или в 1 моль, легко определить следующим образом:
.
Величина NA называется постоянной Авогадро.
Слайд 15

Масса одного моля вещества называется молярной массой (символ М(В), единица –
г/моль или кг/моль). Молярная масса вещества численно равна его относительной молекулярной массе. Например. Mr(H2SО4) = 98, a M(H2SО4) = 98 г/моль.
Молярная масса вещества (М(В)), количество вещества (n(В)) и масса вещества (m(В))связаны между собой соотношением:
n = m / M
Слайд 16

Химической реакцией называется процесс превращения одних веществ в другие.
Способность вещества участвовать
в тех или иных химических реакциях характеризует его химические свойства.
Слайд 17

Слайд 18

Закон сохранения массы
масса веществ, вступающих в химическую реакцию, равна массе веществ,
образующихся в результате реакции.
Автор закона Лавуазье
Слайд 19

Закон постоянства состава
всякое чистое вещество, независимо от способа его получения, имеет
постоянный качественный и количественный состав.
Закон применим только к соединениям с молекулярной структурой.
Автор закона Ж. Л. Пруст
Слайд 20

Закон эквивалентов
Эквивалент – условная или реально существующая частица вещества в
Z раз меньшая, чем соответствующая ФЕ вещества, участвующего в конкретной реакции
Э = ФЕ / Z
где Z – эквивалентное число, которое может быть равно или больше единицы (Z ≥ 1).
Слайд 21

Закон эквивалентов
Первая формулировка закона эквивалентов: в реакции эквивалентные количества реагирующих и
образующихся веществ одинаковы.
Для реакции, записанной в общем виде
А + В + … = Д + F + ...
закон эквивалентов
nэк(А) = nэк(В) = ... = nэк(Д) = nэк(F) = ... .
Слайд 22

Вторая формулировка закона эквивалентов: массы реагирующих веществ пропорциональны молярным массам эквивалентов
этих веществ:
m(В1) / Мэк(В1) = m(В2) / Мэк(В2)
Слайд 23

Эквивалентное количество вещества (символ nэк(В), единица – моль) – физическая величина,
пропорциональная числу эквивалентов вещества Nэк(В):
n(эк) = N(эк) / N(A)
Эквивалентное количество вещества связано с количеством вещества соотношением
nэк(В) = Z⋅n(B).
Слайд 24

Масса одного моля эквивалентов вещества называется молярной массой эквивалентов этого вещества
(символ Мэк(В)), единица – г/моль или кг/моль).
Молярная масса эквивалентов вещества в Z раз меньше молярной массы этого же вещества:
Мэк(В) = М / Z
Молярная масса эквивалентов вещества Мэк(В), масса вещества m(В) и эквивалентное количество вещества nэк(В) связаны между собой соотношением:
nэк(В) = m(В) / Мэк(В)
Слайд 25

Определение Z
В кислотно-основных реакциях эквивалентное число определяют по числу замещённых ионов
водорода (для кислоты) и по числу замещенных гидроксид-ионов (для основания) из расчета на одну ФЕ. Эквивалентное число для иона водорода (Н+ и гидроксид-иона (ОН–) равно единице (Z(Н+) = 1 и Z(OH–)= 1).
H3PО4 + NaOH = NaH2PO4 + H2О; Z(NaOH) = 1, Z(H3PО4) = 1
H3PО4 + 2 NaOH = Na2HPO4 + 2 H2О; Z(NaOH) = 1, Z(H3PО4) = 2
H3PО4 + 3 NaOH = Na3PO4 + 3 H2О. Z(NaOH) = 1, Z(H3PО4) = 3
Слайд 26

Определение Z
В окислительно-восстановительных реакциях эквивалентное число для восстановителя определяют по
числу отданных электронов, а для окислителя – по числу принятых электронов. Расчет ведется на одну ФЕ.
2 Н2 + О2 = 2 Н2О.
Н2 – 2 е → 2Н+; Z(H2) = 2;
О2 + 4е → 2О2–. Z(О2) = 4,
Слайд 27

Закон объёмных отношений
(Гей–Люссака): при неизменных температуре и давлении объемы вступающих в
реакцию газов относятся друг к другу, а также к объемам образующихся газообразных продуктов как небольшие целые числа.
Слайд 28

Газовые законы
Закон Авогадро: в равных объемах любых газов при одинаковых условиях
(Т, р) содержится равное количество молекул.
Слайд 29

Следствия из закона Авогадро
При одинаковых условиях 1 моль любого газа
занимает одинаковый объем.
При н.у. 1 моль различных газов занимает объем 22,4 л (молярный объем газа, л/моль).
Отношение масс равных объемов различных газов равно отношению их молекулярных масс:
Слайд 30

Следствия из закона Авогадро
где m1 и m2 – массы, а и
– молекулярные массы первого и второго газов.
относительная плотность первого газа по второму.
Слайд 31

Объединенный газовый закон
р0 = 101325 Па = 760 мм рт. ст.
= 1 атм.,
Т0 = 0 ºС (273,15 К),
где р0, V0, Т0 – соответственно давление, объем, температура при н.у.; р, V, Т – те же параметры данного количества газообразного вещества при других условиях.
Слайд 32

Объединенный газовый закон
Для 1 моль любого газа при н.у.:
R =
8,314 Дж/(моль⋅К)
Для 1 моля газа уравнение состояния идеального газа
уравнение Менделеева – Клайперона
Слайд 33

Закон парциальных давлений
общее давление смеси газов, химически не взаимодействующих друг
с другом, равно сумме парциальных давлений газов, составляющих смесь:
где р – общее давление; р1, р2 … - парциальные давления газов 1, 2 …
Парциальное давление газа в смеси – давление, которое производило бы это же количество данного газа, если бы он один занимал при этой же температуре весь объем, занимаемый смесью.
Автор закона Дальтон
































 Rates of reaction
Rates of reaction Пластмассалар, пластикалық материалдар
Пластмассалар, пластикалық материалдар Бензины. Основные требования к свойствам бензинов. Автомобильные, Авиационные бензины. Антидетонационные присадки
Бензины. Основные требования к свойствам бензинов. Автомобильные, Авиационные бензины. Антидетонационные присадки Азот. Аммиак (9 класс)
Азот. Аммиак (9 класс) Розрахункові задачі. Обчислення за хімічними рівняннями. Відносного виходу продукту реакції
Розрахункові задачі. Обчислення за хімічними рівняннями. Відносного виходу продукту реакції Оксиген. Кисень, склад молекули, поширеність у природі. Фізичні властивості кисню
Оксиген. Кисень, склад молекули, поширеність у природі. Фізичні властивості кисню osobennosti_i_klassifikatsiya_khimicheskikh_reaktsiy_v_organicheskoy_khimii
osobennosti_i_klassifikatsiya_khimicheskikh_reaktsiy_v_organicheskoy_khimii Ароматические соединения
Ароматические соединения Строение электронных оболочек атомов химических элементов 8 класс
Строение электронных оболочек атомов химических элементов 8 класс Относительная атомная и молекулярная массы
Относительная атомная и молекулярная массы Кислоты. Состав, названия и определение кислот
Кислоты. Состав, названия и определение кислот Introduction to Periodic Table
Introduction to Periodic Table Алкилсульфонаттарды алу және технологиялық сызбанұсқасы
Алкилсульфонаттарды алу және технологиялық сызбанұсқасы Окисно-відновні реакції. 9 клас
Окисно-відновні реакції. 9 клас Етери та естери
Етери та естери Воздушные вяжущие вещества. Гипсоангидритовые вяжущие вещества. Основы процессов схватывания и твердения. (Лекция 1)
Воздушные вяжущие вещества. Гипсоангидритовые вяжущие вещества. Основы процессов схватывания и твердения. (Лекция 1) Ароматические углеводороды (арены)
Ароматические углеводороды (арены) Вуглеводи. Класифікація вуглеводів
Вуглеводи. Класифікація вуглеводів Синтетические моющие средства, порошки, омыление, выпадение в осадок мыла, жиров
Синтетические моющие средства, порошки, омыление, выпадение в осадок мыла, жиров Аминокислоты N H2 – C H – C O O H
Аминокислоты N H2 – C H – C O O H Что такое хорошо и что такое плохо, Или правила игры от очень строгой химички
Что такое хорошо и что такое плохо, Или правила игры от очень строгой химички Азотная кислота
Азотная кислота Коррозия металлов. Классификация коррозионных процессов
Коррозия металлов. Классификация коррозионных процессов Подземное хранение газа и жидкости
Подземное хранение газа и жидкости Масса и формулы. Химия 8 класс
Масса и формулы. Химия 8 класс Метал конструкциялық материалдар
Метал конструкциялық материалдар Вуглеводи
Вуглеводи Процессы и технологическая схема производства сегодня. АО Газпромнефть-ОНПЗ
Процессы и технологическая схема производства сегодня. АО Газпромнефть-ОНПЗ