Содержание
- 2. Урок - зачет
- 3. Периодический закон и периодическая система химических элементов Д.И.Менделеева.
- 4. Периодический закон «Свойства химических элементов и образованных ими веществ находятся в периодической зависимости от заряда ядра
- 5. Порядковый номер элемента, номер периода и номер группы в Периодической системе Д.И.Менделеева отражают какую-либо особенность или
- 6. Порядковый номер элемента указывает на заряд атомного ядра, т.е. число протонов в атоме и на число
- 7. Номер периода указывает на число энергетических уровней в атоме.
- 8. Номер группы указывает на число электронов на внешнем энергетическом уровне атомов для элементов главных подгрупп или
- 9. В каждой группе находятся две подгруппы: главная и побочная. В главной подгруппе находятся и металлы и
- 10. В пределах одного и того же периода металлические свойства ослабевают, а неметаллические усиливаются. В пределах одной
- 11. Виды химической связи.
- 12. Химическая связь – это такое взаимодействие атомов, которое связывает их в молекулы, ионы, радикалы, кристаллы. Различают
- 13. это связь, возникающая между атомами за счет образования общих электронных пар. По степени смещенности общих электронных
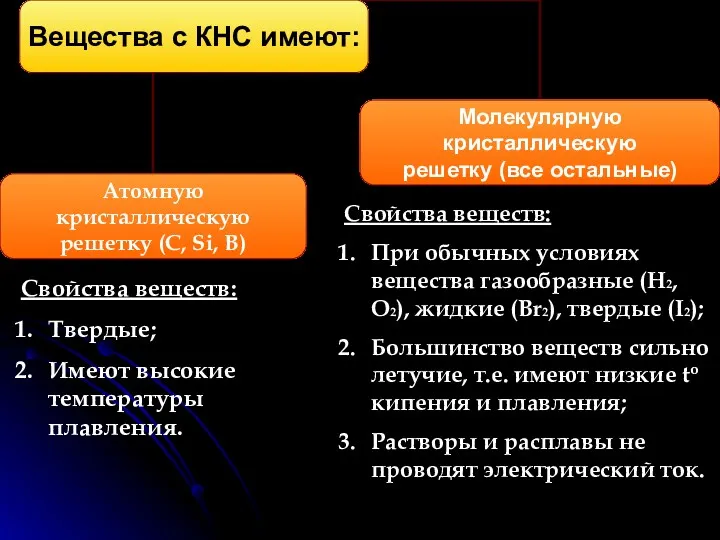
- 14. КНС образуют атомы одного и того же химического элемента. Механизм образования связи. Каждый атом неметалла отдает
- 15. Свойства веществ: Твердые; Имеют высокие температуры плавления. Свойства веществ: При обычных условиях вещества газообразные (H2, O2),
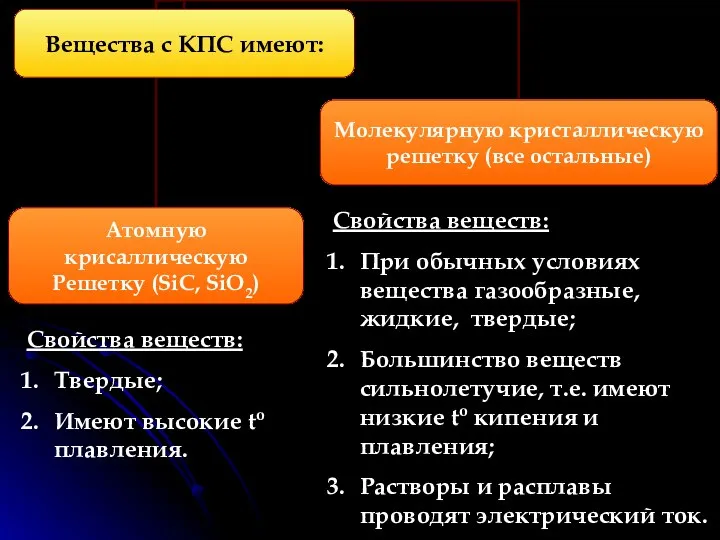
- 16. КПС образуют атомы разных неметаллов (с разной электороотрицательностью). Электроотрицательность (ЭО)- это свойство атомов одного элемента притягивать
- 17. Свойства веществ: При обычных условиях вещества газообразные, жидкие, твердые; Большинство веществ сильнолетучие, т.е. имеют низкие to
- 18. ИС образуется между атомами металлов и неметаллов, т.е. между атомами резко отличающимися друг от друга по
- 19. Свойства веществ: Все вещества при обычных условиях твердые. Имеют высокие температуры кипения и плавления. Расплавы и
- 20. Металлическая связь – связь в металлах и сплавах, которую выполняют относительно свободные электроны между ионами металлов
- 21. Водородная связь – связь между атомами водорода одной молекулы и сильноотрицательными элементами (O, N, F) другой
- 22. Механизм возникновения связи: Протон одной молекулы притягивается неподеленной электронной парой атома другой молекулы. Примеры веществ: водородные
- 23. А-1 В каком ряду написаны вещества только с ковалентной полярной связью? а) хлор, аммиак, хлороводород б)
- 24. А-2. Термин «молекула» нельзя употреблять при характеристике строения 1) сероводорода 2) азотной кислоты 3) озона 4)
- 25. А-3 Какая химическая связь образуется между атомами элементов с порядковыми номерами 9 и 19? 1) ионная
- 26. А-4 Различие в значении температур плавления CO2 (- 56,6) и SiO2 (+ 1728) объясняется 1) различием
- 27. А-5 В веществе CH3 – CH3 связь между атомами углерода 1) ковалентная неполярная 2) ковалентная полярная
- 28. В-1 Установите соответствие между формулой вещества и видом химической связи Формула вещества Вид химической связи А)
- 29. Молодцы!
- 30. Домашнее задание Повторить по записям виды хим.связи и типы кристаллических решёток Придумать свой тест или сделать
- 32. Скачать презентацию



























 бензол
бензол Курс биохимии. Биохимия крови
Курс биохимии. Биохимия крови Инструментальные методы исследования органических веществ
Инструментальные методы исследования органических веществ Беймет алдар
Беймет алдар Классы неорганических веществ
Классы неорганических веществ Классификация и номенклатура неорганических веществ
Классификация и номенклатура неорганических веществ Эко-упаковка
Эко-упаковка IVA группа С, Si, Ge, Sn, Pb (подгруппа титана)
IVA группа С, Si, Ge, Sn, Pb (подгруппа титана) Закон сохранения массы вещества
Закон сохранения массы вещества Комплексні сполуки. Комплексоутворення в біологічних системах
Комплексні сполуки. Комплексоутворення в біологічних системах Влияние состава вещества на эффективность таяния льда и замерзания водных солевых растворов
Влияние состава вещества на эффективность таяния льда и замерзания водных солевых растворов Периодический закон Д.И. Менделеева. Строение атома. Химическая связь
Периодический закон Д.И. Менделеева. Строение атома. Химическая связь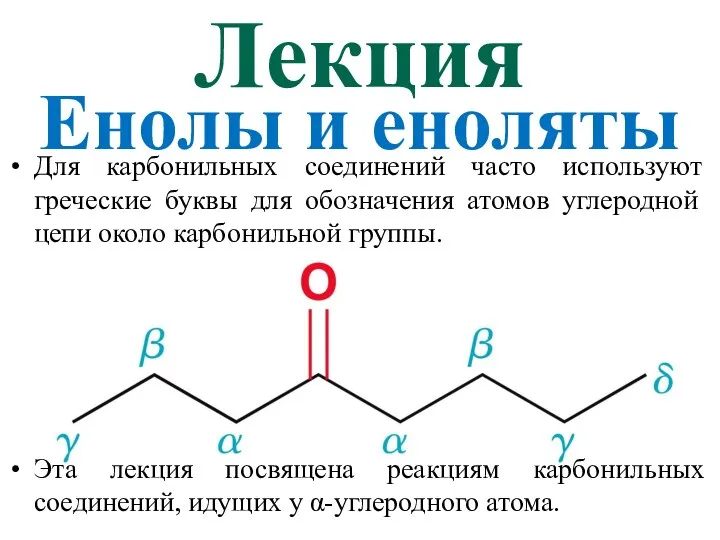 Енолы и еноляты
Енолы и еноляты Периодическая система химических элементов Д.И. Менделеева
Периодическая система химических элементов Д.И. Менделеева Кислород. Общая характеристика и нахождение в природе. 8 класс
Кислород. Общая характеристика и нахождение в природе. 8 класс Гниение. Брожение
Гниение. Брожение Щелочноземельные металлы
Щелочноземельные металлы Виведення молекулярної формули речовини за загальною формулою гомологічного ряду та густиною або відносною густиною
Виведення молекулярної формули речовини за загальною формулою гомологічного ряду та густиною або відносною густиною Химические элементы в организме человека
Химические элементы в организме человека Полімерні композиційні матеріали
Полімерні композиційні матеріали Белки. 9 класс
Белки. 9 класс Введение в органическую химию
Введение в органическую химию Гидролиз органических и неорганических соединений
Гидролиз органических и неорганических соединений Задачи на смеси и сплавы. Метод Пирсона
Задачи на смеси и сплавы. Метод Пирсона Гигиена труда при работе с пестицидами и минеральными удобрениями
Гигиена труда при работе с пестицидами и минеральными удобрениями ГИДРОЛИЗ СОЛЕЙ 9 класс
ГИДРОЛИЗ СОЛЕЙ 9 класс Классификация химических реакций
Классификация химических реакций Химия. Отличие химических свойств от физических
Химия. Отличие химических свойств от физических