Содержание
- 2. Термодинамически однородная по составу и свойствам часть термодинамической системы, отделенная от других фаз поверхностями раздела, на
- 3. ГРАНИЦЫ РАЗДЕЛА ФАЗ
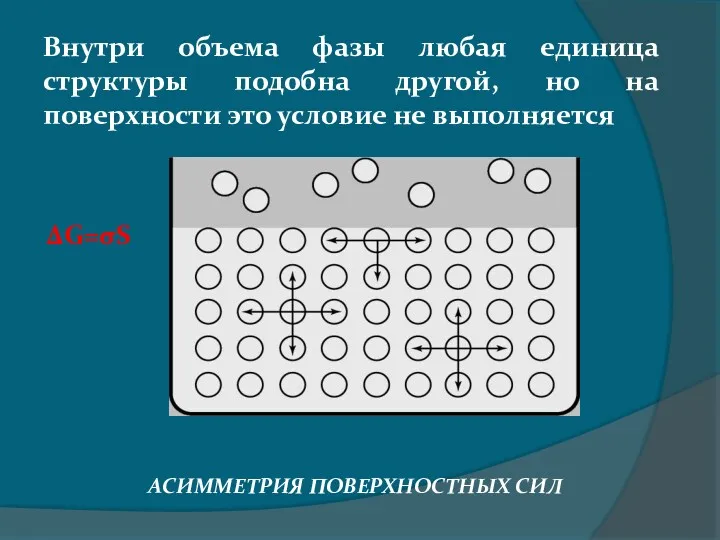
- 4. Внутри объема фазы любая единица структуры подобна другой, но на поверхности это условие не выполняется ΔG=σS
- 5. Поверхностное натяжение (σ) – это удельная свободная поверхностная энергия приходящаяся на единицу межфазной поверхности (сила, отнесенная
- 6. Величина поверхностного натяжения чистой жидкости при данной температуре на данной границе раздела есть величина строго определенная.
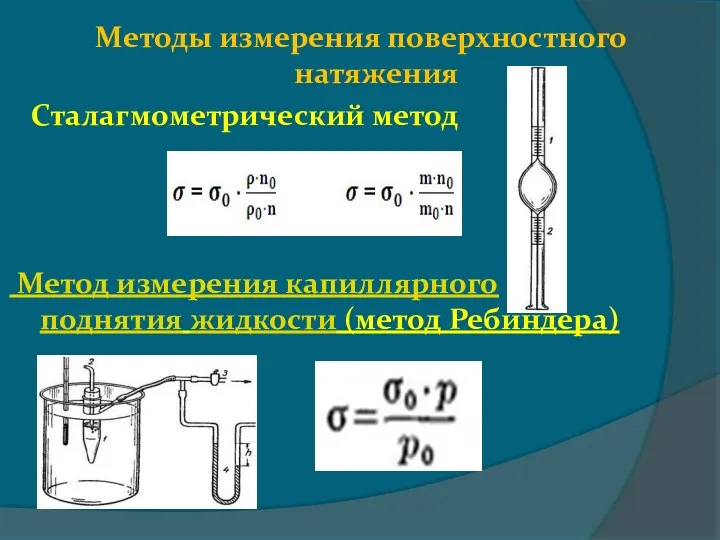
- 7. Методы измерения поверхностного натяжения Сталагмометрический метод Метод измерения капиллярного поднятия жидкости (метод Ребиндера)
- 8. Способность вещества понижать поверхностное натяжение на границе раздела фаз называется поверхностной активностью (g) g=- Δσ/Δc Правило
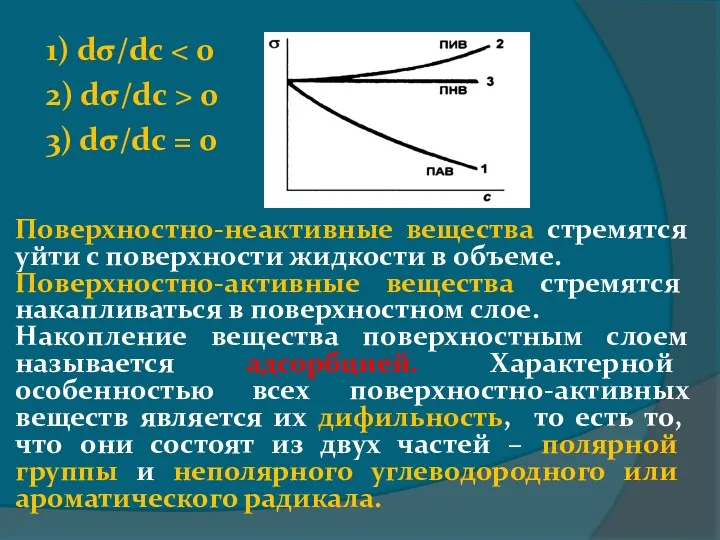
- 9. 1) dσ/dc 2) dσ/dc > 0 3) dσ/dc = 0 Поверхностно-неактивные вещества стремятся уйти с поверхности
- 10. Изменение поверхностного натяжения на поверхностях клеток и органелл играет значительную роль в таких явлениях, как клеточное
- 11. Адсорбция - это явление концентрирования вещества на поверхности раздела фаз. Адсорбент - вещество, на поверхности которого
- 12. Адсорбция происходит на поверхности раздела фаз газ/твердое тело, раствор/твердое тело, газ/жидкость, жидкость/жидкость. Адсорбция бывает мономолекулярная (на
- 13. Типы адсорбционных взаимодействий Физическая адсорбция Молекулярная адсорбция Обусловлена силами межмолекулярного взаимодйствия (Ван-дер-Ваальса), возникающими между частицами адсорбата
- 14. Часто при адсорбции газов образуется мономолекулярный слой. При адсорбции на однородной поверхности концентрация адсорбата в любой
- 15. Дж. Гиббс на основе второго закона термодинамики в 70-х гг. XIX в. вывел важное уравнение, связывающее
- 16. 1. Г > 0, если dσ /dC Т.е. положительная адсорбция всегда наблюдается при уменьшении поверхностного натяжения
- 17. 1.Изотерма Генри При малых давлениях (концентрациях) адсорбата величина адсорбции пропорциональна давлению или концентрации адсорбата: Г =
- 18. 2. Изотерма Ленгмюра. Адсорбция бывает нелокализованная (молекулы адсорбата могут свободно перемещаться вдоль поверхности адсорбента). Локализованная адсорбция
- 19. Адсорбция растворённого в жидкости вещества на твёрдом адсорбенте Различают молекулярную и ионную адсорбцию. Молекулярная адсорбция –
- 20. На молекулярную адсорбцию влияют: -равновесная концентрация растворённого вещества; -природа растворителя; -природа адсорбента; -природа растворённого вещества; -температура,
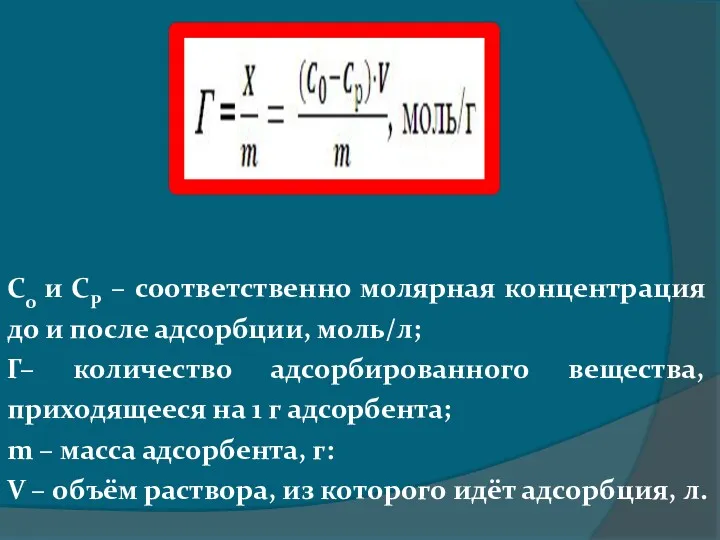
- 21. С0 и СР – соответственно молярная концентрация до и после адсорбции, моль/л; Г– количество адсорбированного вещества,
- 22. Ионнообменная адсорбция В случае ионной адсорбции один из ионов часто адсорбируется избирательно. Правила избирательной адсорбции были
- 23. Особенности ионной адсорбции: Адсорбируются заряженные частицы (ионы), а не молекулы. Адсорбция происходит только на полярных адсорбентах,
- 24. Хроматогра́фия (от др. –греч. χρῶμα — цвет) — динамический сорбционный метод разделения и анализа смесей веществ,
- 25. Качественный хроматографический анализ, т.е. индетификация вещества по его хроматограмме, может быть выполнен сравнением хроматограических характеристик, чаще
- 26. В современной хроматографии для разделения веществ, кроме молекулярной адсорбции, используют и другие физико-химические явления. Имеется несколько
- 27. -По механизмам разделения, т.е. по характеру взаимодействия между сорбентом и сорбатом. По этой классификации хроматографию подразделяют
- 28. Применение адсорбционных процессов в медицине Адсорбция лежит в основе клинического анализа крови на СОЭ (скорость осаждения
- 29. Адсорбционная терапия применяется для удаления токсинов и вредных веществ из пищеварительного тракта. Такие адсорбенты, как гидроксид
- 30. Хорошей адсорбирующей способностью обладает клетчатка. Содержание клетчатки у больных сахарным диабетом должно быть не меньше 25
- 31. Физико-химия дисперсных систем
- 32. «Жизнь – это особая коллоидная система, это особое царство природных вод» (В.И. Вернадский). Дисперсные системы, в
- 33. То вещество, которое присутствует в меньшем количестве и распределено в объеме другого, называют дисперсной фазой. Она
- 34. Признаки дисперсной системы 1. Гетерогенность 2. Дисперсность С уменьшением размера частиц при дроблении вещества увеличивается дисперсность,
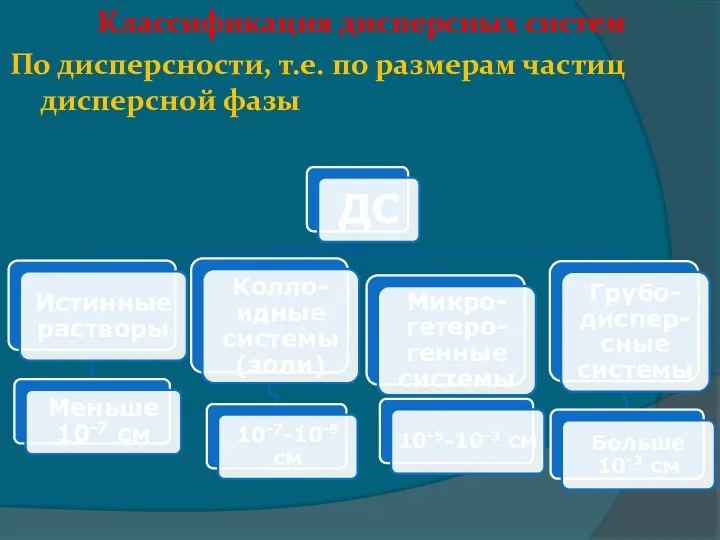
- 35. Классификация дисперсных систем По дисперсности, т.е. по размерам частиц дисперсной фазы
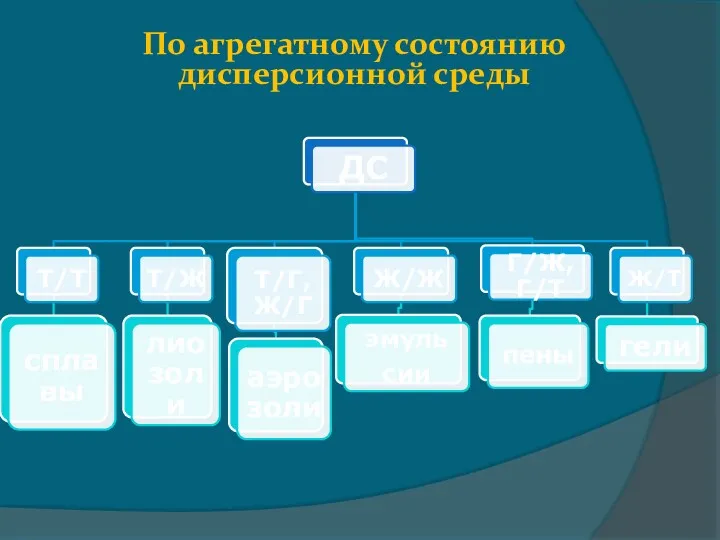
- 36. По агрегатному состоянию дисперсионной среды
- 37. По взаимодействию между частицами дисперсионной среды 1. Свободнодисперсные: частицы дисперсной фазы не связаны друг с другом,
- 38. По межфазному взаимодействию 1. Лиофобные – слабое взаимодействие вещества дисперсной фазы со средой (лиозоли, аэрозоли, эмульсии,
- 39. Переход коллоидной системы из свободнодисперсного состояния в связнодисперсное – гелеобразование, образующиеся при этом структурированные коллоидные системы
- 40. Свойства коллоидных растворов 1. Все коллоидные растворы способны рассеивать свет, т.е. опалесцировать. При наблюдении сбоку виден
- 41. 2. Диффузия частиц в к.р. протекает медленно. 3. К.р. имеют низкое осмотическое давление. Два последних свойства
- 42. Строение коллоидной частицы Для образования коллоидных частиц необходимо три условия: -Дисперсная фаза не должна растворяться в
- 43. Ядро (агрегат), состоящее из большого числа атомов или молекул нерастворимого в растворителе вещества, имеющего кристаллическое строение.
- 44. Двойной электрический слой (ДЭС) ДЭС – это слой, возникающийй на границе твердой и жидкой фазы мицеллы,
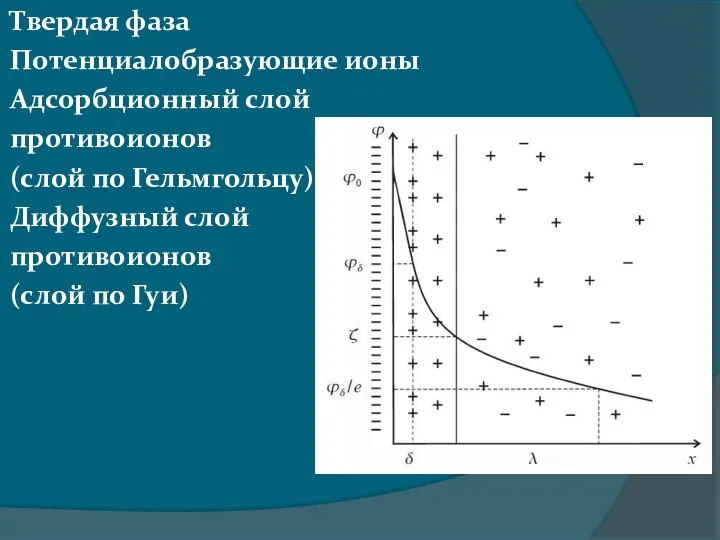
- 45. Твердая фаза Потенциалобразующие ионы Адсорбционный слой противоионов (слой по Гельмгольцу) Диффузный слой противоионов (слой по Гуи)
- 46. AgNO3 + KI = AgI + KNO3 {m [AgI]nI־ (n – x)K+}x־ г р а н
- 47. {m[AgI]nAg+(n- x)NO3־}x+xNO3־ (гранула положительна) {m[AgI]nI ־(n-x)K+}x־xK+ (гранула отрицательна)
- 48. Седиментация - это явление оседания частиц достаточно большой массы под действием гравитационного поля. Грубодисперсные системы (пыль
- 49. Устойчивость коллоидных систем Дисперсные системы в отличие от истинных растворов являются термодинамически неустойчивыми. Под устойчивостью дисперсных
- 50. Факторы, определяющим кинетическую устойчивость -степень дисперсности коллоидных частиц - броуновское движение - вязкость дисперсной среды -
- 51. Коагуляция коллоидных систем Нарушение агрегативной устойчивости коллоидной системы в сторону укрупнения частиц за счет их слипания
- 52. Электролитная коагуляция Основные правила коагуляции: 1. Все электролиты могут вызвать коагуляцию. Но коагулирующим действием обладает только
- 53. Величина ПК зависит от величины заряда иона-коагулятора. Чем выше его валентность, тем меньшая концентрация электролита соответствует
- 54. 3.Коагулирующая способность ионов одинаковой зарядности увеличивается с возрастанием радиуса иона. 4.Коагулирующее действие электролита не сводится только
- 55. Методы получения коллоидных систем I. Диспергирование – дробление крупных частиц грубодисперсных систем до коллоидной степени дисперсности
- 56. Очистка коллоидных систем Низкомолекулярные примеси влияют на свойства системы, поэтому золи приходится очищать с помощью диализа,
- 57. Значение коллоидных систем Многие пищевые продукты, такие как, молоко, сметана, майонез, масло, зефир, пастила, бульон, желе
- 59. Скачать презентацию





































![AgNO3 + KI = AgI + KNO3 {m [AgI]nI־ (n](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/177822/slide-45.jpg)
![{m[AgI]nAg+(n- x)NO3־}x+xNO3־ (гранула положительна) {m[AgI]nI ־(n-x)K+}x־xK+ (гранула отрицательна)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/177822/slide-46.jpg)










 Биогенді (s.p.d) элементтермен олардың қосылыстарының медициналық және биологиялық маңызы
Биогенді (s.p.d) элементтермен олардың қосылыстарының медициналық және биологиялық маңызы Кислоты, их состав и названия
Кислоты, их состав и названия Карбоновые кислоты и их функциональные производные
Карбоновые кислоты и их функциональные производные Ароматические углеводороды
Ароматические углеводороды Гетерофазный катализ. (Лекция 20)
Гетерофазный катализ. (Лекция 20) Горение топлива
Горение топлива Використання радіоактивних ізотопів, як індикаторів у тваринництві і археології
Використання радіоактивних ізотопів, як індикаторів у тваринництві і археології Основные классы неорганических соединений
Основные классы неорганических соединений Соли, их классификация и свойства
Соли, их классификация и свойства Органічна хімія
Органічна хімія Розв’язування задач за рівняннями реакцій з використанням розчинів із певною масовою часткою розчиненої речовини. Урок 13-14
Розв’язування задач за рівняннями реакцій з використанням розчинів із певною масовою часткою розчиненої речовини. Урок 13-14 Жёсткость воды
Жёсткость воды Полисахариды: крахмал и целлюлоза
Полисахариды: крахмал и целлюлоза Растворы. Часть 2. Лекция №7
Растворы. Часть 2. Лекция №7 Химия атмосферы. Химические процессы в тропосфере
Химия атмосферы. Химические процессы в тропосфере Буферные системы
Буферные системы Белки. Строение
Белки. Строение Классификация химических элементов. Составитель. 8 класс
Классификация химических элементов. Составитель. 8 класс Минералы для ИЗБ
Минералы для ИЗБ Концентрация растворов. Массовая доля растворенного вещества. Урок 1
Концентрация растворов. Массовая доля растворенного вещества. Урок 1 Химический элемент медь
Химический элемент медь Кинетика химических реакций
Кинетика химических реакций Кремний и его соединения
Кремний и его соединения Галогены. Расположите галогены в порядке их открытия
Галогены. Расположите галогены в порядке их открытия Важнейшие реакции в органической химии
Важнейшие реакции в органической химии Технология производства аминоальдегидных смол
Технология производства аминоальдегидных смол Углерод. Физические и химические свойства
Углерод. Физические и химические свойства Гидролиз солей
Гидролиз солей