Содержание
- 2. Цель урока: выявить причину существования органической химии как самостоятельного раздела химии Результаты урока: 1. Приводить определения
- 3. Вода Бензин Азот Нефть Жиры Белки Хлорка Капрон Аспирин Мрамор Вискоза Сода Углеводы Мел Серная кислота
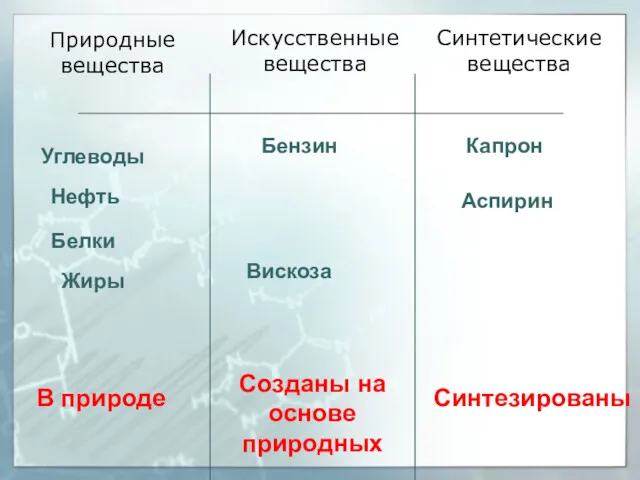
- 4. Природные вещества В природе Созданы на основе природных Синтезированы Искусственные вещества Cинтетические вещества
- 5. 1807 г. Берцелиус 1878 г. Шорлеммер 1845 г. Кекуле
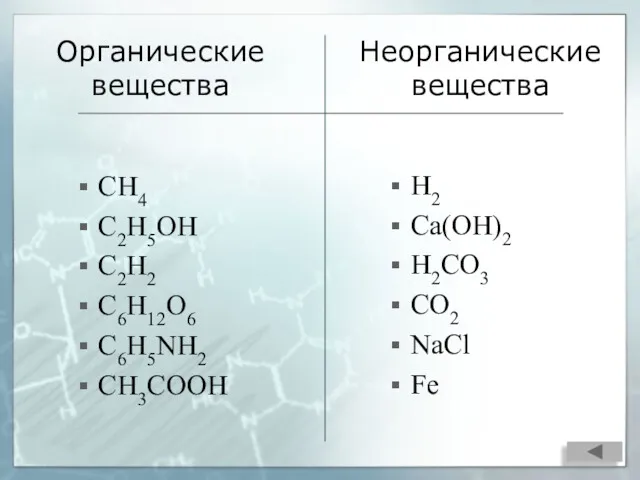
- 6. Органические вещества CH4 C2H5OH C2H2 C6H12O6 C6H5NH2 CH3COOH H2 Ca(OH)2 H2CO3 CO2 NaCl Fe Неорганические вещества
- 7. Особенности органических веществ 1. В состав обязательно входят атомы С и Н Горючесть, обугливание при нагревании
- 8. Органические вещества горючи
- 9. Обугливаются при нагревании Древесина Мясо Сахар
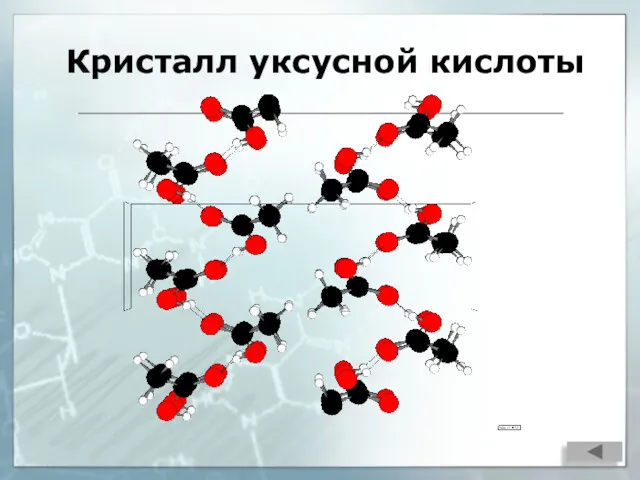
- 10. Кристалл уксусной кислоты
- 11. Большинство органических веществ не растворимо в воде
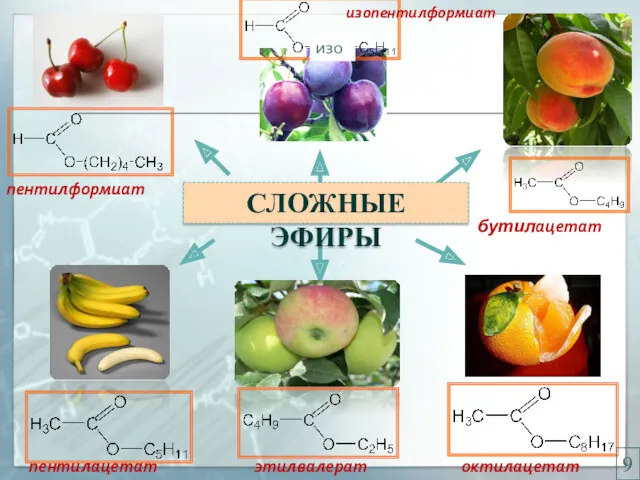
- 12. пентилформиат изопентилформиат пентилацетат октилацетат изо бутилацетат этилвалерат СЛОЖНЫЕ ЭФИРЫ 9
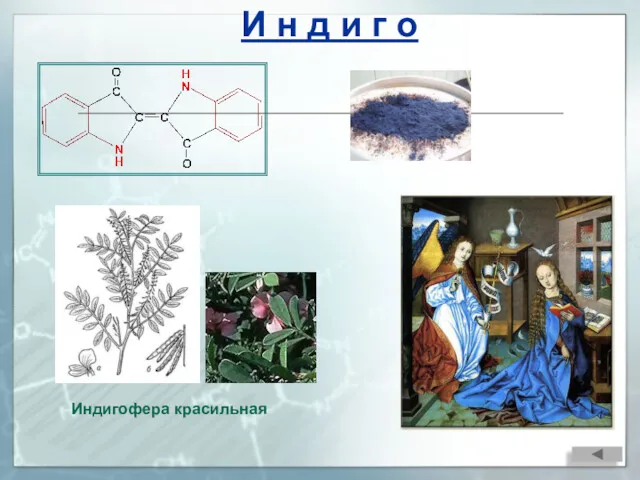
- 13. И н д и г о
- 14. Органические соединения ~ 100 млн. ~ 700 тыс. Неорганические соединения
- 15. ↓ Многочисленность органических веществ ↓↑ ↓ ↓ 2s2 2p2 ↓ Валентность углерода IV Маленький радиус атома
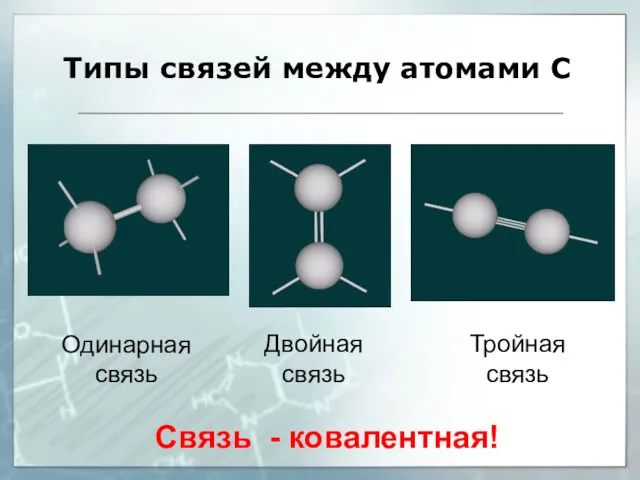
- 16. Типы связей между атомами С Тройная связь Двойная связь Одинарная связь Связь - ковалентная!
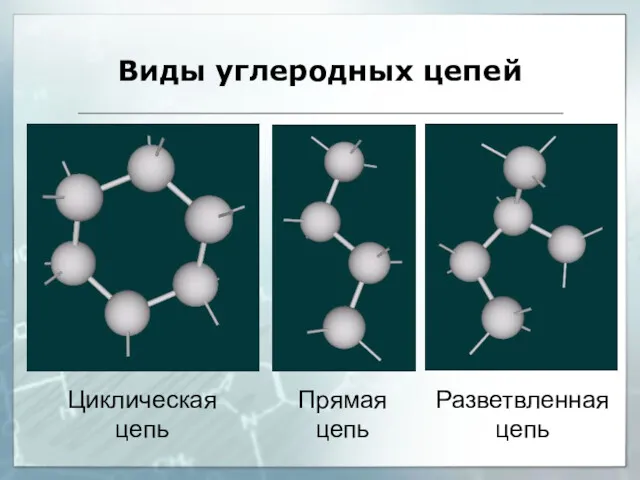
- 17. Виды углеродных цепей Разветвленная цепь Прямая цепь Циклическая цепь
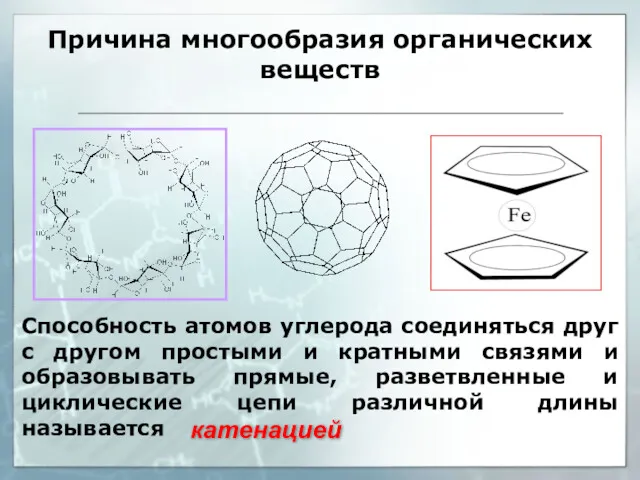
- 18. Причина многообразия органических веществ Способность атомов углерода соединяться друг с другом простыми и кратными связями и
- 19. ИЗОМЕРИЯ АПЕЛЬСИН СПАНИЕЛЬ ПАЛЬТО ЛАПОТЬ
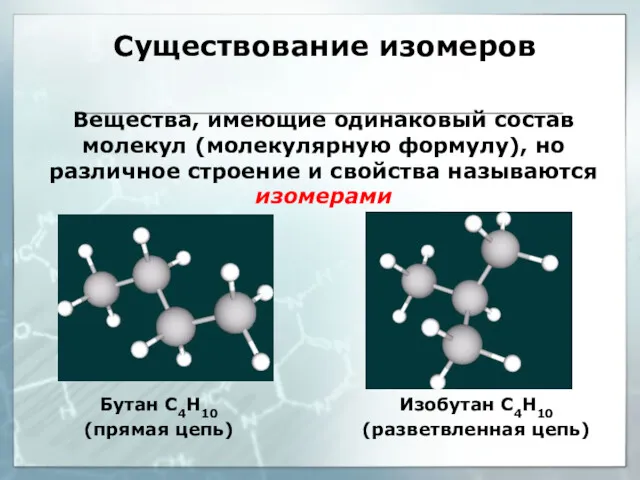
- 20. Существование изомеров Вещества, имеющие одинаковый состав молекул (молекулярную формулу), но различное строение и свойства называются изомерами
- 21. Изомерия - явление существования изомеров
- 22. Существование гомологов Молекулярные формулы первых представителей гомологических рядов предельных углеводородов и предельных одноатомных спиртов + СН2
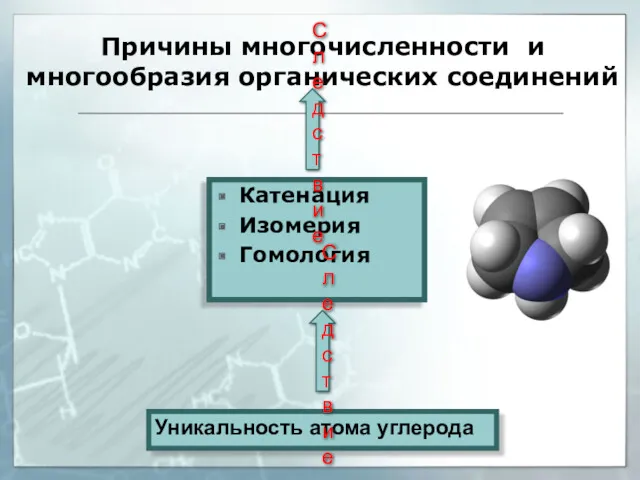
- 23. Причины многочисленности и многообразия органических соединений Катенация Изомерия Гомология Следствие Уникальность атома углерода Следствие
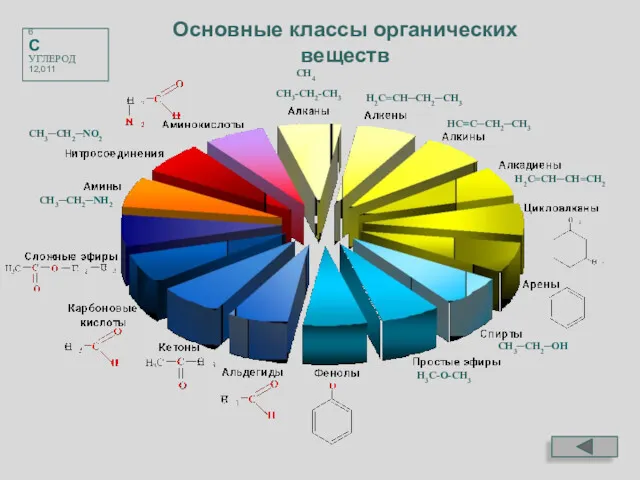
- 24. H3C-O-CH3 CH3-CH2-CH3 6 C УГЛЕРОД 12,011 Основные классы органических веществ H2C=CH─CH2─CH3 HC≡C─CH2─CH3 H2C=CH─CH=CH2 CH3─CH2─OH CH3─CH2─NH2 CH3─CH2─NO2
- 25. Первые попытки объяснения строения органических веществ
- 26. Теория витализма Название образовано от словосочетания “Vis vitalis”-(Лат.)- жизненная сила. Теория, основанная на предположении о том,
- 27. Теория радикалов Ю. Либих Я. Берцелиус Ф. Велер Все молекулы состоят из двух частей- положительно заряженного
- 28. Теория типов Ш. Жерар О. Лоран Существует несколько типов, на которые классифицируют вещества +: Формула и
- 29. Домашнее задание § 1, записи в тетради Принести тетрадь 12 л в обложке для практических работ.
- 30. Экспресс-работа
- 31. Цель: понимание сущности и методологического значения теории органических веществ А.М. Бутлерова Перечислять предпосылки создания теории строения
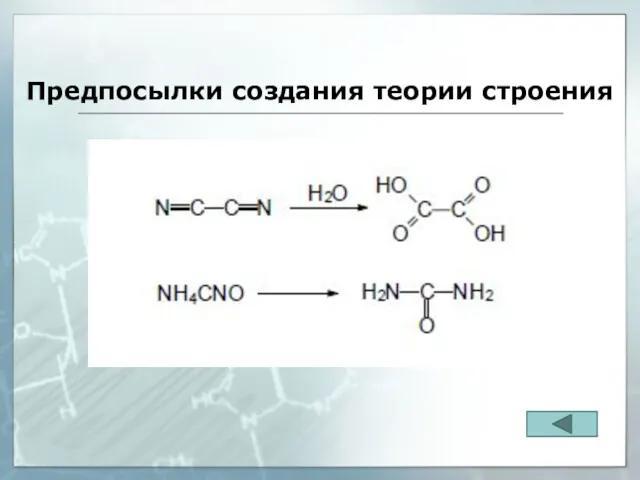
- 32. Предпосылки создания теории строения Личностные качества А.М. Бутлерова
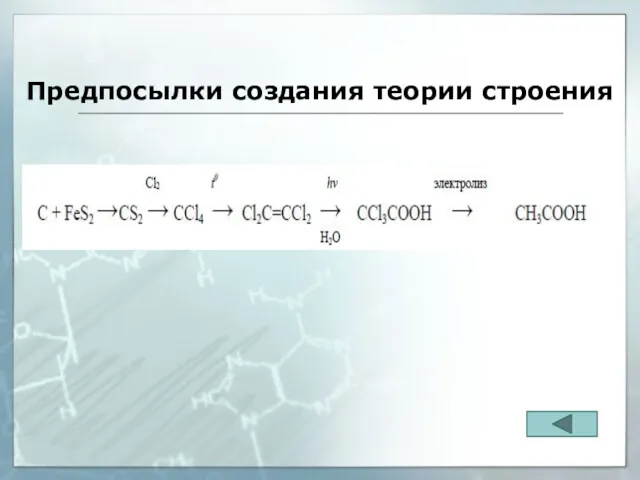
- 33. Предпосылки создания теории строения
- 34. Предпосылки создания теории строения
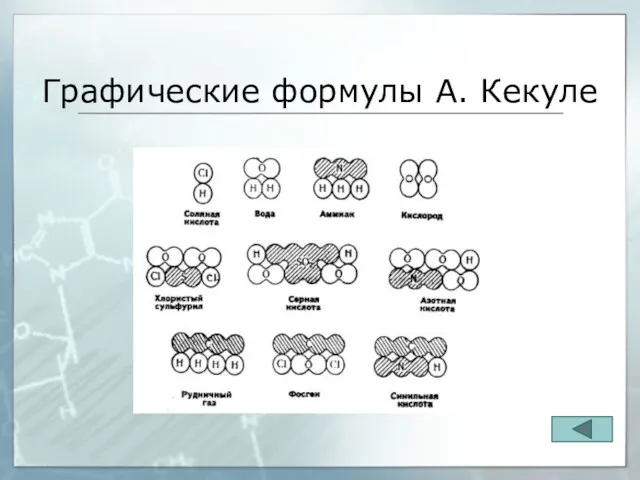
- 35. Графические формулы А. Кекуле
- 36. Химические формулы А. Купера
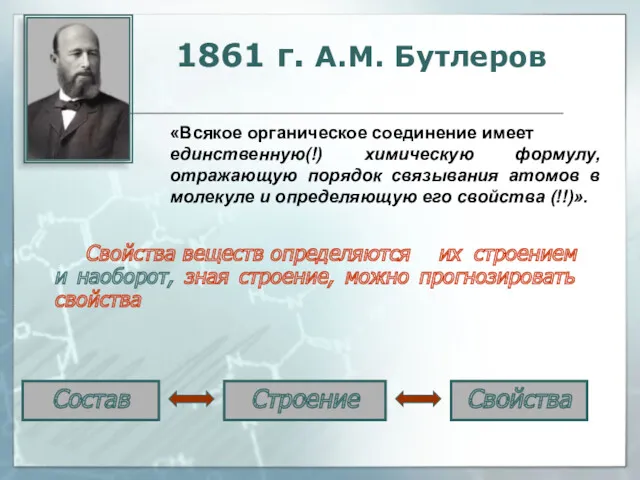
- 37. 1861 г. А.М. Бутлеров Съезд немецких естествоиспытателей г. Карлсруэ «Исходя из мысли, что каждый химический атом,
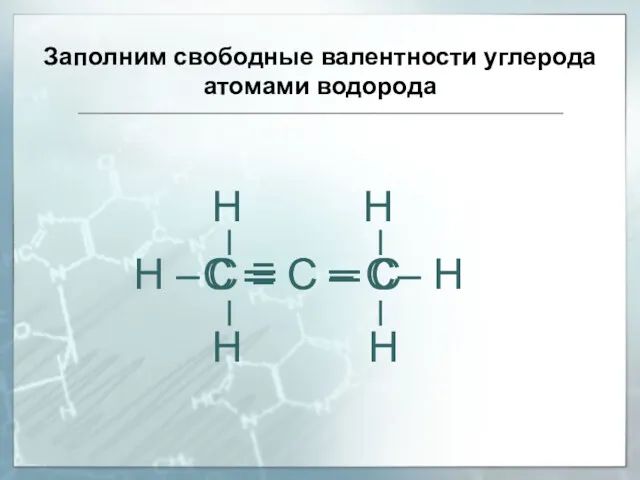
- 38. Заполним свободные валентности углерода атомами водорода С – С – С С ═ С – С
- 39. Заполним свободные валентности углерода атомами водорода С ═ С ═ С Н Н Н Н С
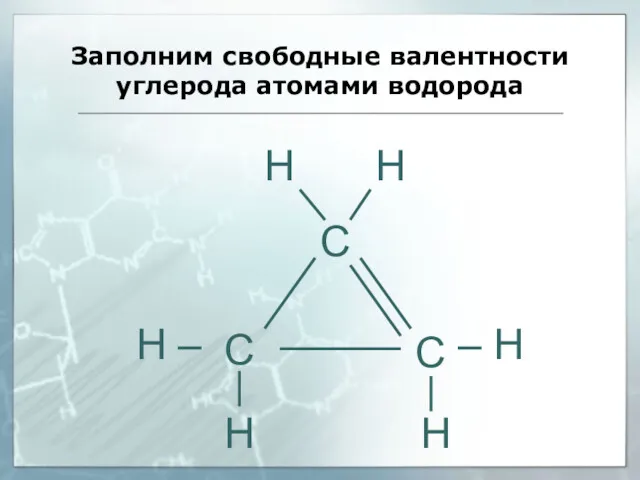
- 40. Заполним свободные валентности углерода атомами водорода С С С – Н Н – Н Н Н
- 41. Свойства веществ определяются их строением и наоборот, зная строение, можно прогнозировать свойства Состав Строение Свойства 1861
- 42. Идентификация, установление состава и строения Элементный анализ – определение содержания атомов различных элементов. 2. Измерение физических
- 43. Луи Пастер: исследования 1848-1854 гг. Две формы винной кислоты идентичны по всем свойствам, исключая: (1) способности
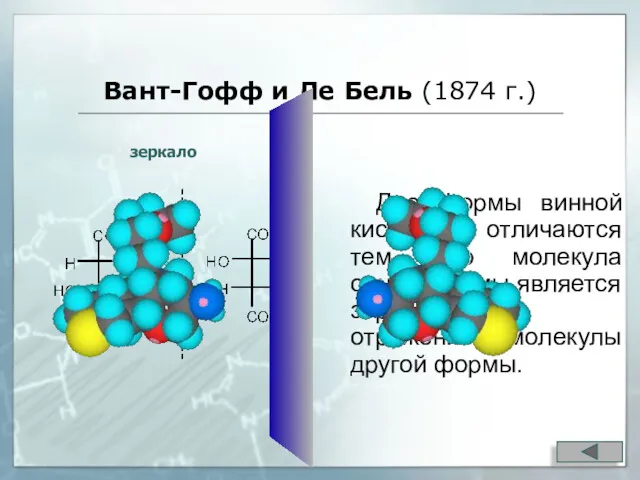
- 44. Вант-Гофф и Ле Бель (1874 г.) Две формы винной кислоты отличаются тем, что молекула одной формы
- 45. «когда четыре сродства атома углерода насыщены четырьмя различными одновалентными группами, можно получить два и только два
- 46. Л. Полинг «Теория резонанса» все молекулы имеют одинаковую геометрию и электронную структуру, но эта последняя такова,
- 47. Домашнее задание Приготовиться к устному ответу по материалам урока Приготовиться к сам. работе Задачи
- 49. Скачать презентацию




























 Растворы. Термодинамика процесса растворения. Способы выражения концентрации. Идеальные растворы. Законы Рауля
Растворы. Термодинамика процесса растворения. Способы выражения концентрации. Идеальные растворы. Законы Рауля Фосфор красный, белый и черный
Фосфор красный, белый и черный Переработка угля
Переработка угля Виды химических реакций
Виды химических реакций Супрамолекулярний контроль для дослідження реакційної здатності та каталізу
Супрамолекулярний контроль для дослідження реакційної здатності та каталізу Алкени і алкіни
Алкени і алкіни Полимеры. Классификация. Строение
Полимеры. Классификация. Строение Лигандообменные равновесия и процессы. Строение комплексных соединений
Лигандообменные равновесия и процессы. Строение комплексных соединений Моделирование, как метод научного исследования. Ограниченный метод Хартри-Фока
Моделирование, как метод научного исследования. Ограниченный метод Хартри-Фока Дисперсные системы
Дисперсные системы Азот и его соединения. Повторение
Азот и его соединения. Повторение Металлы. Определения. Положение в периодической системе. Металлы в алхимии
Металлы. Определения. Положение в периодической системе. Металлы в алхимии Полимерлер-біздің болашағымыз
Полимерлер-біздің болашағымыз Кислородсодержащие органические соединения. 9 класс
Кислородсодержащие органические соединения. 9 класс Водород
Водород Расчеты по химическим уравнениям. Алгоритм решения расчетных задач
Расчеты по химическим уравнениям. Алгоритм решения расчетных задач Тепловой эффект химических реакций. 8 класс
Тепловой эффект химических реакций. 8 класс Теория сильных и слабых электролитов
Теория сильных и слабых электролитов Защита металлов от коррозии
Защита металлов от коррозии Решение комбинированных задач. Задачи на смеси
Решение комбинированных задач. Задачи на смеси Аммиак. Соли аммония
Аммиак. Соли аммония Apparatus of installations with circulating ball catalyst
Apparatus of installations with circulating ball catalyst Циклоалканы
Циклоалканы Ароматические азотсодержащие соединения
Ароматические азотсодержащие соединения Электролитическая диссоциация
Электролитическая диссоциация Атомы и молекулы. Простые и сложные вещества. 8 класс
Атомы и молекулы. Простые и сложные вещества. 8 класс Особенности выбора связующих и наполнителей для производства деталей машин из ПКМ
Особенности выбора связующих и наполнителей для производства деталей машин из ПКМ Гидросульфит натрия (пищевая добавка Е222)
Гидросульфит натрия (пищевая добавка Е222)