Содержание
- 2. Теория электролитической диссоциации (С. Аррениус, 1888–1889) Р а с т в о р ы электролиты неэлектролиты
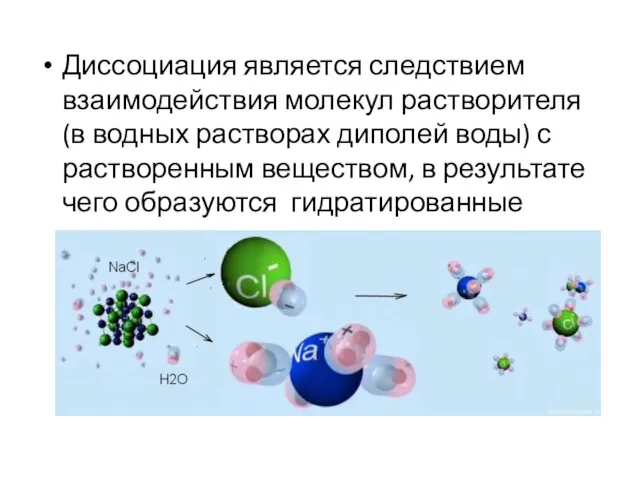
- 3. Диссоциация является следствием взаимодействия молекул растворителя (в водных растворах диполей воды) с растворенным веществом, в результате
- 4. Диссоциация электролитов характеризуется степенью диссоциации α = n / N , где n – число молекул,
- 5. Сильные электролиты при растворении или расплавлении практически полностью распадаются на ионы (α>0.3). К ним относят почти
- 6. Сильные электролиты Оказывается, в растворах сильных электролитов, ожидаемые при полной диссоциации электролита величины повышения температуры кипения,
- 7. Активность электролита Для приближения расчетных данных сильных электролитов Льюис ввел понятие активности электролита, или активности его
- 8. Активность можно представить себе как произведение концентрации на некоторый коэффициент – коэффициент активности: а = f
- 9. Для характеристики зависимости активности иона от концентрации всех находящихся в растворе ионов Льюис ввел понятие об
- 10. Ионная сила плазмы крови 0,15 моль/л, f С увеличением концентрации раствора сильного электролита количество ионов в
- 11. Слабые электролиты. Константа диссоциации. К растворам слабых электролитов, как к равновесным гомогенным системам, приложим закон действующих
- 12. Связь константы диссоциации со степенью диссоциации называется законом разбавления Оствальда : Пусть С - См электролита,
- 13. Многоосновные кислоты и многокислотные основания диссоциируют ступенчато. Например, диссоциация фосфорной кислоты протекает в три ступени: Н3РО4
- 14. Константа диссоциации каждой последующей ступени гораздо меньше предыдущей. Это объясняется тем, что отрыв иона от нейтральной
- 15. Ионное произведение воды. Понятие о рН. Вода, как известно, очень слабый электролит. При комнатной температуре в
- 16. Величина ионного произведения воды является постоянной только при постоянной температуре. Водородным показателем рН называется обратный десятичный
- 17. Реакция среды в растворах слабых кислот. Концентрация ионов Н+, а также рН слабых кислот могут быть
- 18. Прологарифмируем это выражение: lg [Н+] = ½ lg КС; - lg [Н+] = рН; рН =
- 19. Значения рН для различных жидкостей человеческого организма. Одним из удивительных свойств живых организмов является кислотно-основной гомеостаз
- 20. Теория Аррениуса Диссоциация различных классов неорганических веществ – электролитов с точки зрения теории электролитической диссоциации: Кислоты
- 21. Протонная ( протолитическая) теория Бренстеда и Лоури Согласно этой теории кислотой (НА ) называется молекула или
- 22. Основание(В) – молекула или ион, способные присоединять протон: В + Н+ ↔ ВН+ основание сопряженная кислота
- 23. Согласно протонной теории, кислота, отдавая свой протон, превращается в сопряженное основание по схеме кислота I ↔
- 24. Амфолиты Некоторые вещества способны выступать в одних реакциях в роли донора протона, а в других –
- 25. Типичным амфолитом является вода. Молекула воды способна отдать протон той молекуле, которая будет его удерживать прочнее;
- 26. Типы протолитических реакций: Реакция нейтрализации - протолитическая реакция переноса протона от кислоты к основанию, например: кислота
- 27. Гидролиз солей Реакция гидролиза - протолитический процесс взаимодействия ионов солей с молекулами воды, приводящий к образованию
- 28. Гидролиз солей. Гидролиз соли - обменная реакция ионов соли с молекулами воды, приводящая к образованию слабых
- 29. Типы реакций гидролиза. 1. Соль образована ионами сильного основания и сильной кислоты (например, NaCl, KNO3 и
- 30. 2. Соль образована ионами сильного основания и слабой кислоты(например: Na2CO3, KSCN и др.). Na2CO3 + Н2О
- 31. 3. Соль образована ионами слабого основания и сильной кислоты(например, А1С13, FeSO4 и др.). А1Сl3 + Н2О
- 32. 4. Соль образована ионами слабого основания и слабой кислоты: а) соль растворима в воде (например, (NH4)2СО3,
- 33. Реакция среды растворов солей Реакцию среды растворов солей, подвергающихся гидролизу, можно вычислить по формулам: а) для
- 34. Реакция среды растворов солей б) для растворов солей, образованных слабым основанием и сильной кислотой (гидролиз идет
- 35. Гетерогенные равновесия в растворах с осадком . В насыщенных растворах малорастворимых веществ устанавливается равновесие между осадком
- 36. Произведение растворимости это произведение концентраций ионов малорастворимого вещества в его насыщенном растворе в степенях, соответствующих их
- 37. При смешивании растворов, содержащих ионы, дающие нерастворимую соль, начинается выпадение осадка. В первые моменты времени концентрация
- 38. Условие образования осадка: произведение концентраций ионов в растворе должно быть больше, чем величина произведения растворимости данного
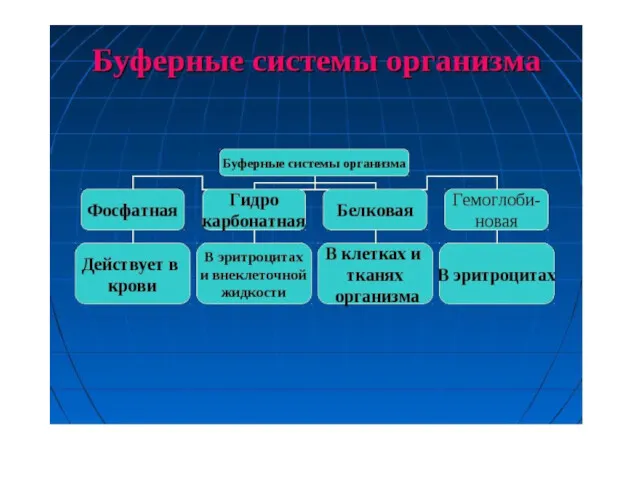
- 39. Буферные растворы Буферными называются растворы, рН которых практически не изменяется от добавления к ним небольших количеств
- 40. К числу исключительных свойств живых организмов относится их способность поддерживать постоянство рН биологических жидкостей, тканей и
- 42. Условие образования буферной системы: Для того чтобы раствор обладал буферными свойствами, в нем должны содержаться слабая
- 43. При добавлении к такому раствору сильной кислоты она будет вступать в реакцию нейтрализации с присутствующим в
- 44. Буферные растворы Простейший буферный раствор- это смесь слабой кислоты и соли, имеющей с этой кислотой общий
- 45. В растворе происходят следующие процессы диссоциации: СН3СООН ↔ СН3СОО- +Н+ - очень слабо СН3СООNa → СН3СОО-
- 46. Механизм буферного действия: Добавим щелочь NaОН (ОН-). Ионы ОН-связываются с ионами Н+ из СН3СООН с образованием
- 47. рН буферной системы Определение рН буферной смеси на примере ацетатной буферной смеси: СН3СООН + СН3СООNa. СН3СООН
- 48. рН буферной системы Так как СН3СООNa → СН3СОО- + Na+ полностью диссоциируют, то [СН3СОО-] = [Сосн]
- 50. Приготовление буферных растворов Для приготовления буферных смесей с желаемым значением рН необходимо взять слабую кислоту или
- 51. Буферная емкость Предел, в котором проявляется буферное действие, называется буферной емкостью (В . Она выражается количеством
- 52. Значение буферных растворов организма Биологическое значение буферных систем огромно. В живых и растительных организмах буферные системы
- 54. Все буферные системы крови и тканевых жидкостей тесно связаны между собой и функционируют как единое целое.
- 57. Скачать презентацию















![Прологарифмируем это выражение: lg [Н+] = ½ lg КС; -](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/124794/slide-17.jpg)




































 Изомеры – это вещества, имеющие одинаковый состав
Изомеры – это вещества, имеющие одинаковый состав Природный газ
Природный газ Благородные металлы
Благородные металлы Типы химических реакций
Типы химических реакций General characteristics of halogens. Halogen compounds
General characteristics of halogens. Halogen compounds Свойства воды. Гидросфера
Свойства воды. Гидросфера Углеводороды (классификация и номенклатура)
Углеводороды (классификация и номенклатура) Прості і складні речовини. Метали і неметали
Прості і складні речовини. Метали і неметали Металлы и сплавы
Металлы и сплавы Создание слоев пористого кремния на p-Si
Создание слоев пористого кремния на p-Si становление органической химии
становление органической химии Ультраосновные породы (гипербазиты)
Ультраосновные породы (гипербазиты) Термодинамика
Термодинамика Роль хімії у розв`язанні екологічної проблеми
Роль хімії у розв`язанні екологічної проблеми Су - тіршілік көзі
Су - тіршілік көзі Амінокислоти
Амінокислоти Химия аминокислот. Лекция № 4
Химия аминокислот. Лекция № 4 Скорость химических реакций
Скорость химических реакций Сравнительный анализ установки изомеризации между Павлодарским НПЗ и Московским НПЗ
Сравнительный анализ установки изомеризации между Павлодарским НПЗ и Московским НПЗ Каучук туралы жалпы мәліметтер
Каучук туралы жалпы мәліметтер Обобщение по типам химических реакций
Обобщение по типам химических реакций Теория электролитической диссоциации
Теория электролитической диссоциации Строение электронных оболочек атомов химических элементов 8 класс
Строение электронных оболочек атомов химических элементов 8 класс Көміртек оксидтері
Көміртек оксидтері Химические реакции
Химические реакции Химическое равновесие. Классификация реакций по признаку обратимости
Химическое равновесие. Классификация реакций по признаку обратимости Химия и повседневная жизнь человека
Химия и повседневная жизнь человека Гидроксид железа
Гидроксид железа