Слайд 2

Цели урока: повторить отличия химических явлений от физических. Сформировать знания о
признаках и условиях протекания химических реакций, эндо – экзотермических реакциях.
Слайд 3

Правила техники безопасности при проведение лабораторных опытов в кабинете химии
Как правильно
закрепить пробирку в держателе?
Можно ли пробовать реактивы на вкус?
Как правильно определить запах вещества?
Как правильно нагревать пробирку?
Как правильно растворять кислоты водой?
Как правильно зажечь спиртовку?
Как правильно затушить спиртовку?
Почему при проведении опытов необходимо использовать защитную одежду?
Когда можно приступать к выполнению лабораторных опытов?
Слайд 4
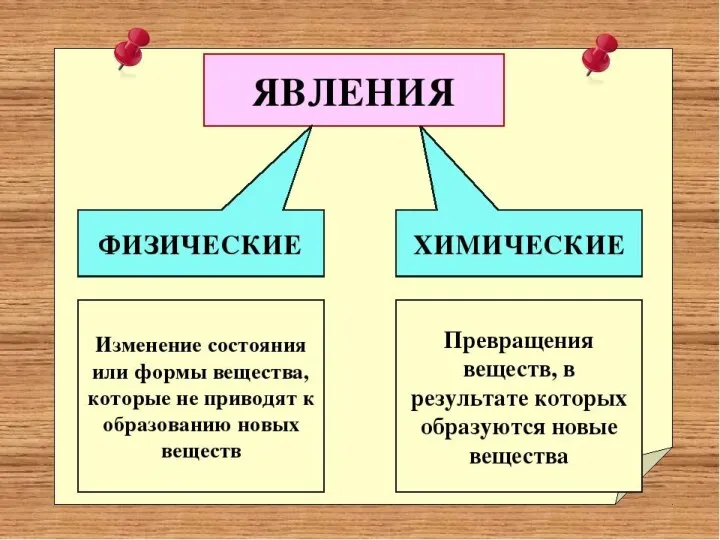
Слайд 5
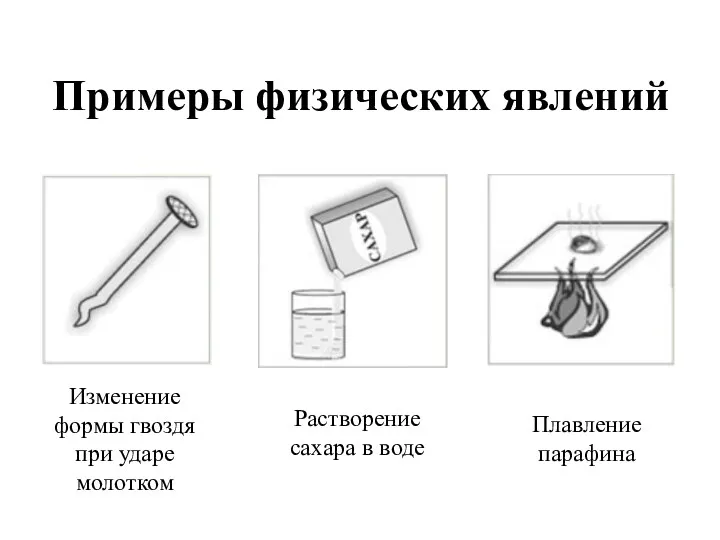
Примеры физических явлений
Изменение формы гвоздя при ударе молотком
Растворение сахара в воде
Плавление
парафина
Слайд 6

Примеры химических явлений
Ржавление железа
Горение бензина
Скисание молока
Слайд 7

Проверь себя
Укажите о каких явлениях (физических или химических) идет речь.
кипение воды;
образование на деревьях инея;
скисание молока;
ржавление гвоздя;
таяние льда;
горение бенгальских огней;
гниение растений;
выпадение дождя;
приготовление сахарной пудры из сахара;
горение свечи.
Слайд 8
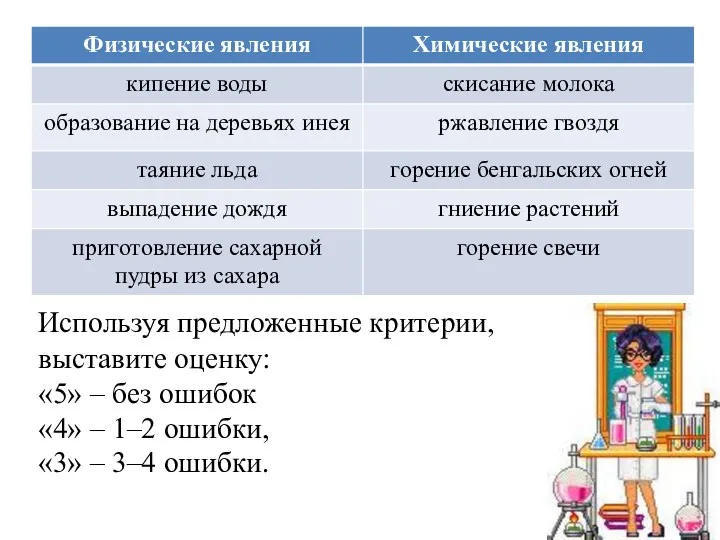
Используя предложенные критерии,
выставите оценку:
«5» – без ошибок
«4» – 1–2 ошибки,
«3»
– 3–4 ошибки.
Слайд 9

Слайд 10

Опыт №1. «Взаимодействие хлорида аммония с гидроксидом натрия»
« К белому кристаллическому
веществу добавили щелочи и подогрели. В результате появился резкий ____________.
Вывод. Признак превращения – появление ____________. Значит это - ________________ явление.»
Слайд 11

Опыт №2. «Взаимодействие гидроксида натрия с серной кислотой»
«К раствору щелочи добавили
раствор индикатора фенолфталеина. Раствор приобрел ________ цвет. После добавления раствора кислоты цвет раствора стал __________.
Вывод. Признак превращения – изменение ____________ . Значит это ________________ явление»
Слайд 12
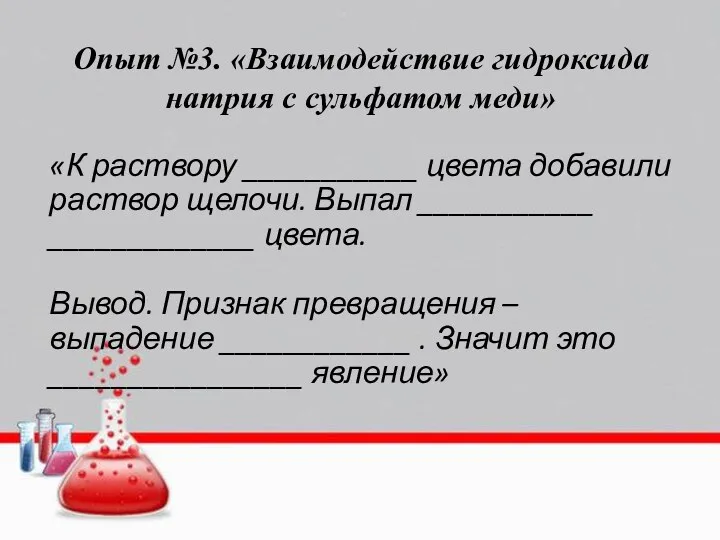
Опыт №3. «Взаимодействие гидроксида натрия с сульфатом меди»
«К раствору ___________ цвета
добавили раствор щелочи. Выпал ___________ _____________ цвета.
Вывод. Признак превращения – выпадение ____________ . Значит это ________________ явление»
Слайд 13

Опыт №4. «Взаимодействие гидроксида меди с серной кислотой»
«К осадку ___________ цвета
добавили раствор кислоты. Наблюдали ___________ осадка
Вывод. Признак превращения растворение ____________ . Значит это ________________ явление»
Слайд 14

Опыт №5. «Разложение перманганата калия»
« При поджигании сыпучего кристаллического вещества _____________
цвета происходит выделение ____________.
Вывод. Признак превращения – выделение ___________ . Значит это - __________ явление.
Слайд 15

Опыт №6. «Взаимодействие карбоната кальция с соляной кислотой»
« К белому кристаллическому
веществу добавили кислоту. В результате выделяется ____________.
Вывод. Признак превращения – выделение ____________. Значит это - ________________ явление.»
Слайд 16

Опыт №7. «Горение магния»
« При поджигании сыпучего кристаллического вещества _____________ цвета
происходит выделение ____________.
Вывод. Признак превращения – выделение ___________ . Значит это - __________ явление.
Слайд 17

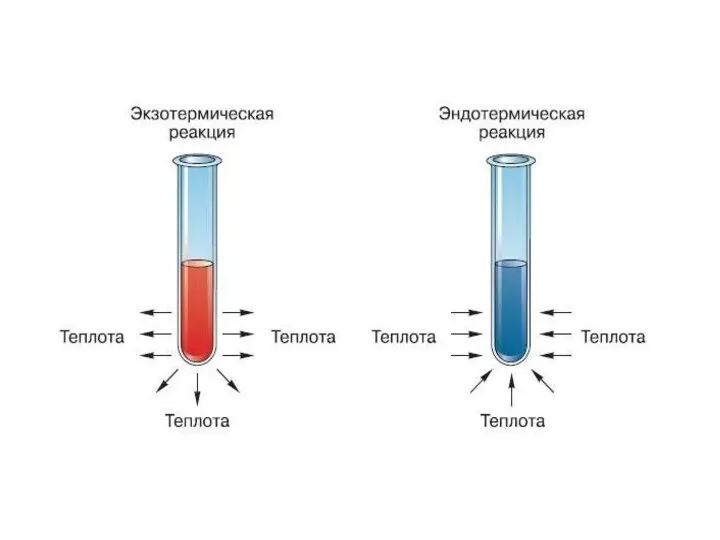
Признаки химической реакции
Выделение или поглощение теплоты
Изменение цвета
Выделение запаха
Выпадение (растворение) осадка
Выделение газа
Выделение
света
Слайд 18
Слайд 19

Проверь себя
Определите, какие реакции в данном перечне относятся к экзо-, а
какие к эндотермическим.
а) 2Н2О = 2Н2 + О2 – Q;
б) 2Mg + О2 = 2MgO + Q;
в) Fе + S = FеS + 95,4 кДж;
г) N2 + О2 = 2NO – 180,8 кДж;
Слайд 20

Подведение итогов
Что изучали на уроке?
Какие признаки химических реакций вы знаете?
Какие реакции
называются экзотермическими?
Какие реакции называются эндотермическими?



















 Гетероциклдық қосылыстардың туындылары
Гетероциклдық қосылыстардың туындылары Непредельные углеводороды этиленового ряда (олефины, алкены)
Непредельные углеводороды этиленового ряда (олефины, алкены) План характеристики елемента за його положенням у періодичній системі та будовою атома
План характеристики елемента за його положенням у періодичній системі та будовою атома Кислородсодержащие органические соединения. Спирты
Кислородсодержащие органические соединения. Спирты Biomass Feedstocks
Biomass Feedstocks Химическая взрывчатка
Химическая взрывчатка Электрофизические свойства GaAs, зонная структура, полупроводящий и полуизолирующий GaAs, способы создания p-n перехода
Электрофизические свойства GaAs, зонная структура, полупроводящий и полуизолирующий GaAs, способы создания p-n перехода Оксиды, их классификация и свойства (8 класс)
Оксиды, их классификация и свойства (8 класс) Практическая работа. Химический состав клетки
Практическая работа. Химический состав клетки Оксиды. Классификация оксидов
Оксиды. Классификация оксидов Закон Авогадро. Молярный объём газов
Закон Авогадро. Молярный объём газов Значення хімії у повсякденному житті
Значення хімії у повсякденному житті Пегматитовые месторождения
Пегматитовые месторождения Строение, свойства и функции белков
Строение, свойства и функции белков Спирты. Виды спирта
Спирты. Виды спирта Геохимические барьеры
Геохимические барьеры Классификация органических соединений
Классификация органических соединений Азотсодержащие соединения
Азотсодержащие соединения Ковалентний зв’язок. Донорно - акцепторний механізм утворення ковалентного зв'язку
Ковалентний зв’язок. Донорно - акцепторний механізм утворення ковалентного зв'язку Водород. Химический знак - H
Водород. Химический знак - H Проект: жило-было мыло
Проект: жило-было мыло Электрохимический ряд напряжений металлов. Свойства металлов
Электрохимический ряд напряжений металлов. Свойства металлов Магний и кальций
Магний и кальций Водород. Нахождение в природе. Физические и химические свойства. Применение
Водород. Нахождение в природе. Физические и химические свойства. Применение Синтетичні високомолекулярні речовини і полімерні матеріали на їх основі
Синтетичні високомолекулярні речовини і полімерні матеріали на їх основі Группа веществ, изолируемых из биологического материала дистилляцией
Группа веществ, изолируемых из биологического материала дистилляцией Количество вещества. 8 класс
Количество вещества. 8 класс Железоуглеродистые сплавы
Железоуглеродистые сплавы