Содержание
- 2. Кислоты это сложные вещества, имеющие в своем составе водород, способный замещаться на металл, и кислотный остаток.
- 3. Узнай загадочную кислоту “Из всех кислот она конечно, прима! Присутствует везде и зримо и не зримо.
- 4. Самая важная кислота Для взрывчатых веществ нужна она, для красителей, лаков, лекарств идет самая важная из
- 5. Узнай загадочную кислоту Алхимикам удалось получить эту кислоту еще в X веке при прокаливании некоторых сульфатов
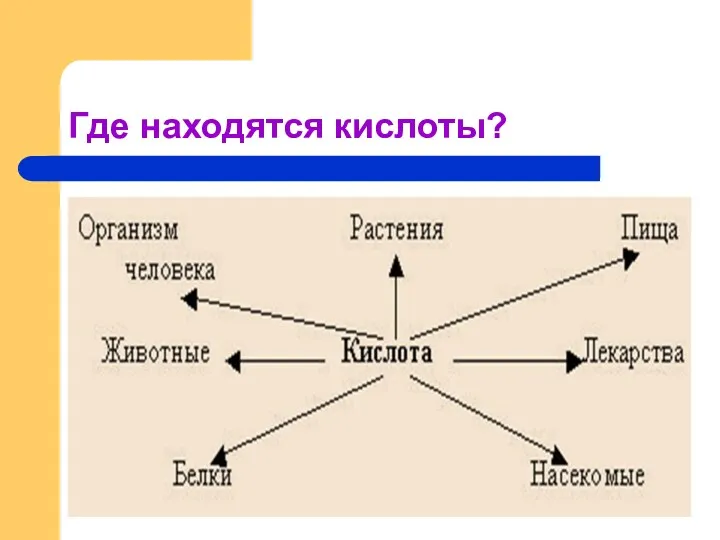
- 6. Где находятся кислоты?
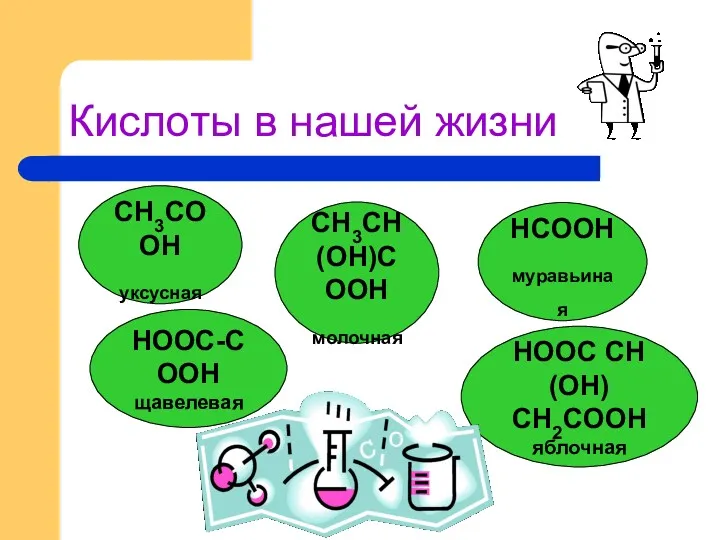
- 7. Кислоты в нашей жизни HCOОH муравьиная НOОС-COОH щавелевая НOОС СН(ОН) СН2COОH яблочная СH3COОH уксусная СH3CH (OH)COОH
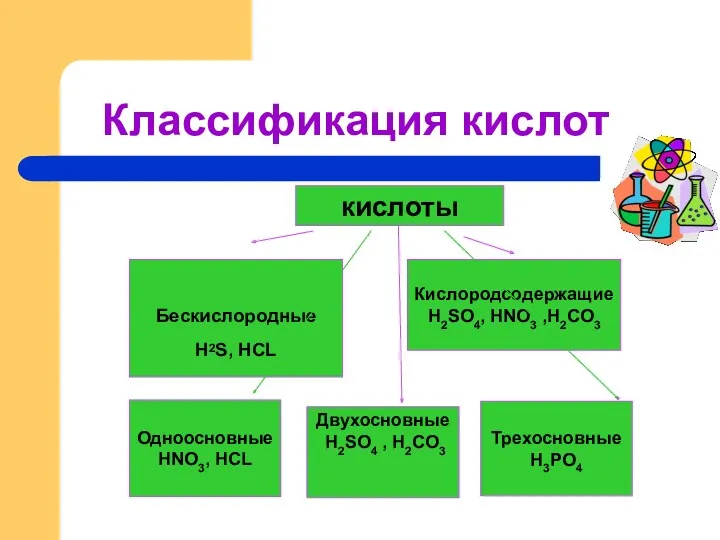
- 8. Классификация кислот
- 9. Получение кислот
- 10. Получение кислот Кислотный оксид +Н2О = Кислота SO3 + Н2О = Н2SO4 Простое вещ-во + Простое
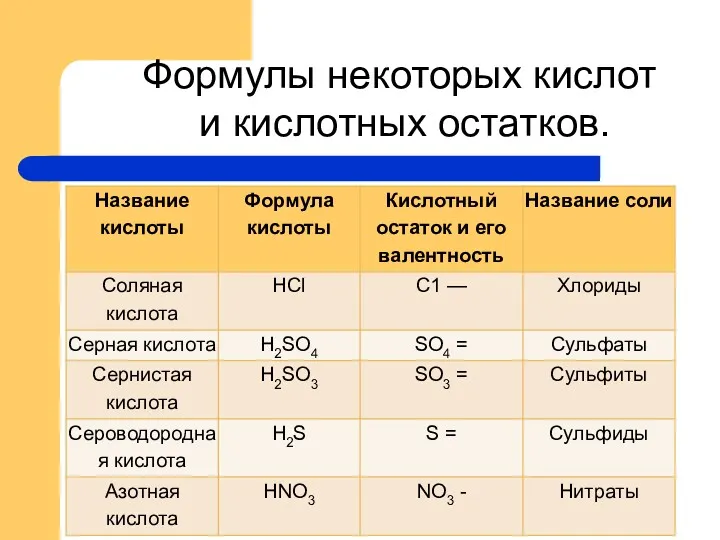
- 11. Формулы некоторых кислот и кислотных остатков.
- 13. Свойства кислот
- 14. Физические свойства кислот а) жидкости (кроме кремниевой кислоты), б) без цвета, в) без запаха, г) кислые
- 15. Практическое определение химических свойств кислот
- 16. Химические свойства кислот Действие индикатора. Взаимодействие с металлами. Взаимодействие с основными оксидами. Взаимодействие с гидроксидами. Взаимодействие
- 17. Домашнее задание §20,стр 76 таблица Кому было легко – упражнение 4,2,5; Кто затруднялся - упражнение1; Кому
- 18. МОЛОДЦЫ!
- 20. Скачать презентацию













 Аммиак
Аммиак Химия p-элементов. VI и VII группы главные подгруппы
Химия p-элементов. VI и VII группы главные подгруппы Биологически активные вещества и их содержание в лекарственных растениях
Биологически активные вещества и их содержание в лекарственных растениях Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Первичная переработка нефти
Первичная переработка нефти Нуклеиновые кислоты
Нуклеиновые кислоты Карбонаты
Карбонаты Спирты: общая характеристика
Спирты: общая характеристика Каликсарены
Каликсарены Кислородсодержащие соединения серы SO2
Кислородсодержащие соединения серы SO2 Политетрафторэтилен
Политетрафторэтилен Термодинамика
Термодинамика Арены. Бензол
Арены. Бензол Откуда берутся кристаллы
Откуда берутся кристаллы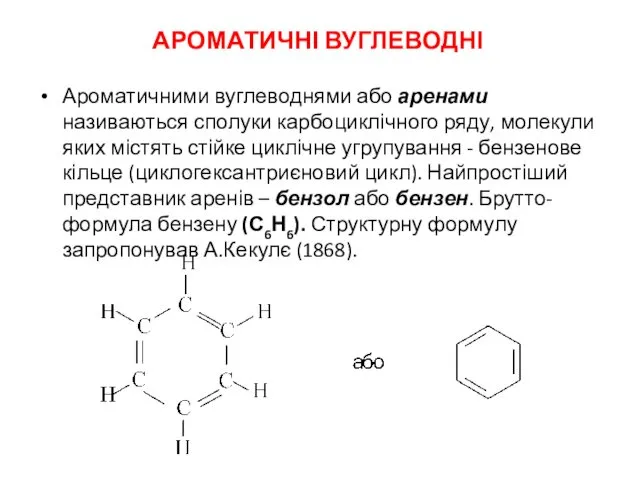 Ароматичні вуглеводні
Ароматичні вуглеводні Разбор заданий
Разбор заданий Облучение. Радиационная окраска
Облучение. Радиационная окраска Кислород
Кислород Окисно-відновні реакції. Процеси окиснення, відновлення, окисник та відновник
Окисно-відновні реакції. Процеси окиснення, відновлення, окисник та відновник Нефть как природный источник углеводородов
Нефть как природный источник углеводородов Етилен і ацетилен – ненасичені вуглеводні
Етилен і ацетилен – ненасичені вуглеводні Массообменные процессы
Массообменные процессы Лекция 3. Разновидности химических связей
Лекция 3. Разновидности химических связей Органічні сполуки. 3D моделі органічних сполук
Органічні сполуки. 3D моделі органічних сполук Соединения железа
Соединения железа Жоғары молекулалық қосылыстар химиясы
Жоғары молекулалық қосылыстар химиясы Растворы. Свойства растворов. (Тема 3)
Растворы. Свойства растворов. (Тема 3) Реакції йонного обміну між електролітами у водних розчинах. Практична робота №1. 9 клас
Реакції йонного обміну між електролітами у водних розчинах. Практична робота №1. 9 клас