Слайд 2

ЧТО ТАКОЕ ОСНОВАНИЯ?
Основания- сложные вещества, состоящие из атома металла, связанного с
одной или несколькими гидроксогруппами -ОН.
Слайд 3

Слайд 4

Общая формула оснований:
Ме(ОН)n, где
Ме - металл
n-число гидроксогрупп и одновременно валентность
металла.
Слайд 5

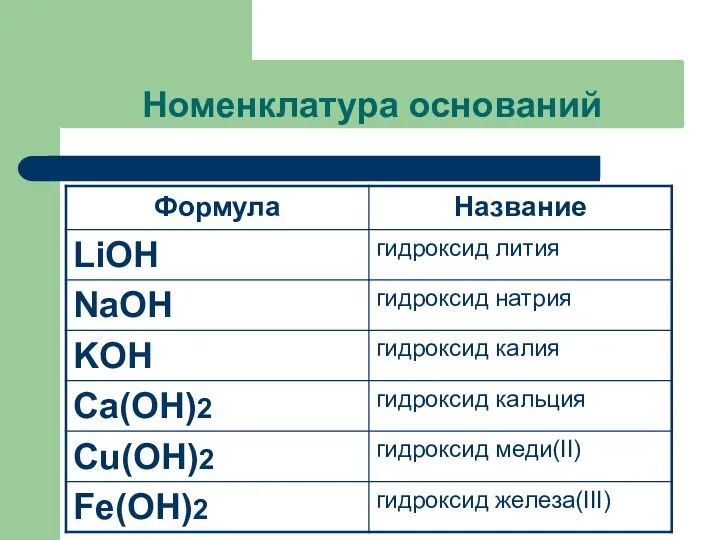
Номенклатура оснований
Название оснований=
Гидроксид + название металла в родительном падеже +
валентность римскими цифрами (переменная)
Слайд 6
Слайд 7

Например:
Fе(ОН)3
Гидроксид железа (ΙΙΙ)
Ва(ОН)2
Гидроксид бария
Слайд 8

Дайте названия гидроксидам:
LiOH
Ba(OH)2
Fe(OH)2
Al(OH)3
NaOH
гидроксид лития
гидроксид бария
гидроксид железа (II)
гидроксид алюминия
гидроксид натрия
Слайд 9
Слайд 10
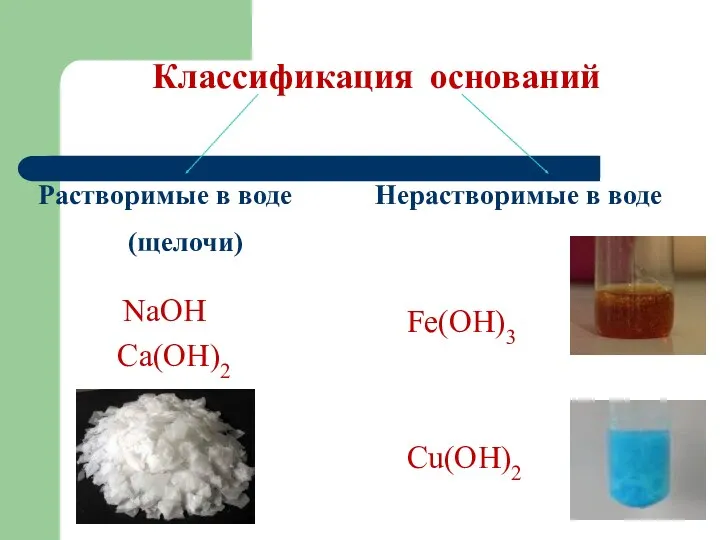
Классификация оснований
Растворимые в воде
(щелочи)
Нерастворимые в воде
NaOH
Ca(OH)2
Fe(OH)3
Сu(OH)2
Слайд 11

Амфотерные гидроксиды
Амфотерность
(от др.греч. амфотеро — «двойственный», «обоюдный») — способность некоторых соединений проявлять как
кислотные, так и основные свойства .
Слайд 12

К амфотерным гидроксидам относятся:
Ве(ОН)2, Zn(ОН)2, Аl(ОН)3, Сr(ОН)3, Sn(ОН)2, Рb(OH)2 , Cu(ОН)2
, Fe(ОН)3 ,
Слайд 13
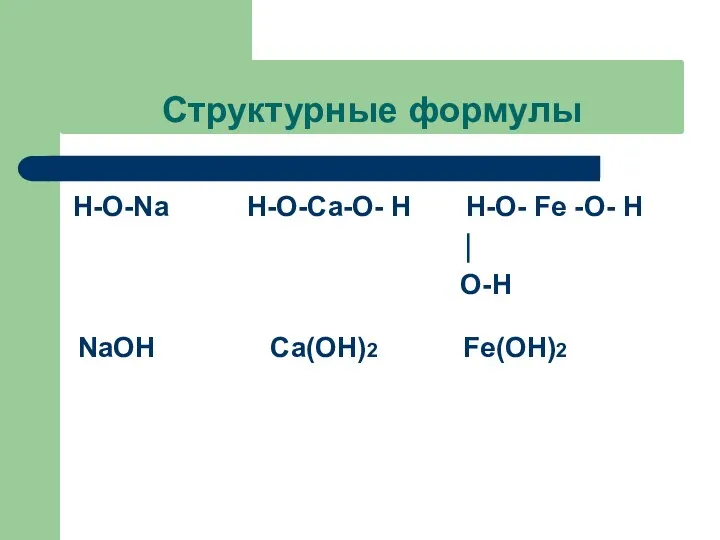
Структурные формулы
Н-О-Na Н-О-Ca-О- Н Н-О- Fe -О- Н
⏐
О-Н
NaOH
Ca(OH)2
Слайд 14

Физические свойства
Основания - твердые кристаллические вещества.
В воде растворимы щелочи:
LiOH , NaOH, KOH, CsOH, RbOH, Ca(OH)2, Sr(OH)2,Ba(OH)2,
другие - малорастворимы.
Слайд 15

Физические свойства
Основания – твердые вещества.
Щелочи растворяются в воде ( к
ним относят основания металлов 1 и 2 а подгрупп, кроме магния и бериллия), мылки на ощупь.
Щелочи очень едкие вещества, могут разъедать ткани и кожу, поэтому обращаться с ними нужно очень осторожно. При попадании на кожу щелочь нейтрализуются слабым раствором уксусной, борной кислот и смывают большим количеством воды.
Слайд 16
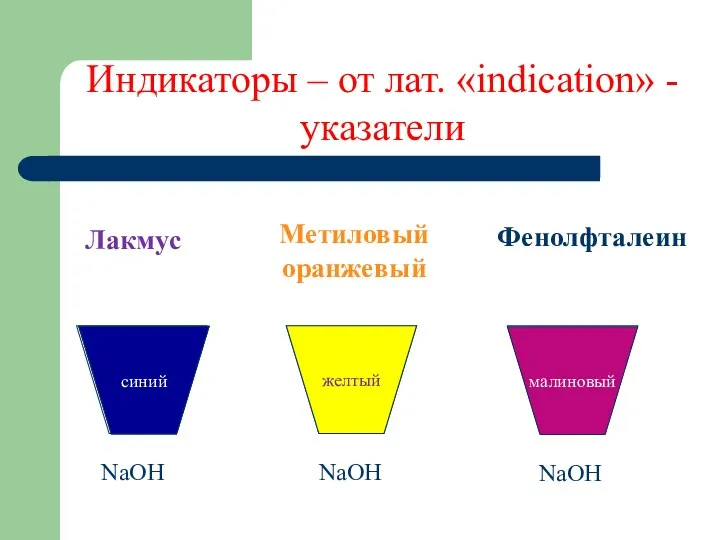
Индикаторы – от лат. «indication» - указатели
NaOH
NaOH
NaOH
Лакмус
Метиловый оранжевый
Фенолфталеин
желтый
малиновый
синий
Слайд 17
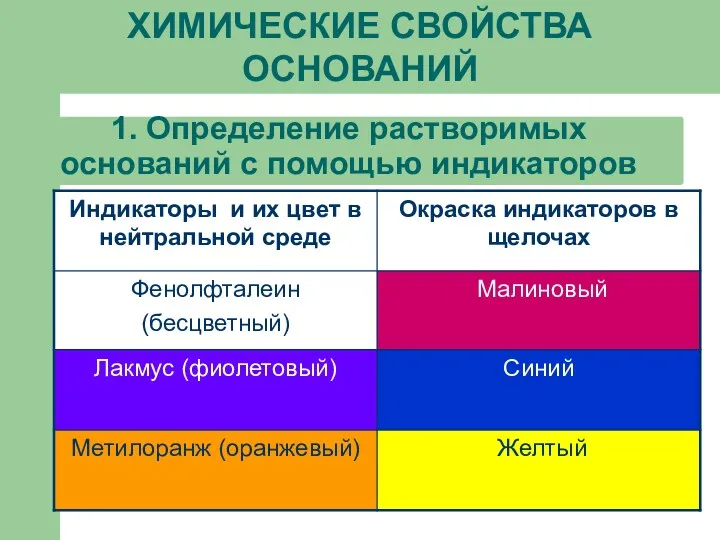
1. Определение растворимых оснований с помощью индикаторов
ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ
Слайд 18

ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ
2.Взаимодействие с кислотами
KOH+HCl=KCl+H2O
Cu(OH)2+2HCl=CuCl2+2H2O
Слайд 19

Взаимодействие с кислотами:
2NaOH + H2SO4 → Na2SO4 + 2H2O
реакция нейтрализации
Слайд 20

Cu(OH)2↓+ H2SO4 → CuSO4 +2 H2O
Слайд 21

ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ
3.Взаимодействие с кислотными оксидами
2KOH+CO2=K2CO3+H2O
Слайд 22

Взаимодействие с кислотными оксидами
Са(ОН)2 + СО2 → СаСО3↓ + Н2О
реакция обмена
Слайд 23

ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ
4.Взаимодействие с амфотерными оксидами
2KOH+ZnO=K2ZnO2+H2O
Слайд 24

ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ
5.Взаимодействие с солями, если образуется малорастворимая соль или малорастворимое
основание
2NaOH+CuCl2=Cu(OH)2 = 2NaCl
Слайд 25
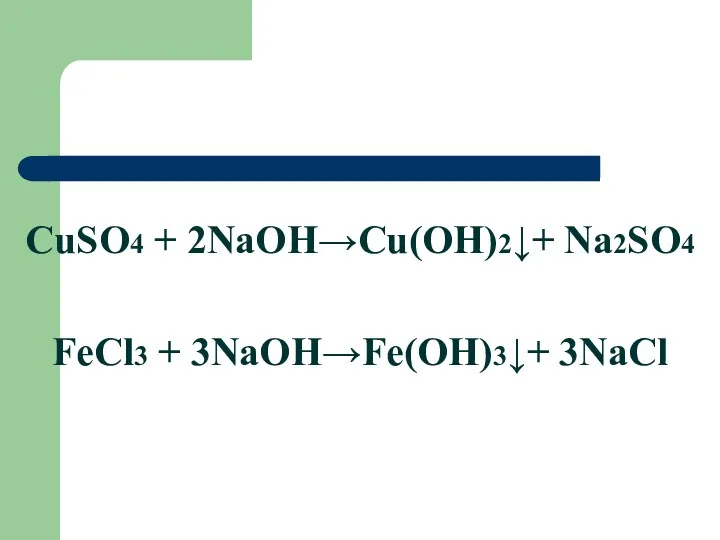
CuSO4 + 2NaOH→Cu(OH)2↓+ Na2SO4
FeCl3 + 3NaOH→Fe(OH)3↓+ 3NaCl
Слайд 26

ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ
6.При нагревании разлагаются
(кроме LiOH):
Cu (OH)2 =
Слайд 27

Отношение оснований к нагреванию
Cu(OH)2 → CuO↓ + H2O
t
Слайд 28

ХИМИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ
7. Амфотерные гидроксиды Al(OH)3, Zn(OH)2, Be(OH)2, Fe(OH)3
и
другие взаимодействуют с кислотами
Zn (OH)2+2HCl=ZnCl2+2H2O
Взаимодействуют с щелочами Al(OH)3+NaOH=Na[Al(OH)4]
Слайд 29

Важнейшие представители и их применение
NaOH, KOH, Ca(OH)2:
твердые, очень едкие вещества,
растворимые в воде, мылкие на ощупь. При попадании на кожу их следует нейтрализовать слабым раствором борной или уксусной кислоты и смыть водой.
NaOH - гидроксид натрия или едкий натр. Используют при производстве мыла, в кожевенной и фармацевтической промышленности.
KOH - гидроксид калия или едкое кали. Применяют при производстве жидкого мыла, стекла.
Ca(OH)2 - гидроксид кальция или гашеная известь. Немного растворимо в воде. Прозрачный раствор гидроксида кальция называется известковой водой. Ее используют для обнаружения углекислого газа (при пропускании СО2 известковая вода мутнеет, т.к. образуется нерастворимый карбонат кальция) Гидроксид кальция применяется в строительстве, для побелки, получения дезинфицирующего средства (хлорной извести)
Слайд 30

Щелочи в быту
Гидроксид натрия, техническое название едкий натр или каустическая
сода. Едкий натр кристаллическое вещество белого или желтоватого цвета, изготавливают в промышленности в виде гранул. Обладает сильнейшим моющим действием, хорошо растворяет жиры. Используется очистки масляных пятен с различных изделий, для прочистки от жировых отложений в канализационных трубах.
Гидроксид кальция, техническое название -гашеная известь. Используется в строительстве для штукатурки стен внутри помещений, для побелки стен бытового и технического назначения.
Раствор аммиака (нашатырный спирт)-жидкость с раздражающим слизистые оболочки носа и глаз запахом. В быту используется 25% раствор. Применяется для стирки шерстяных изделий, для удаления пятен органического происхождения: молока, смол, жиров. Находит широкое применение в средствах для мытья стекол. Обладая хорошим моющим действием нашатырный спирт не оставляет разводов на поверхности. Раствор аммиака можно использовать для очистки изделий из золота и серебра, опуская их в нагретый раствор. Аммиак образует с металлами растворимые в воде соединения.
.
Слайд 31

ЗАГАДКА
Я растворчик изучал.
Лакмус в нем синее стал.
Поглощал раствор тотчас
Кислый углекислый газ!
Про
такой раствор я знаю,
Что среда в нем …
Слайд 32

ОТВЕТ:
Я растворчик изучал.
Лакмус в нем синее стал.
Поглощал раствор тотчас
Кислый углекислый газ!
Про
такой раствор я знаю,
Что среда в нем …
(Щелочная)
Слайд 33

ЗАГАДКА
Капля воды попала на кусок и превратилась в кипяток.
Слайд 34

ОТВЕТ:
Капля воды попала на кусок и превратилась в кипяток.
(Вода и щелочи)
Слайд 35

Слайд 36

Задание
Не является щёлочью :
1)NaOH;
2)Ca(OH)2;
3)Mg(OH)2;
4)KOH.
Слайд 37
Домашнее задание:
Выучить §19 , №4(письменно)




































 Комплексные соединения. Природа химической связи: метод молекулярных орбиталей
Комплексные соединения. Природа химической связи: метод молекулярных орбиталей Классификация химических реакций. 8 класс
Классификация химических реакций. 8 класс Хімічні властивості алкенів
Хімічні властивості алкенів Молярный объем газов
Молярный объем газов Сероводород, Сульфиды. Оксид серы (IV). Сернистая кислота
Сероводород, Сульфиды. Оксид серы (IV). Сернистая кислота Разноцветные кристаллы
Разноцветные кристаллы Строение атома. Планетарная модель Резерфорда
Строение атома. Планетарная модель Резерфорда Электрохимическая защита
Электрохимическая защита Азот и фосфор
Азот и фосфор Структура нуклеїнових кислот
Структура нуклеїнових кислот Нуклеофильное замещение галогена и других функциональных групп
Нуклеофильное замещение галогена и других функциональных групп Задачи на электролиз. 11 класс
Задачи на электролиз. 11 класс Карбонильные соединения. Альдегиды и кетоны
Карбонильные соединения. Альдегиды и кетоны Производные хинолина и хинуклидина, производные 4-замещенных хинолина
Производные хинолина и хинуклидина, производные 4-замещенных хинолина Химический элемент алюминий
Химический элемент алюминий Основания как электролиты, их классификация по различным признакам. Химические свойства оснований
Основания как электролиты, их классификация по различным признакам. Химические свойства оснований Реакция карамелизации
Реакция карамелизации Пластические массы и изделия на их основе
Пластические массы и изделия на их основе Классификация химических реакций
Классификация химических реакций Суспензии: получение, свойства
Суспензии: получение, свойства Химическая посуда и ее значение (1)
Химическая посуда и ее значение (1) Валентность и степень окисления 8 класс
Валентность и степень окисления 8 класс Аминокислоты 2
Аминокислоты 2 Предмет химии. Вещества
Предмет химии. Вещества Гетероциклические соединения природного и синтетического происхождения. Производные фурана и бензофурана. (Лекция 1-2)
Гетероциклические соединения природного и синтетического происхождения. Производные фурана и бензофурана. (Лекция 1-2) Интегрированный урок по химии и немецкому языку “Anwendung Hydrolyse von Wasser”
Интегрированный урок по химии и немецкому языку “Anwendung Hydrolyse von Wasser” Химические свойства воды
Химические свойства воды Галогены VII группа
Галогены VII группа