Содержание
- 2. Основания – это сложные вещества, состоящие из ионов металлов и связанных с ними гидроксид-анионов. Met (OH)
- 3. Заряд гидроксид-иона равен ОН Количество гидроксид-ионов определяется зарядом иона металла, образующего основание. Например: 1- 1+ 2+
- 4. Название оснований Гидроксид + Название металла в родительном падеже + Степень окисления римскими цифрами
- 5. Примеры оснований NaOH Ca(OH)2 Fe(OH)2 Fe(OH)3 Al(OH)3 Гидроксид натрия Гидроксид железа (II) Гидроксид кальция Гидроксид алюминия
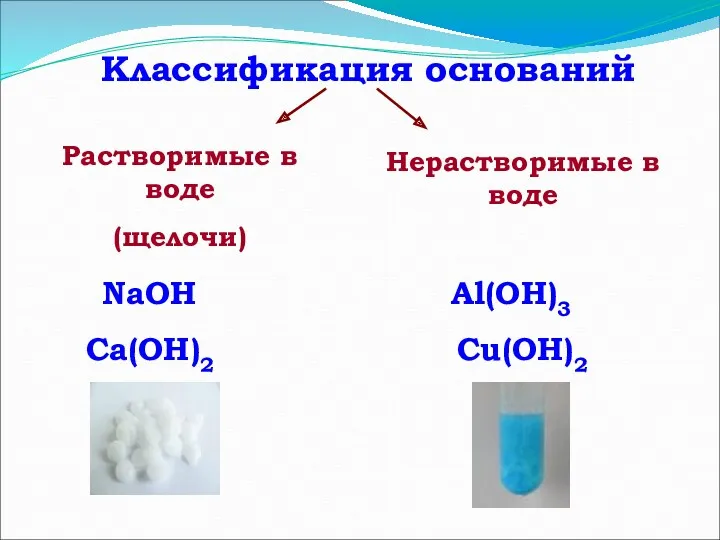
- 6. Классификация оснований Растворимые в воде (щелочи) Нерастворимые в воде NaOH Ca(OH)2 Al(OH)3 Сu(OH)2
- 7. Щелочи получают взаимодействием активных металлов с водой. К активным (т.е. щелочным металлам относятся Li, Na, K,
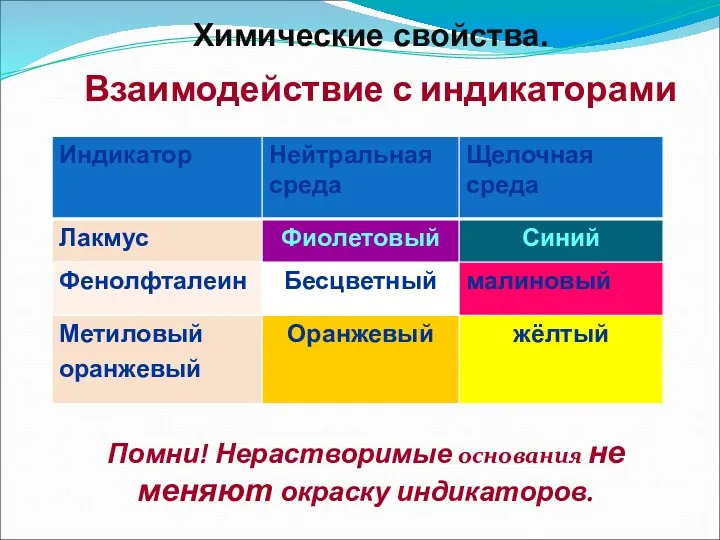
- 8. Взаимодействие с индикаторами Помни! Нерастворимые основания не меняют окраску индикаторов. Химические свойства.
- 9. Щёлочь + оксид неметалла → соль + вода ( реакция обмена) УСЛОВИЕ: оксиду неметалла должна соответствовать
- 10. Щелочь + соль → новое основание + новая соль ( реакция обмена) 3NaOH+FeCl3→Fe(OH)3↓+ 3NaCl Условия протекания
- 11. Основание + кислота → соль + вода (реакция обмена, нейтрализации) Растворимые основания: NaOH + HCl →
- 12. Нерастворимое основание →оксид металла + вода (разложение при нагревании) Mg(OH)2 → MgO + H2O 2Fe(OH)3 →
- 14. Скачать презентацию









 Гетероциклдық қосылыстардың туындылары
Гетероциклдық қосылыстардың туындылары Классы неорганических соединений. 8 класс
Классы неорганических соединений. 8 класс Figure
Figure Методы выращивания монокристаллов кремния. Сравнение. Сферы применения монокристаллов, выращенных различными методами
Методы выращивания монокристаллов кремния. Сравнение. Сферы применения монокристаллов, выращенных различными методами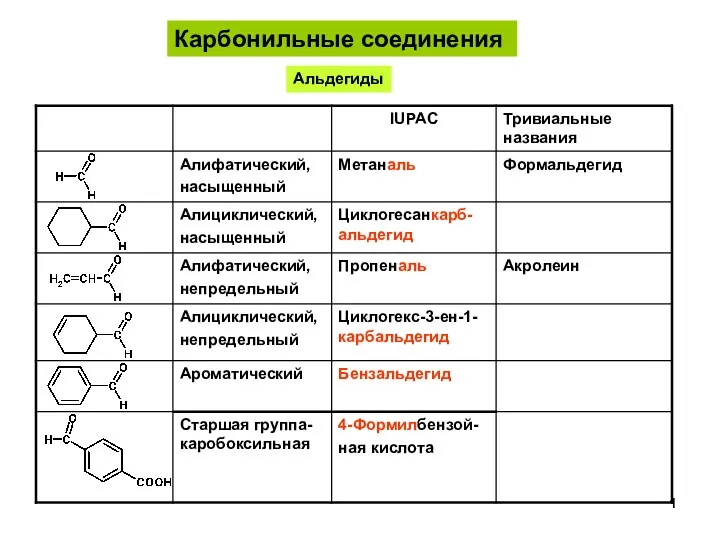 АльдегидыКетоны-1
АльдегидыКетоны-1 Серная кислота и её свойства
Серная кислота и её свойства Жиры. Сложные эфиры глицерина и высших карбоновых кислот
Жиры. Сложные эфиры глицерина и высших карбоновых кислот Типы химических реакций
Типы химических реакций Соли. CaSO4 - Сульфат кальция
Соли. CaSO4 - Сульфат кальция Каменный уголь
Каменный уголь Механизмы органических реакций
Механизмы органических реакций ПОЛИСАХАРИДЫ
ПОЛИСАХАРИДЫ Химическая посуда и ее назначение (4)
Химическая посуда и ее назначение (4) Обобщающий урок по теме: Металлы
Обобщающий урок по теме: Металлы Электролитическая диссоциация. 9 класс
Электролитическая диссоциация. 9 класс Химическое равновесие. Азот и Фосфор. 9 класс
Химическое равновесие. Азот и Фосфор. 9 класс Кристаллические решетки
Кристаллические решетки Химия нефти и газа. Свойства нефти и нефтепродуктов. Свойства газов
Химия нефти и газа. Свойства нефти и нефтепродуктов. Свойства газов D-элементы VII-В группы. Марганец
D-элементы VII-В группы. Марганец Гидродинамические свойства полимеров. Полиэлектролиты
Гидродинамические свойства полимеров. Полиэлектролиты Изомеры – это вещества, имеющие одинаковый состав
Изомеры – это вещества, имеющие одинаковый состав Классы неорганических веществ
Классы неорганических веществ Залізо. Фізичні та хімічні властивості
Залізо. Фізичні та хімічні властивості Электрофильное замещение в ароматических соединениях, SE
Электрофильное замещение в ароматических соединениях, SE Вещества и физические тела
Вещества и физические тела Сложные эфиры
Сложные эфиры Тірі ағзада жүретін процесстер – физика-химиялық интерпретация
Тірі ағзада жүретін процесстер – физика-химиялық интерпретация Амфотерные оксиды и гидроксиды
Амфотерные оксиды и гидроксиды