Содержание
- 2. План урока: 1. Дать характеристику алюминия по его положению в периодической системе химических элементов. 2. На
- 3. «Серебро из глины» Немецкий учёный Ф. Велер (1827 г.) получил алюминий при нагревании хлорида алюминия со
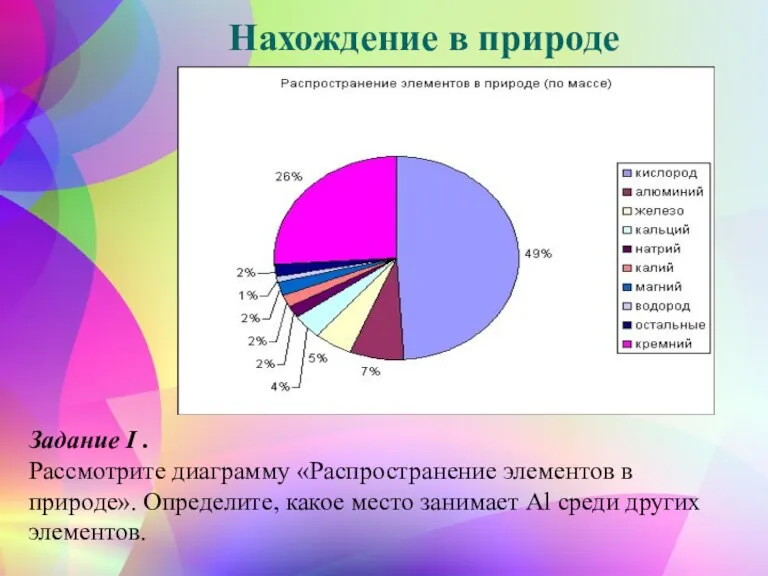
- 4. Нахождение в природе Задание I . Рассмотрите диаграмму «Распространение элементов в природе». Определите, какое место занимает
- 5. Нефелины — KNa3[AlSiO4]4 Глинозёмы (смеси каолинов с песком SiO2, известняком CaCO3, магнезитом MgCO3) Корунд (сапфир, рубин,
- 6. Строение атома алюминия Al 27 +13 0 2 8 3 P = 13 e = 13
- 7. Периодическая система химических элементов Д.И.Менделеева Периоды 1 2 3 4 5 6 7 Ряды 1 2
- 8. Неметаллами Кислородом Щелочами Водой Кислотами Оксидами металлов Алюминий восстанавливает все элементы, находящиеся справа от него в
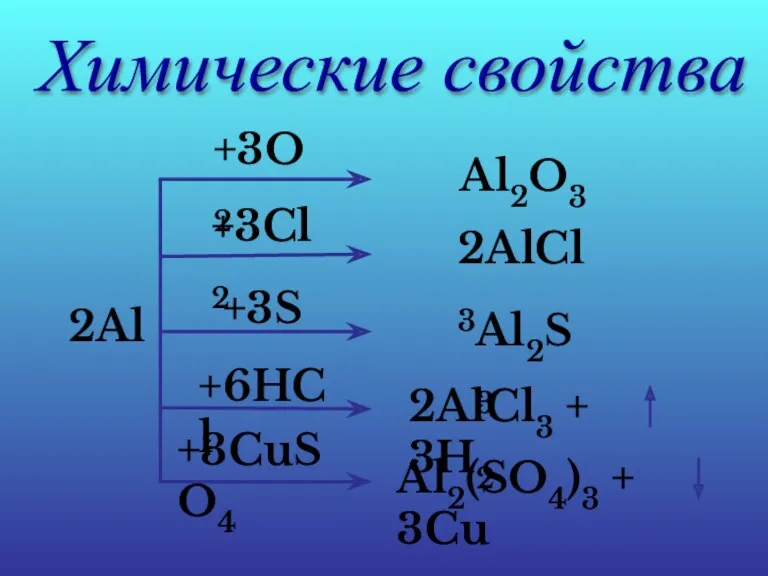
- 9. Химические свойства 2Al +3O2 Al2O3 +3Cl2 2AlCl3 +3S Al2S3 +6HCl 2AlCl3 + 3H2 +3CuSO4 Al2(SO4)3 +
- 10. 2Al + 2NaOH + 6H2O = 2Na[Al(OH)4] + 3H2 Взаимодействие со щелочами Задание 2 Напишите уравнения
- 11. Применение алюминия Al
- 12. Алюминий – металл будущего ? Задание 4 Ответьте на вопрос: « Почему алюминий называют металлом будущего?»
- 14. Скачать презентацию


![Нефелины — KNa3[AlSiO4]4 Глинозёмы (смеси каолинов с песком SiO2, известняком](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/436495/slide-4.jpg)



![2Al + 2NaOH + 6H2O = 2Na[Al(OH)4] + 3H2 Взаимодействие](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/436495/slide-9.jpg)


 Одноосновные ненасыщенные кислоты
Одноосновные ненасыщенные кислоты Белки. Определение
Белки. Определение Циклоалканы. Строение циклоалканов
Циклоалканы. Строение циклоалканов Молекулярные свойства жидкостей
Молекулярные свойства жидкостей Биофизические основы патологии клетки. Свободные радикалы и болезни человека
Биофизические основы патологии клетки. Свободные радикалы и болезни человека Общая характеристика элементов VA -группы. Азот, распространение, физические и химические свойства. Круговорот в природе
Общая характеристика элементов VA -группы. Азот, распространение, физические и химические свойства. Круговорот в природе Качественные реакции на анионы
Качественные реакции на анионы Токсикология пестицидов
Токсикология пестицидов Маңызды химиялық өндірістер
Маңызды химиялық өндірістер Серная кислота. 9 класс
Серная кислота. 9 класс Физические свойства минералов
Физические свойства минералов Анионы. Группы анионов
Анионы. Группы анионов Азотсодержащие соединения. Амины. Аминокислоты
Азотсодержащие соединения. Амины. Аминокислоты Щелочные металлы
Щелочные металлы Алюминий и его соединения
Алюминий и его соединения Электрохимическая система
Электрохимическая система Сполуки неметалічних елементів з Гідрогеном. Особливості водних розчинів цих сполук, їх застосування
Сполуки неметалічних елементів з Гідрогеном. Особливості водних розчинів цих сполук, їх застосування Реакции ионного обмена
Реакции ионного обмена Углерод. Аллотропные состояния углерода
Углерод. Аллотропные состояния углерода Карбоновые кислоты
Карбоновые кислоты Основні властивості металів. Хімія металургійних процесів. Теорія сплавів. Корозія металів
Основні властивості металів. Хімія металургійних процесів. Теорія сплавів. Корозія металів Строение и химические свойства кислот
Строение и химические свойства кислот Химия 20 века
Химия 20 века Перегонка с водяным паром
Перегонка с водяным паром Закон збереження маси речовини. Хімічні рівняння
Закон збереження маси речовини. Хімічні рівняння Горение топлива
Горение топлива Типы химических реакций в органической химии
Типы химических реакций в органической химии История развитии химии
История развитии химии