Простые вещества. Аллотропия. Классификация простых веществ. Бинарные соединения. Оксиды презентация
Содержание
- 2. 1. Простые вещества 1.1. Аллотропия 1.2. Классификация простых веществ 2. Бинарные соединения 3. Оксиды 3.1. Основные
- 3. Простые вещества — химические вещества, состоящие исключительно из атомов одного химического элемента. Примеры: О2, С, Al,
- 4. 1.1. Аллотропия Рис.1. Аллотропные формы углерода: графит, алмаз, фуллерен Аллотропия— это процесс, при котором один химический
- 5. 1.2. Классификация простых веществ
- 6. Бинарные соединения — это собирательная группа веществ, которые имеют различное химическое строение, но состоят из двух
- 7. 3. Оксиды
- 8. Основными называют оксиды, которые реагируют с кислотами, образуя соль и воду. Основные оксиды образуются химическими элементами
- 9. 1. Основные оксиды образуются типичными металлами, а также металлами переменной валентности в низшей степени окисления (например,
- 10. 3. С водой реагируют только оксиды щелочных и щелочно-земельных металлов: BaO (основной оксид)+H2O (вода)=Ba(OH)2 (основание щелочнозем.
- 11. Кислотными называют оксиды, которые реагируют с основаниями, образуя соль и воду. Кислотные оксиды образуют элементы —
- 12. 1. Кислотные оксиды вступают в реакцию с водой, в результате с которой образуют кислоты: CO2 +H2
- 13. 3. Также кислотные оксиды взаимодействуют с основаниями, в результате чего образуются соли: SO3 (кислотный оксид)+2NaOH (основание)=Na2
- 14. Амфотерными называют оксиды, которые реагируют как с кислотами, так и с основаниями, образуя соли. Амфотерные свойства
- 15. 1. Амфотерные оксиды взаимодействуют с кислотами и кислотными оксидами. При этом амфотерные оксиды взаимодействуют, как правило,
- 16. Пероксиды или перекиси — сложные вещества, в которых атомы кислорода соединены друг с другом. Пероксиды —
- 17. Кислота – это сложное вещество, в молекуле которого имеется один или несколько атомов водорода и кислотный
- 18. По количеству атомов водорода, способных замещаться на металл, все кислоты делятся на одноосновные (с одним атомом
- 19. Названия бескислородных кислот образуются от названия элемента с суффиксом -о и прибавлением слов «водородная кислота»: HF
- 20. 1.Водные растворы кислот изменяют окраску индикаторов. В кислой среде фиолетовый лакмус, метилоранж и универсальный индикатор становятся
- 21. 5. Взаимодействие кислот с солями. А) Кислоты реагируют с растворами солей, если в результате реакции один
- 22. 7. Взаимодействие с металлами. Азотная и концентрированная серная кислоты являются сильными окислителями и могут взаимодействовать с
- 23. Основания - это сложные вещества, состоящие из атома металла, связанного с одной или несколькими гидроксильными группами
- 24. Классификация оснований по числу групп ОН: 5.1. Номенклатура оснований: Названия оснований состоят из слова «гидроксид» и
- 25. 1. Неорганические основания способны реагировать с кислотами с образованием соли и воды, причем, нерастворимые в воде
- 26. 4. Щелочей также способны вступать в реакции взаимодействия (ОВР) с некоторыми неметаллами: 2NaOH + Si +
- 27. Солями называются вещества, в которых атомы металла связаны с кислотными остатками. Исключением являются соли аммония, в
- 28. Средние соли содержат только атомы металла и кислотного остатка. Например: Ca(NO3)2нитрат кальция PbSO4 сульфат свинца Кислые
- 30. Скачать презентацию



























 Классификация химических элементов
Классификация химических элементов Азотная кислота. Соли азотной кислоты. Получение и применение (9 класс)
Азотная кислота. Соли азотной кислоты. Получение и применение (9 класс) Алкины. Непредельные углеводороды
Алкины. Непредельные углеводороды Характеристика химического элемента по кислотно-основным свойствам образуемых им соединений. Амфотерные оксиды и гидроксиды
Характеристика химического элемента по кислотно-основным свойствам образуемых им соединений. Амфотерные оксиды и гидроксиды Химические элементы в организме человека
Химические элементы в организме человека Обратимость химических реакций. Химическое равновесие и способы его смещения
Обратимость химических реакций. Химическое равновесие и способы его смещения Непредельные углеводороды
Непредельные углеводороды Химические свойства получение и применение солей
Химические свойства получение и применение солей Роль хімії в природі
Роль хімії в природі Кислоты. Состав и классификация кислот. Формулы и названия основных неорганических кислот
Кислоты. Состав и классификация кислот. Формулы и названия основных неорганических кислот Кислотно-основные равновесия. Введение в титриметрию
Кислотно-основные равновесия. Введение в титриметрию Фтор (Fluorum), F
Фтор (Fluorum), F Опасности среды обитания человека
Опасности среды обитания человека Строение атома. Химическая связь
Строение атома. Химическая связь Скорость химических реакций. Факторы, влияющие на скорость химической реакции
Скорость химических реакций. Факторы, влияющие на скорость химической реакции Факторы и процессы формирования химического состава подземных вод
Факторы и процессы формирования химического состава подземных вод Лекция Атомное строение твердых тел. 1-01
Лекция Атомное строение твердых тел. 1-01 Геохимия метасоматтческого процесса. (Лекция 7)
Геохимия метасоматтческого процесса. (Лекция 7) Соединения химических элементов. Валентность и степень окисления элементов
Соединения химических элементов. Валентность и степень окисления элементов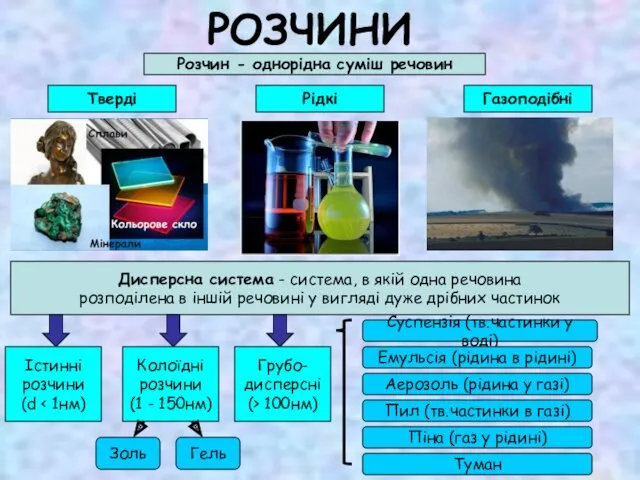 Розчини
Розчини Открытие периодического закона
Открытие периодического закона Азотсодержащие соединения. Амины. Аминокислоты
Азотсодержащие соединения. Амины. Аминокислоты Основные характеристики различных сортов меда
Основные характеристики различных сортов меда Тыңайтқышты тиімді пайдалансақ
Тыңайтқышты тиімді пайдалансақ Волшебные кристалы
Волшебные кристалы М.В.Ломоносов о пользе стекла
М.В.Ломоносов о пользе стекла Взаимодействия кислорода с металлом
Взаимодействия кислорода с металлом Электоролиз заңы
Электоролиз заңы