Содержание
- 2. Физическая теория Растворы – однородные смеси, состоящие из двух или более веществ. Растворение – это диффузия.
- 3. Химическая теория В 1887 году доказал, что растворение является результатом химического взаимодействия растворенного вещества с молекулами
- 4. 1. В процессе растворения некоторые вещества меняют цвет. Безводный сульфат меди CuSO4 белого цвета (слева) при
- 5. 2. В процессе растворения может поглощаться и выделяться энергия. При растворении нитрата аммония стаканчик примерзает к
- 6. 3. В процессе растворения может уменьшаться объем раствора по сравнению с суммой объема исходных компонентов. Например
- 7. Физико-химическая теория растворов Раство́р — гомогенная (однородная) система, состоящая из растворителя, растворенных веществ и продуктов их
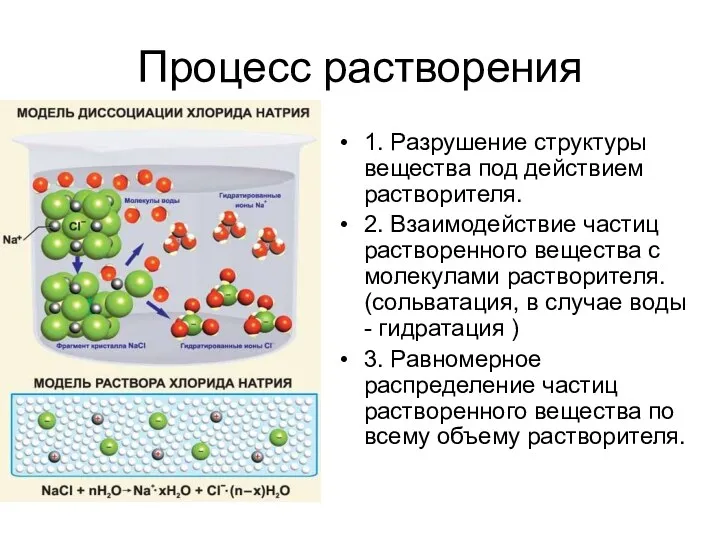
- 8. Процесс растворения 1. Разрушение структуры вещества под действием растворителя. 2. Взаимодействие частиц растворенного вещества с молекулами
- 9. Растворы по агрегатному состоянию могут быть 1. газообразными 2. жидкими: в жидкости – газ в жидкости
- 10. Газообразные растворы раствор кислорода и углекислого газа в азоте – воздух
- 11. Жидкие растворы 3.в жидкости – твердое вещество 1. в жидкости – газ 2. в жидкости –
- 12. Твердые растворы 1. Сплавы металлов, амальгамы Растворы газов в металле Изделия из медно-никелевого сплава Сплав из
- 13. Растворитель 1. Растворителем считают то вещество, агрегатное состояние которого при образовании раствора не изменяется 2. Если
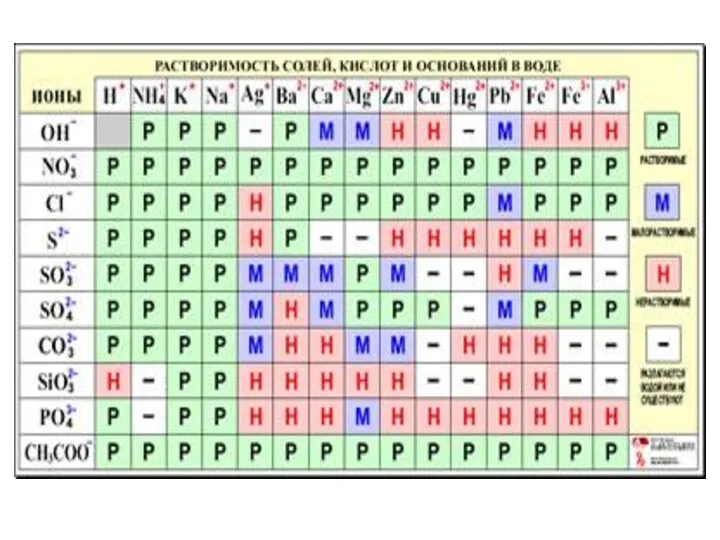
- 14. Растворимость Это способность веществ разрушаться до структурных единиц под действием растворителя. Растворимость зависит от: природы вещества,
- 16. Растворы Коэффициент растворимости показывает сколько граммов вещества может растворяться в 100 г растворителя. В соответствии с
- 17. Насыщенный раствор — раствор — раствор, в котором растворённое вещество при данных условиях больше не растворяется.
- 18. Ненасыщенный раствор — раствор, в котором при данных условиях можно растворить еще некоторое количество растворенного вещества.
- 19. Пересыщенный раствор — раствор, содержащий при данных условиях больше растворённого вещества, чем в насыщенном растворе, избыток
- 21. Скачать презентацию
















 Александр Евгеньевич Ферсман
Александр Евгеньевич Ферсман Кислород и озон
Кислород и озон Алкандар. Метан және оның құрылысы
Алкандар. Метан және оның құрылысы Соли аммония
Соли аммония Химические свойства алканов
Химические свойства алканов Свободное окисление и токсические формы кислорода
Свободное окисление и токсические формы кислорода Формирование ключевых и предметных компетенций учащихся при изучении темы “Металлы”
Формирование ключевых и предметных компетенций учащихся при изучении темы “Металлы” Углерод. Оксиды углерода
Углерод. Оксиды углерода Применение соляной кислоты и её солей
Применение соляной кислоты и её солей Антибиотики как ЛС
Антибиотики как ЛС Соли. CaSO4 - Сульфат кальция
Соли. CaSO4 - Сульфат кальция Class micro and macro elements
Class micro and macro elements Строение атома. Периодический закон Менделеева
Строение атома. Периодический закон Менделеева Простые вещества – неметаллы
Простые вещества – неметаллы Вычисление массовой доли растворенного вещества. 8 класс
Вычисление массовой доли растворенного вещества. 8 класс Цинк в функциональных пищевых и кормовых продуктах
Цинк в функциональных пищевых и кормовых продуктах Ювелирное дело. Империя самоцветов
Ювелирное дело. Империя самоцветов Ферменты в биотехнологии
Ферменты в биотехнологии Строение вещества и агрегатные состояния вещества
Строение вещества и агрегатные состояния вещества Мило та миловаріння
Мило та миловаріння Почему мыло пенится
Почему мыло пенится Основные классы неорганических соединений
Основные классы неорганических соединений Тренувальні вправи. Задачі
Тренувальні вправи. Задачі Період як особлива синтаксична конструкція
Період як особлива синтаксична конструкція Кислородсодержащие органические соединения. Лабораторная работа
Кислородсодержащие органические соединения. Лабораторная работа Химия элементов. Общая характеристика элементов
Химия элементов. Общая характеристика элементов Вклад М.В. Ломоносова в развитие химии
Вклад М.В. Ломоносова в развитие химии Узагальнення знань з теми Вуглеводні
Узагальнення знань з теми Вуглеводні