Слайд 2

Спирты – производные углеводородов, содержащие функциональную группу –ОН(гидроксил). Спирты, в которых
имеется одна группа ОН, называются одноатомными, а спирты с несколькими группами ОН – многоатомными.
Слайд 3

Строение.
По строению различают спирты первичные, вторичные и третичные в зависимости от
того, при каком атоме углерода группа ОН:
Первичный: СН3-СН2-СН2-ОН ПРОПАНОЛ-1
ВТОРИЧНЫЙ: СН3-СН(ОН)-СН3 ПРОПАНОЛ-2
ТРЕТИЧНЫЙ: СН3-С(СН3)(ОН)-СН3 2-МЕТИЛПРОПАНОЛ-2
Слайд 4

Физические свойства одноатомных спиртов.
Одноатомные спирты – бесцветные жидкости (до С12Н25ОН), растворимые
в воде. Простейший спирт – метанол СН3ОН чрезвычайно ядовит. С увеличением молярной массы температура кипения спиртов повышается.
Слайд 5

Химические свойства одноатомных спиртов.
Водород группы ОН в спиртах может замещаться на
металл.
Этанолы и производные других спиртов(алкоголяты)легко гидролизуются.
Группу ОН можно заменить на Cl илиBr.
При действии водоотнимающих средств, например концентрированной Н2SO4, происходит межмолекулярная дегидратация.
Слайд 6

Физические свойства многоатомных спиртов.
Простейшие представители двух- и трехатомных спиртов – этандиол-1,2(этиленгликоль)
и пропантриол-1,2,3(глицерин).При комнатной температуре – бесцветные вязкие жидкости, неограниченно растворимые в воде. Этиленгликоль ядовит.
Слайд 7

Химические свойства многоатомных спиртов.
Кислотные свойства многоатомных спиртов проявляются в том, что
водород группы ОН замещается на металл под действием не только металлов, но и гидроксидов металлов.
Слайд 8

Получение спиртов.
В промышленности – гидратация алкенов в присутствии катализаторов(Н2SO4,Al2О3).
В лаборатории- при
взаимодействии галогенпроизводных углеводородов с водой или водным раствором щелочи при нагревании.
Слайд 9

Применение спиртов.
Спирты используются как сырье в органическом синтезе, в качестве растворителей
(для лаков, красок и т.п.),а также в бумажной, полиграфической, парфюмерной, фармакологической и пищевой промышленности.
Слайд 10

Названия некоторых распространенных спиртов









 Комплексные соединения. Природа химической связи: метод молекулярных орбиталей
Комплексные соединения. Природа химической связи: метод молекулярных орбиталей Классификация химических реакций. 8 класс
Классификация химических реакций. 8 класс Хімічні властивості алкенів
Хімічні властивості алкенів Молярный объем газов
Молярный объем газов Сероводород, Сульфиды. Оксид серы (IV). Сернистая кислота
Сероводород, Сульфиды. Оксид серы (IV). Сернистая кислота Разноцветные кристаллы
Разноцветные кристаллы Строение атома. Планетарная модель Резерфорда
Строение атома. Планетарная модель Резерфорда Электрохимическая защита
Электрохимическая защита Азот и фосфор
Азот и фосфор Структура нуклеїнових кислот
Структура нуклеїнових кислот Нуклеофильное замещение галогена и других функциональных групп
Нуклеофильное замещение галогена и других функциональных групп Задачи на электролиз. 11 класс
Задачи на электролиз. 11 класс Карбонильные соединения. Альдегиды и кетоны
Карбонильные соединения. Альдегиды и кетоны Производные хинолина и хинуклидина, производные 4-замещенных хинолина
Производные хинолина и хинуклидина, производные 4-замещенных хинолина Химический элемент алюминий
Химический элемент алюминий Основания как электролиты, их классификация по различным признакам. Химические свойства оснований
Основания как электролиты, их классификация по различным признакам. Химические свойства оснований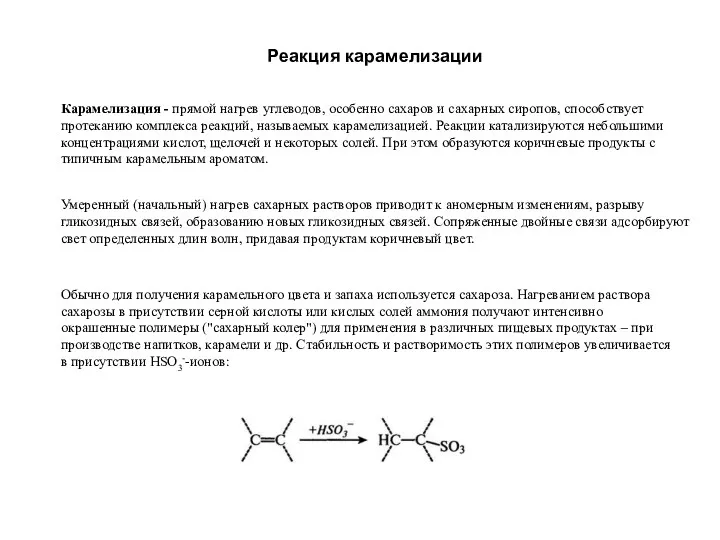 Реакция карамелизации
Реакция карамелизации Пластические массы и изделия на их основе
Пластические массы и изделия на их основе Классификация химических реакций
Классификация химических реакций Суспензии: получение, свойства
Суспензии: получение, свойства Химическая посуда и ее значение (1)
Химическая посуда и ее значение (1) Валентность и степень окисления 8 класс
Валентность и степень окисления 8 класс Аминокислоты 2
Аминокислоты 2 Предмет химии. Вещества
Предмет химии. Вещества Гетероциклические соединения природного и синтетического происхождения. Производные фурана и бензофурана. (Лекция 1-2)
Гетероциклические соединения природного и синтетического происхождения. Производные фурана и бензофурана. (Лекция 1-2) Интегрированный урок по химии и немецкому языку “Anwendung Hydrolyse von Wasser”
Интегрированный урок по химии и немецкому языку “Anwendung Hydrolyse von Wasser” Химические свойства воды
Химические свойства воды Галогены VII группа
Галогены VII группа