Содержание
- 2. АРЕНЫ (ароматические углеводороды) соединения, молекулы которых содержат устойчивые циклические группы атомов (бензольные ядра) с особым характером
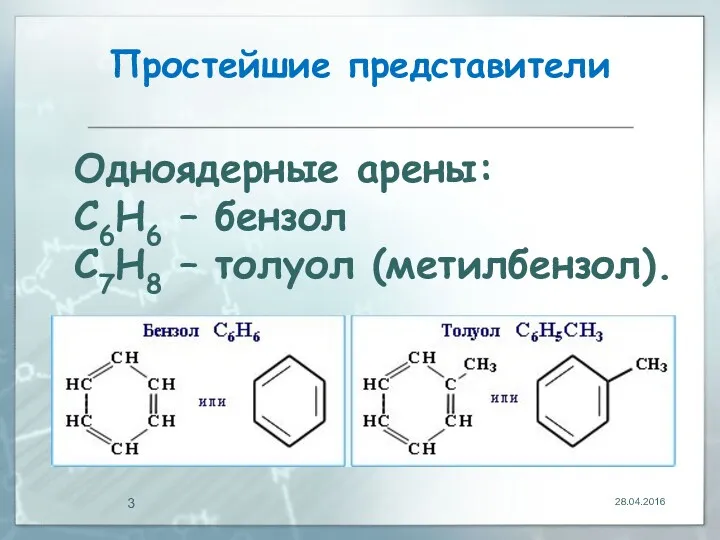
- 3. Простейшие представители 28.04.2016 Одноядерные арены: С6Н6 – бензол С7Н8 – толуол (метилбензол).
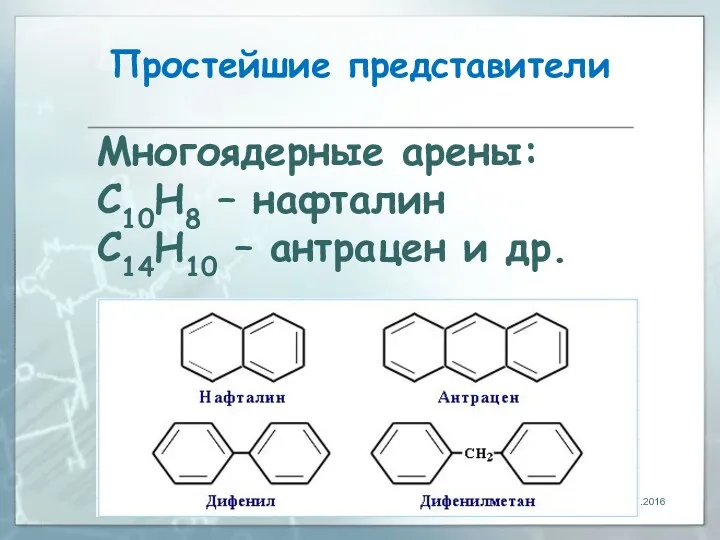
- 4. Простейшие представители 28.04.2016 Многоядерные арены: С10Н8 – нафталин С14Н10 – антрацен и др.
- 5. Арены Ароматичность молекулы означает ее повышенную устойчивость, обусловленную делокализацией p-электронов в циклической системе. Термин "ароматические соединения"
- 6. Критерии ароматичности аренов: Атомы углерода в sp2-гибридизованном состоянии образуют циклическую систему. Атомы углерода располагаются в одной
- 7. Строение бензола Бензол С6Н6 – родоначальник ароматических углеводородов. Каждый из шести атомов углерода в его молекуле
- 8. Строение бензола Валентные углы между каждой парой s-связей равны 120°. скелет σ-связей представляет собой правильный шестиугольник,
- 9. Строение бензола р-Электроны всех атомов углерода взаимодействуют между собой путем бокового перекрывания соседних 2р-АО, расположенных перпендикулярно
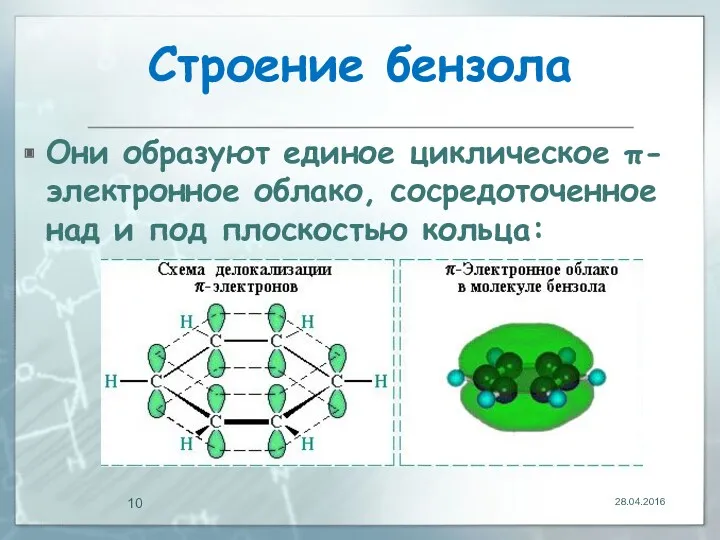
- 10. Строение бензола Они образуют единое циклическое π-электронное облако, сосредоточенное над и под плоскостью кольца: 28.04.2016
- 11. Строение бензола Все связи С-С в бензоле равноценны, их длина равна 0,140 нм, что соответствует промежуточному
- 12. Номенклатура аренов Гомологи бензола – соединения, образованные заменой одного или нескольких атомов водорода в молекуле бензола
- 13. Номенклатура аренов Широко используются тривиальные названия (толуол, ксилол, кумол и т.п.). Систематические названия строят из названия
- 14. Номенклатура аренов Если радикалов два или более, их положение указывается номерами атомов углерода в кольце, с
- 15. Номенклатура аренов Для дизамещенных бензолов R-C6H4-R используется также и другой способ построения названий, при котором положение
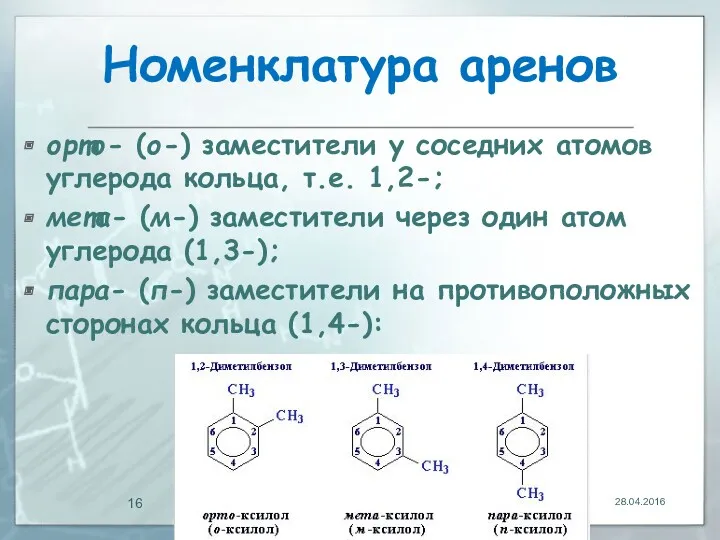
- 16. Номенклатура аренов орто- (о-) заместители у соседних атомов углерода кольца, т.е. 1,2-; мета- (м-) заместители через
- 17. Номенклатура аренов Ароматические одновалентные радикалы имеют общее название "арил". Из них наиболее распространены в номенклатуре органических
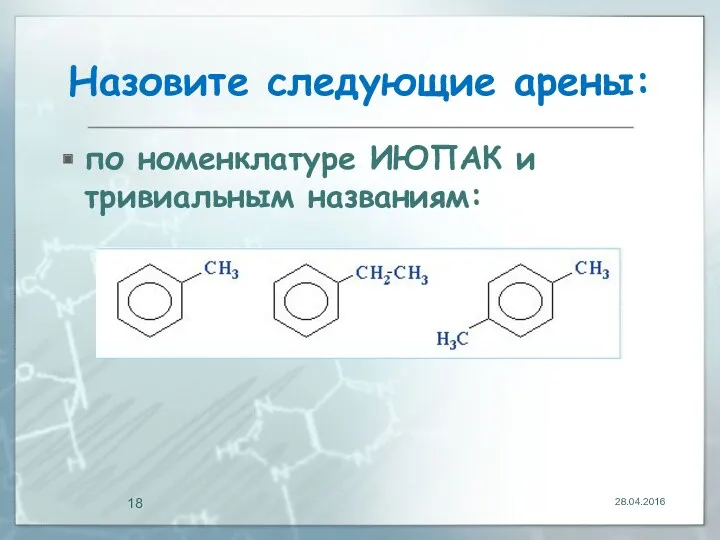
- 18. Назовите следующие арены: по номенклатуре ИЮПАК и тривиальным названиям: 28.04.2016
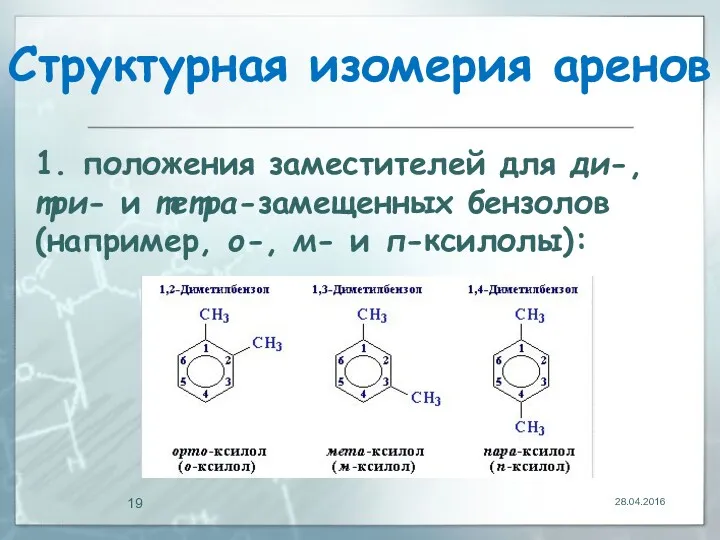
- 19. Структурная изомерия аренов 28.04.2016 1. положения заместителей для ди-, три- и тетра-замещенных бензолов (например, о-, м-
- 20. Структурная изомерия аренов 28.04.2016 2. углеродного скелета в боковой цепи, содержащей не менее 3-х атомов углерода:
- 21. Структурная изомерия аренов 28.04.2016 3. изомерия заместителей R, начиная с R = С2Н5. Например, молекулярной формуле
- 22. Структурная изомерия аренов 28.04.2016 4. Межклассовая изомерия с непредельными соединениями: формуле С6Н6 соответствует сразу несколько соединений:
- 23. Пространственная изомерия аренов Пространственная изомерия относительно бензольного кольца в алкилбензолах отсутствует 28.04.2016
- 24. Физические свойства аренов Бензол и его ближайшие гомологи – бесцветные жидкие вещества, нерастворимые в воде, но
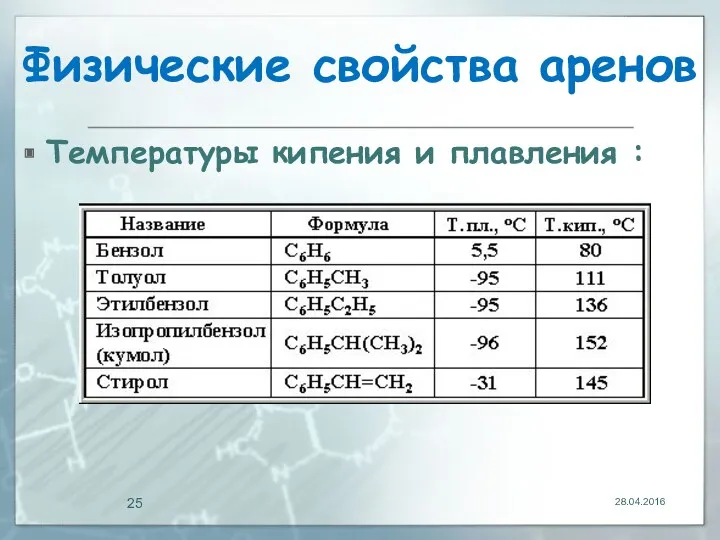
- 25. Физические свойства аренов Температуры кипения и плавления : 28.04.2016
- 26. Химические свойства аренов Отличаются от предельных и непредельных углеводородов. Это объясняется особенностями строения бензольного кольца. Делокализация
- 27. Химические свойства аренов арены не склонны вступать в реакции присоединения или окисления, которые ведут к нарушению
- 28. Химические свойства аренов Наличие областей повышенной p-электронной плотности с двух сторон плоского ароматического цикла ведет к
- 29. Химические свойства аренов для ароматических соединений наиболее типичны реакции электрофильного замещения: Другие реакции (присоединение, окисление) идут
- 30. Химические свойства аренов Механизм электрофильного замещения обозначается символом SЕ (по первым буквам английских терминов: S –
- 31. Галогенирование (присоединение галогенов) Замещение атома водорода в бензольном кольце на галоген происходит в присутствии катализаторов (кислот
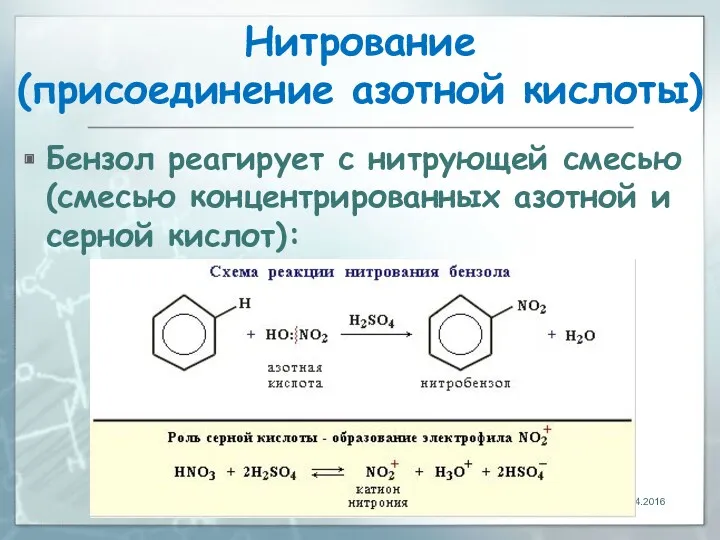
- 32. Нитрование (присоединение азотной кислоты) Бензол реагирует с нитрующей смесью (смесью концентрированных азотной и серной кислот): 28.04.2016
- 33. Алкилирование Замещение атома водорода в бензольном кольце на алкильную группу (алкилирование) происходит под действием алкилгалогенидов или
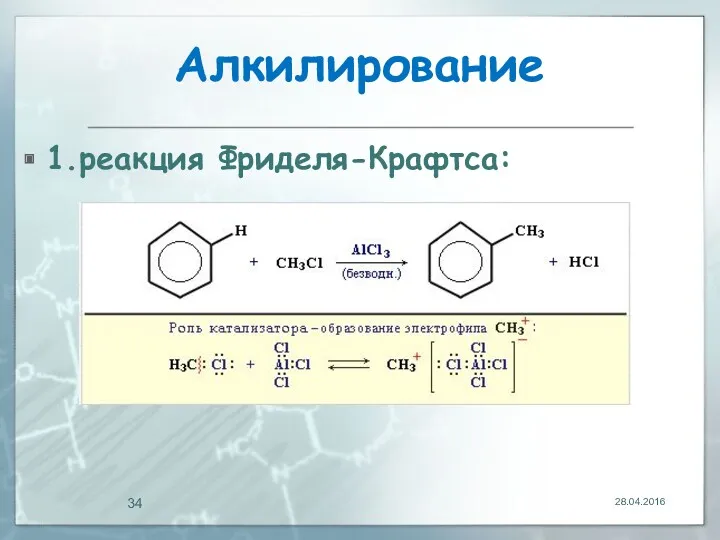
- 34. Алкилирование 1.реакция Фриделя-Крафтса: 28.04.2016
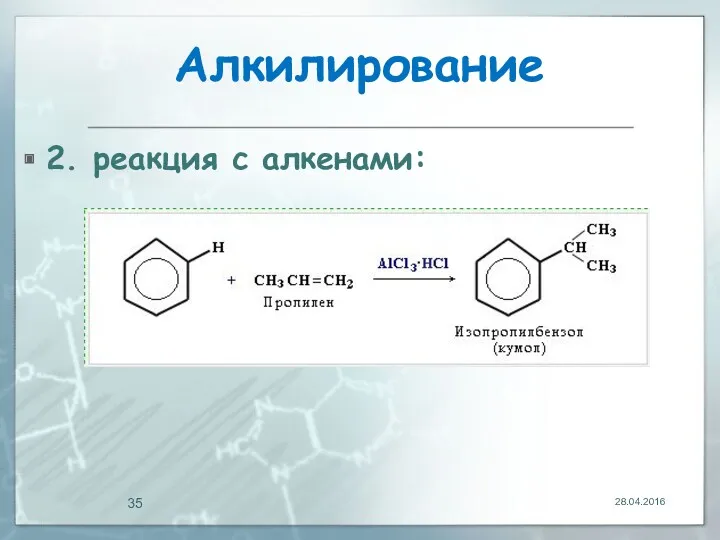
- 35. Алкилирование 2. реакция с алкенами: 28.04.2016
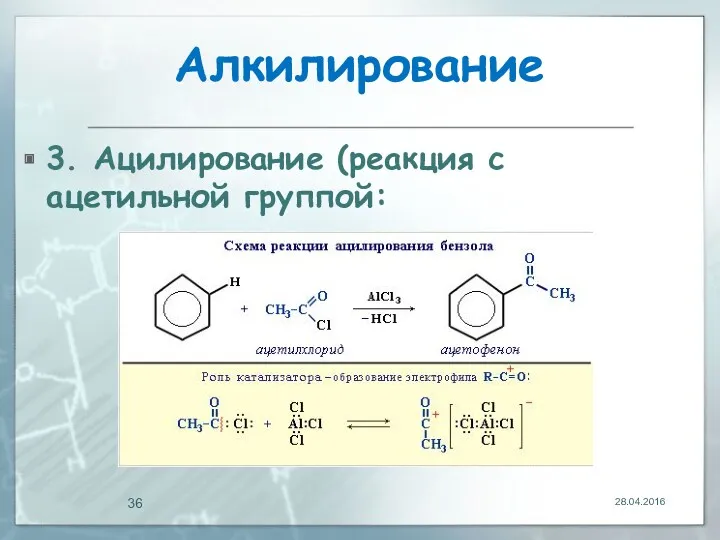
- 36. Алкилирование 3. Ацилирование (реакция с ацетильной группой: 28.04.2016
- 37. Замещение в алкилбензолах Получение тринитротолуола (при нитровании толуола С6Н5CH3 (70°С) происходит замещение не одного, а трех
- 38. Реакции присоединения В реакции присоединения, приводящие к разрушению ароматической структуры бензольного кольца, арены могут вступать с
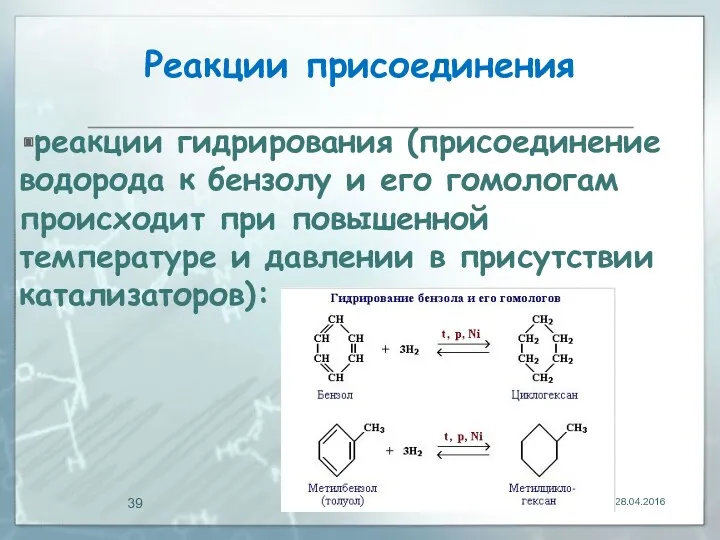
- 39. Реакции присоединения реакции гидрирования (присоединение водорода к бензолу и его гомологам происходит при повышенной температуре и
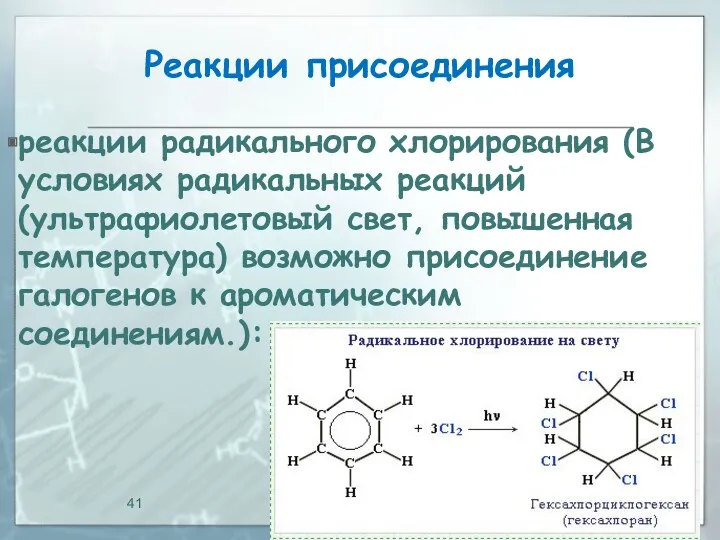
- 40. Реакции присоединения реакции хлорирования: Практическое значение имеет радикальное хлорирование бензола для получения "гексахлорана" (средство борьбы с
- 41. Реакции присоединения реакции радикального хлорирования (В условиях радикальных реакций (ультрафиолетовый свет, повышенная температура) возможно присоединение галогенов
- 42. Окисление аренов Бензол не окисляется даже под действием сильных окислителей (KMnO4, K2Cr2O7 и т.п.). Поэтому он
- 43. Окисление аренов 1. При действии раствора KMnO4 и нагревании в гомологах бензола окислению подвергаются только боковые
- 44. Окисление аренов Окисление других гомологов (этилбензол, пропилбензол и т.д.) также приводит к образованию бензойной кислоты. Разрыв
- 45. Окисление аренов 2. Бензол и его гомологи на воздухе горят коптящим пламенем, что обусловлено высоким содержанием
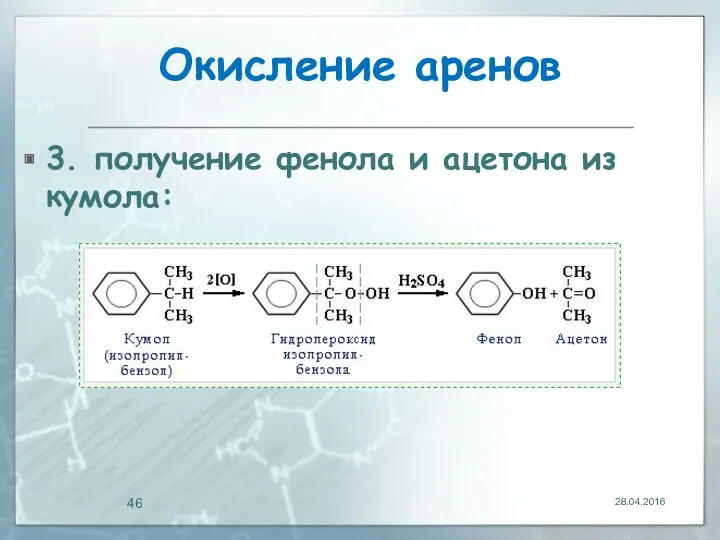
- 46. Окисление аренов 3. получение фенола и ацетона из кумола: 28.04.2016
- 47. Получение ароматических углеводородов I. При коксовании каменного угля образуется каменноугольная смола, из которой выделяют бензол, толуол,
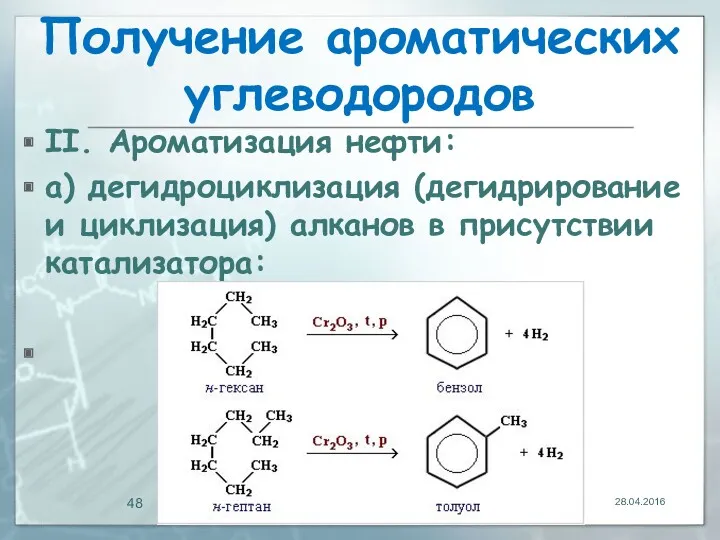
- 48. Получение ароматических углеводородов II. Ароматизация нефти: а) дегидроциклизация (дегидрирование и циклизация) алканов в присутствии катализатора: 28.04.2016
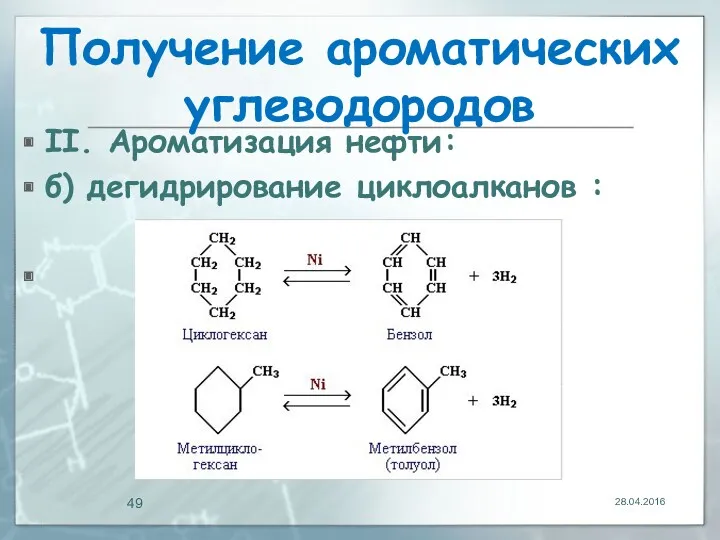
- 49. Получение ароматических углеводородов II. Ароматизация нефти: б) дегидрирование циклоалканов : 28.04.2016
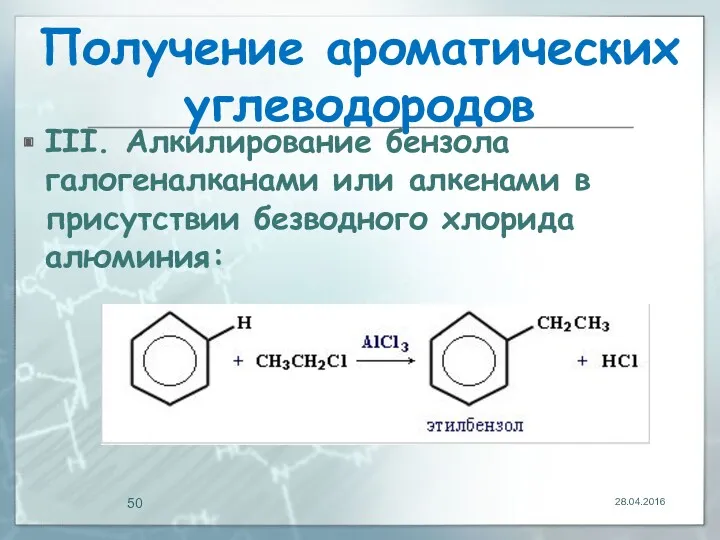
- 50. Получение ароматических углеводородов III. Алкилирование бензола галогеналканами или алкенами в присутствии безводного хлорида алюминия: 28.04.2016
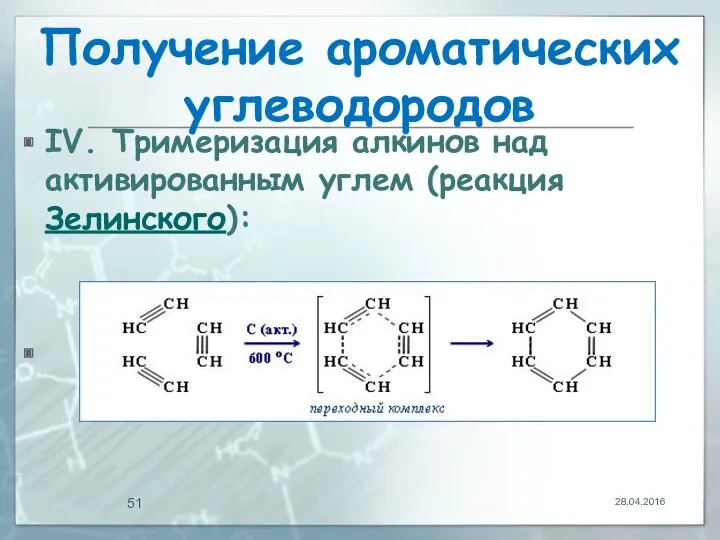
- 51. Получение ароматических углеводородов IV. Тримеризация алкинов над активированным углем (реакция Зелинского): 28.04.2016
- 52. Получение ароматических углеводородов V. Сплавление солей ароматических карбоновых кислот со щёлочью (лабораторный метод): 28.04.2016
- 53. Применение аренов Бензол С6Н6 используется как исходный продукт для получения различных ароматических соединений – нитробензола, хлорбензола,
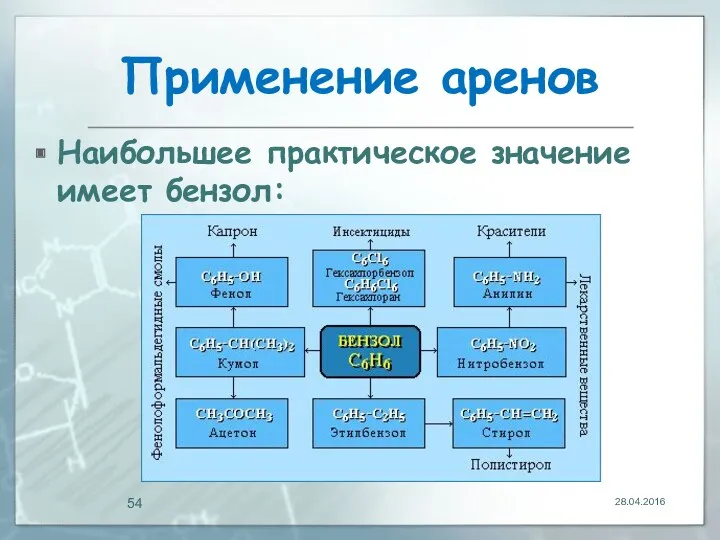
- 54. Применение аренов Наибольшее практическое значение имеет бензол: 28.04.2016
- 55. Применение аренов Толуол С6Н5-СН3 применяется в производстве красителей, лекарственных и взрывчатых веществ (тротил, тол). Ксилолы С6Н4(СН3)2
- 56. Применение аренов Изопропилбензол (кумол) С6Н4-СН(СН3)2 – исходное вещество для получения фенола и ацетона. Винилбензол (стирол) C6H5-CН=СН2
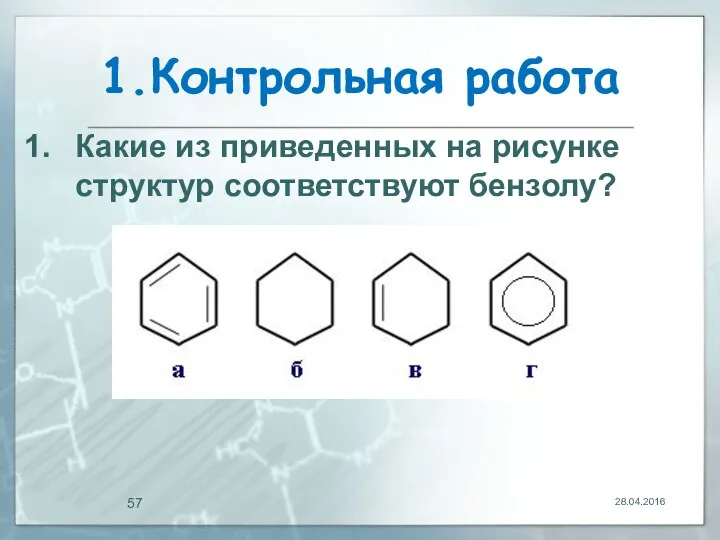
- 57. 1.Контрольная работа 28.04.2016 Какие из приведенных на рисунке структур соответствуют бензолу?
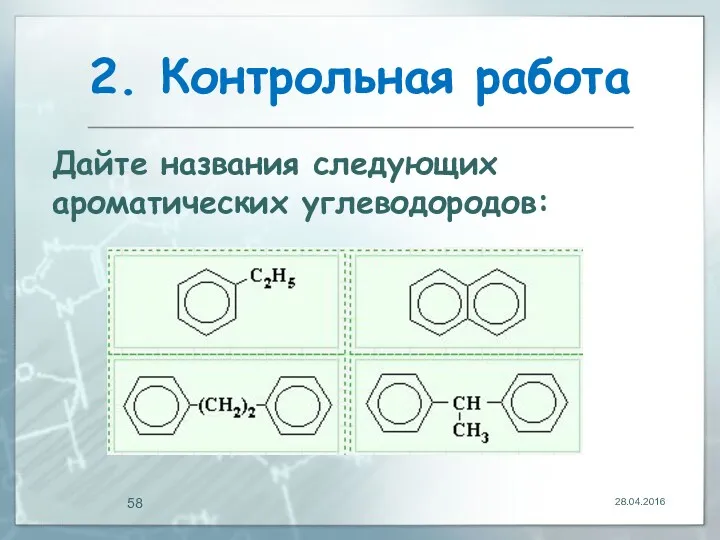
- 58. 2. Контрольная работа 28.04.2016 Дайте названия следующих ароматических углеводородов:
- 59. 3.Контрольная работа 28.04.2016 Какой тип гибридизации характерен для атомов углерода в молекуле бензола? Ответ 1: sp3
- 60. 4. Контрольная работа 28.04.2016 Какие арены изомерны друг другу: а) орто-ксилол; б) этилбензол; в) метилбензол; г)
- 61. 5. Контрольная работа 28.04.2016 Нарисуйте структурную формулу бензола и:
- 62. 6. Контрольная работа 28.04.2016 Нарисуйте следующие соединения:
- 63. 7. Контрольная работа 28.04.2016 Массовая доля выхода бензола при тримеризации ацетилена составляет 42%. Чему равна масса
- 64. 8. Контрольная работа 28.04.2016 Какое вещество из образующихся в приведенной схеме превращений (X, Y или Z)
- 65. Напишите уравнения реакций, проанализировав видеоролики из папки «Лабораторные опыты». 28.04.2016
- 66. Получение аренов Получение и свойства бензола. Напишите уравнение реакции: (видеоролик exp6.exe в папке лабораторные опыты) 28.04.2016
- 67. Свойства аренов Напишите уравнение реакции: (видеоролик exp7.exe в папке лабораторные опыты) 28.04.2016
- 68. Свойства аренов Напишите уравнение реакции: (видеоролик exp8.exe в папке лабораторные опыты) 28.04.2016
- 70. Скачать презентацию














































 Классификация химических элементов
Классификация химических элементов Азотная кислота. Соли азотной кислоты. Получение и применение (9 класс)
Азотная кислота. Соли азотной кислоты. Получение и применение (9 класс) Алкины. Непредельные углеводороды
Алкины. Непредельные углеводороды Характеристика химического элемента по кислотно-основным свойствам образуемых им соединений. Амфотерные оксиды и гидроксиды
Характеристика химического элемента по кислотно-основным свойствам образуемых им соединений. Амфотерные оксиды и гидроксиды Химические элементы в организме человека
Химические элементы в организме человека Обратимость химических реакций. Химическое равновесие и способы его смещения
Обратимость химических реакций. Химическое равновесие и способы его смещения Непредельные углеводороды
Непредельные углеводороды Химические свойства получение и применение солей
Химические свойства получение и применение солей Роль хімії в природі
Роль хімії в природі Кислоты. Состав и классификация кислот. Формулы и названия основных неорганических кислот
Кислоты. Состав и классификация кислот. Формулы и названия основных неорганических кислот Кислотно-основные равновесия. Введение в титриметрию
Кислотно-основные равновесия. Введение в титриметрию Фтор (Fluorum), F
Фтор (Fluorum), F Опасности среды обитания человека
Опасности среды обитания человека Строение атома. Химическая связь
Строение атома. Химическая связь Скорость химических реакций. Факторы, влияющие на скорость химической реакции
Скорость химических реакций. Факторы, влияющие на скорость химической реакции Факторы и процессы формирования химического состава подземных вод
Факторы и процессы формирования химического состава подземных вод Лекция Атомное строение твердых тел. 1-01
Лекция Атомное строение твердых тел. 1-01 Геохимия метасоматтческого процесса. (Лекция 7)
Геохимия метасоматтческого процесса. (Лекция 7) Соединения химических элементов. Валентность и степень окисления элементов
Соединения химических элементов. Валентность и степень окисления элементов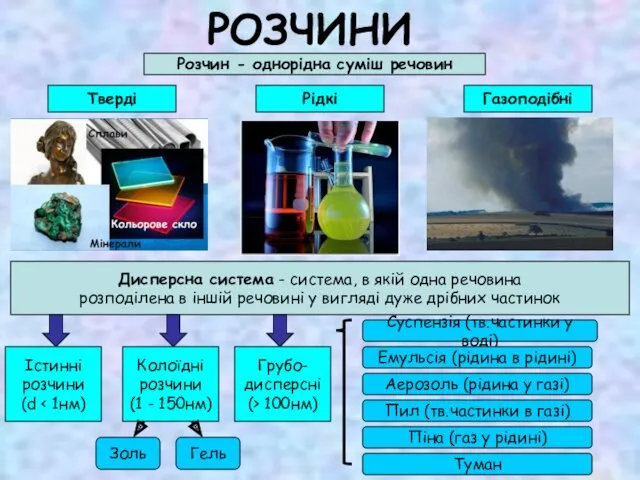 Розчини
Розчини Открытие периодического закона
Открытие периодического закона Азотсодержащие соединения. Амины. Аминокислоты
Азотсодержащие соединения. Амины. Аминокислоты Основные характеристики различных сортов меда
Основные характеристики различных сортов меда Тыңайтқышты тиімді пайдалансақ
Тыңайтқышты тиімді пайдалансақ Волшебные кристалы
Волшебные кристалы М.В.Ломоносов о пользе стекла
М.В.Ломоносов о пользе стекла Взаимодействия кислорода с металлом
Взаимодействия кислорода с металлом Электоролиз заңы
Электоролиз заңы