Содержание
- 2. ВОДОРОД
- 3. Тема: Водород, получение, свойства и применение Цель: 8.4.2.1 уметь получать водород, изучать его свойства и применение
- 4. Водород — первый элемент периодической системы элементов; обозначается символом H.
- 5. Генри Кавендиш Первым убедился,что при действии кислот на некоторые металлы образуется«ГОРЮЧИЙ ГАЗ», который в смеси с
- 6. Антуан Лавуазье Первым установил, что водород при сгорании образует воду, и назвал его Hydrogenium – «рождающий
- 7. Распространение в природе В земной коре – массовая доля всего – 1% (из-за малой массы атомов
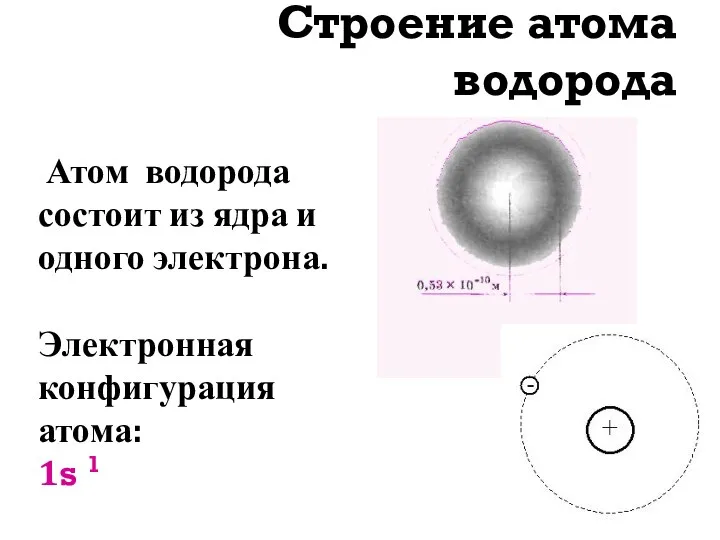
- 8. Строение атома водорода Атом водорода состоит из ядра и одного электрона. Электронная конфигурация атома: 1s 1
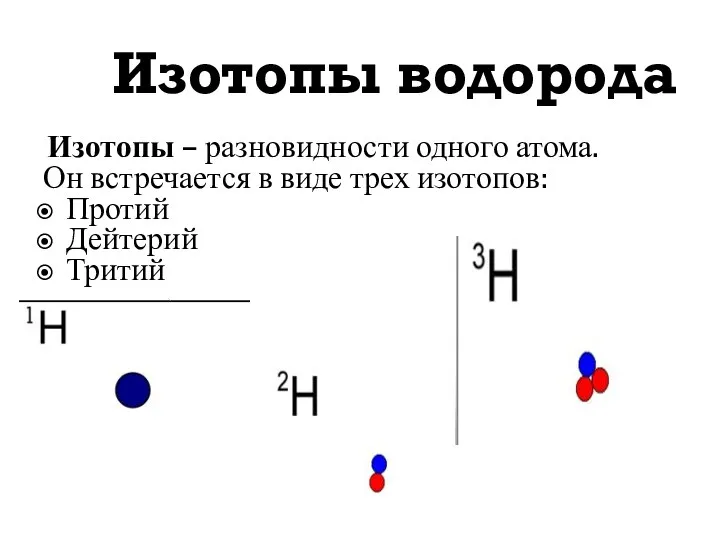
- 9. Изотопы водорода Изотопы – разновидности одного атома. Он встречается в виде трех изотопов: Протий Дейтерий Тритий
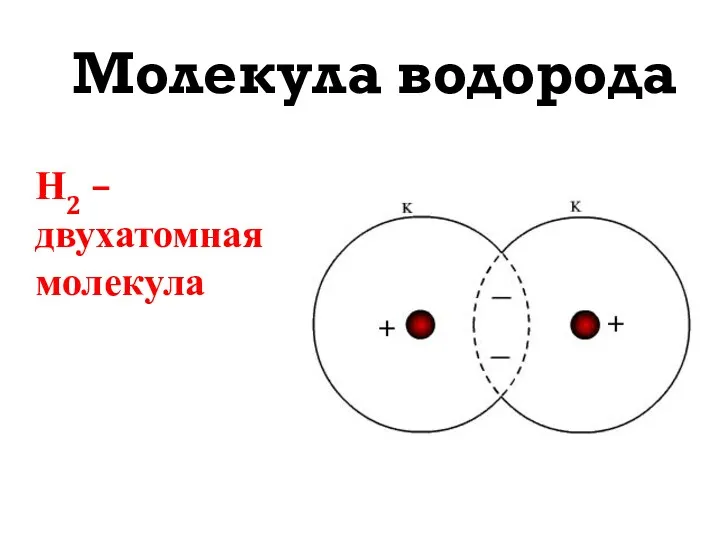
- 10. Молекула водорода Н2 – двухатомная молекула
- 11. Физические свойства Бесцветный газ Без запаха Почти нерастворим в воде ( 1: 50 ) Плотность –
- 12. Получение водорода В лаборатории: Взаимодействие цинка с соляной кислотой: Zn+2HCl = ZnCl2+ H2 В промышленности: 1.Разложение
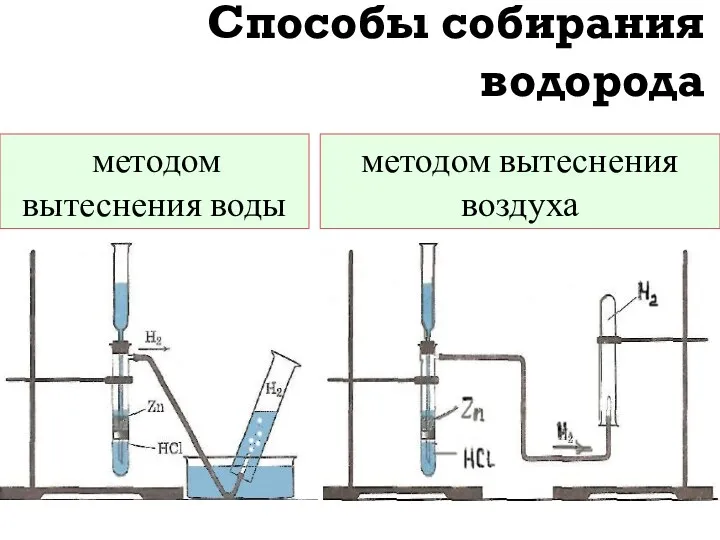
- 13. Способы собирания водорода методом вытеснения воды методом вытеснения воздуха
- 15. Скачать презентацию








 Теоретические основы органической химии
Теоретические основы органической химии Кислоты, их классификация и свойства в свете ТЭД
Кислоты, их классификация и свойства в свете ТЭД Основания. 8 класс
Основания. 8 класс Электролитическая диссоциация. Электролиты и неэлектролиты
Электролитическая диссоциация. Электролиты и неэлектролиты Закономерности химических реакций. (Лекция 3)
Закономерности химических реакций. (Лекция 3) Практическая работа. Химический состав клетки
Практическая работа. Химический состав клетки Накопление химических знаний в доисторические времена
Накопление химических знаний в доисторические времена Установка гидрокрекинга
Установка гидрокрекинга Аналитическая химия. Кислотно-основное титрование
Аналитическая химия. Кислотно-основное титрование Амфотерность
Амфотерность Oxygen, O2
Oxygen, O2 Флотационные реагенты. Активаторы
Флотационные реагенты. Активаторы Мини-тақталарда немесе дәптерде қатты, сұйық және газтектес заттардың құрылысын сал
Мини-тақталарда немесе дәптерде қатты, сұйық және газтектес заттардың құрылысын сал Гидролиз неорганических солей
Гидролиз неорганических солей Предельные углеводороды
Предельные углеводороды Галогены. Хлор
Галогены. Хлор Кислотность и основность органических соединений. (Лекция 3)
Кислотность и основность органических соединений. (Лекция 3) Тепловой эффект химических реакций
Тепловой эффект химических реакций Группа редкоземельных элементов
Группа редкоземельных элементов Химические уравнения Закон сохранения массы веществ
Химические уравнения Закон сохранения массы веществ Зеленая химия полиуретанов: механизм, катализ, проблемы использования возобновляемого сырья
Зеленая химия полиуретанов: механизм, катализ, проблемы использования возобновляемого сырья Сероводород, сернистый водород
Сероводород, сернистый водород Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Химический элемент - водород
Химический элемент - водород Соли
Соли Теория электролитической диссоциации (ТЭД), ионные уравнения
Теория электролитической диссоциации (ТЭД), ионные уравнения Производство серной кислоты
Производство серной кислоты Металл серебро
Металл серебро