Содержание
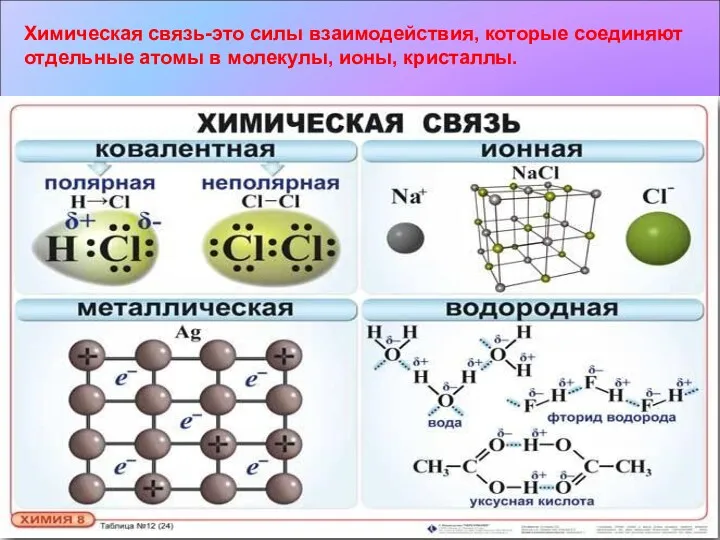
- 2. Химическая связь-это силы взаимодействия, которые соединяют отдельные атомы в молекулы, ионы, кристаллы.
- 3. * Ковалентная неполярная связь Химическая связь, возникающая в результате образования общих электронных пар, называется ковалентной. Связь
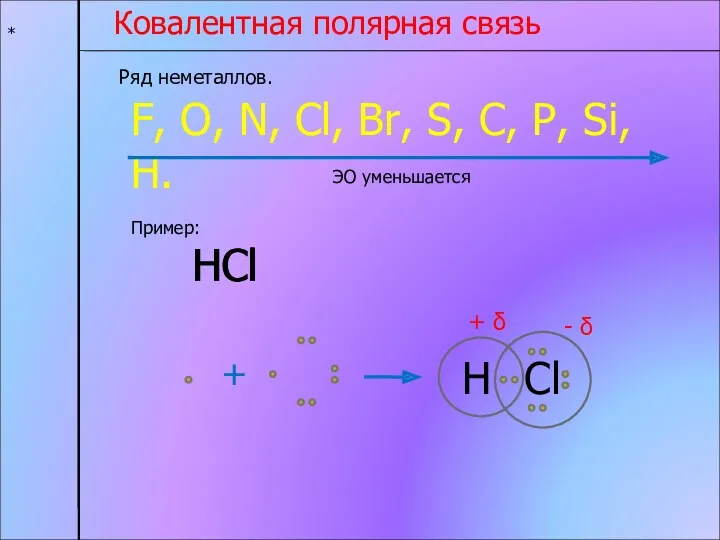
- 4. * Ковалентная полярная связь Ряд неметаллов. F, O, N, Cl, Br, S, C, P, Si, H.
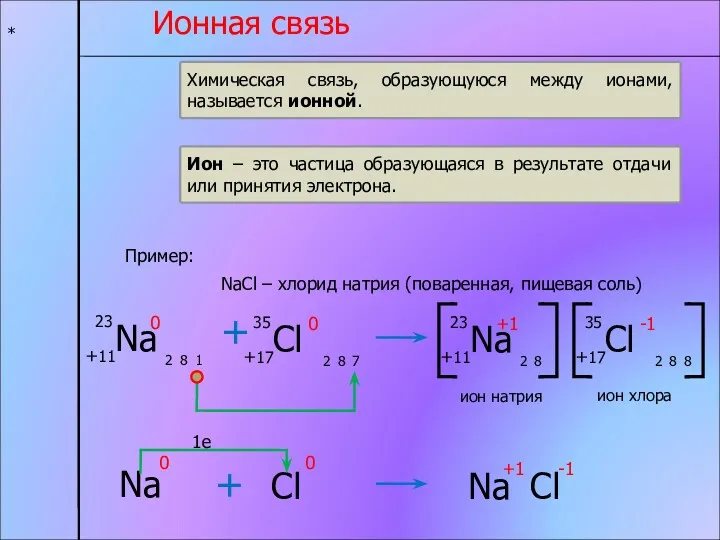
- 5. * Ионная связь Химическая связь, образующуюся между ионами, называется ионной. Ион – это частица образующаяся в
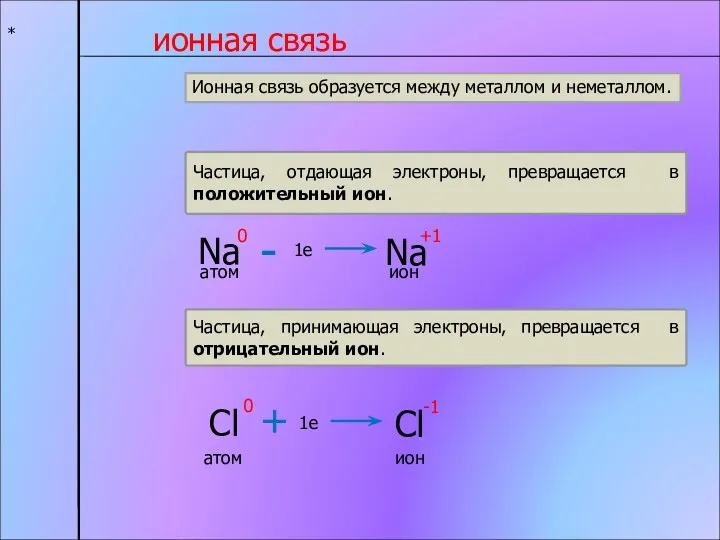
- 6. * ионная связь Частица, отдающая электроны, превращается в положительный ион. Частица, принимающая электроны, превращается в отрицательный
- 7. * Металлическая связь Связь в металлах и сплавах между атом – ионами посредством обобществленных электронов называют
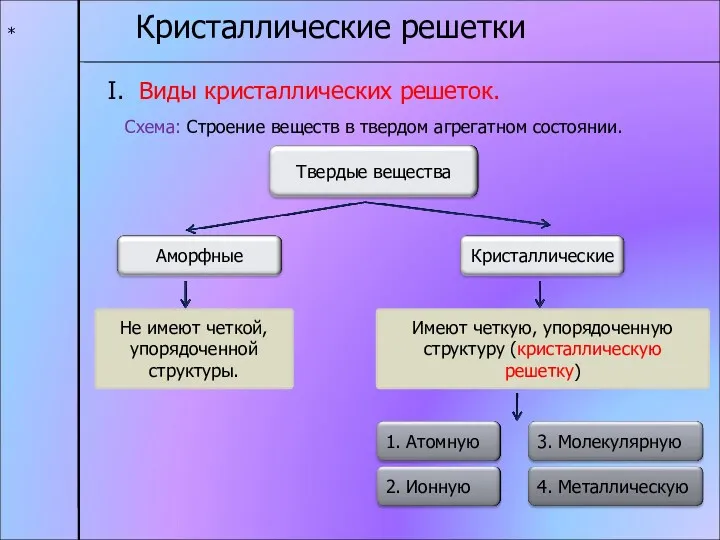
- 8. * Кристаллические решетки I. Виды кристаллических решеток. Схема: Строение веществ в твердом агрегатном состоянии. Не имеют
- 9. *
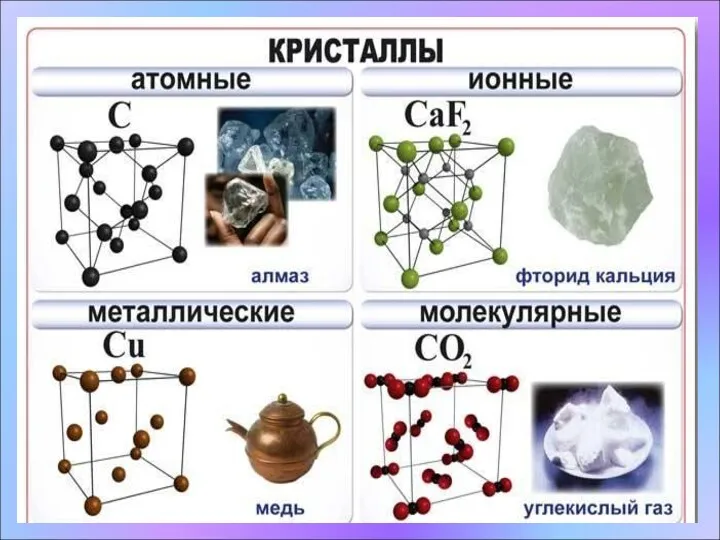
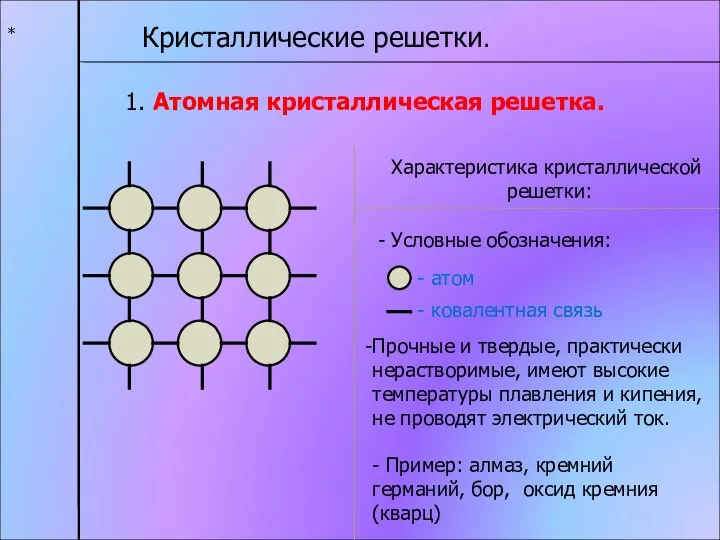
- 10. * Кристаллические решетки. 1. Атомная кристаллическая решетка. Характеристика кристаллической решетки: - атом - ковалентная связь Прочные
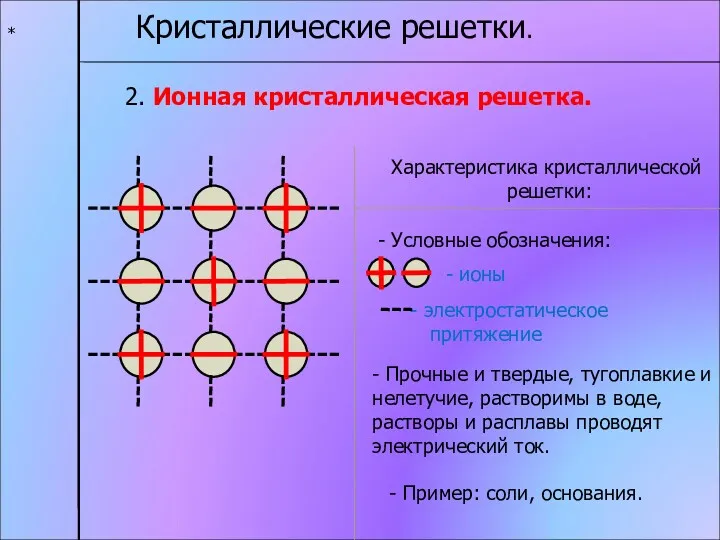
- 11. * Кристаллические решетки. 2. Ионная кристаллическая решетка. Характеристика кристаллической решетки: - ионы электростатическое притяжение - Прочные
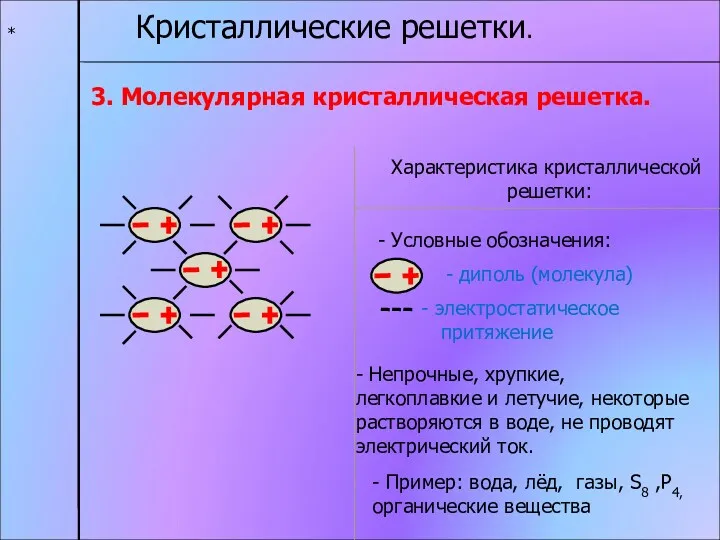
- 12. * Кристаллические решетки. 3. Молекулярная кристаллическая решетка. Характеристика кристаллической решетки: - диполь (молекула) электростатическое притяжение -
- 14. Скачать презентацию


 Физико-химические свойства сырья, продукции, реагентов и материалов (часть 2)
Физико-химические свойства сырья, продукции, реагентов и материалов (часть 2)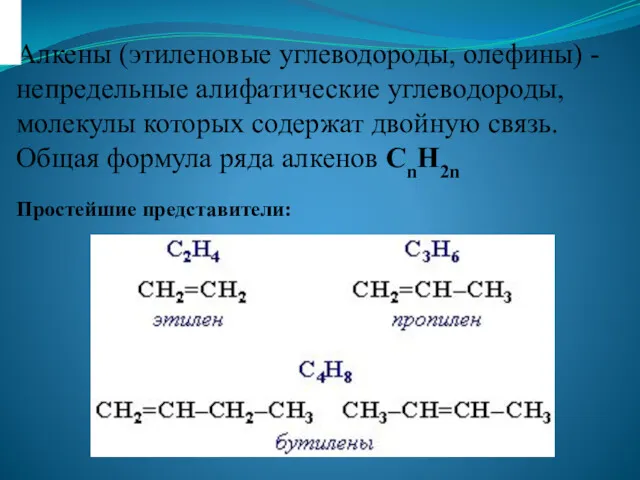 Алкены (этиленовые углеводороды, олефины)
Алкены (этиленовые углеводороды, олефины) Основные характеристи нефти и нефтеподуктов
Основные характеристи нефти и нефтеподуктов Химическая связь
Химическая связь Общая характеристика углеводов: глюкоза
Общая характеристика углеводов: глюкоза Элемент № 24 периодической таблицы. Хром
Элемент № 24 периодической таблицы. Хром Керамика на основе Al2O3
Керамика на основе Al2O3 Анализ качества неорганических лекарственных средств количественно определяемых методами редоксиметрии
Анализ качества неорганических лекарственных средств количественно определяемых методами редоксиметрии Нитрид галлия. Основные свойства и применение. GaN и твердые растворы на его основе
Нитрид галлия. Основные свойства и применение. GaN и твердые растворы на его основе Физико-химия полимеров и их растворов
Физико-химия полимеров и их растворов Щелочные металлы
Щелочные металлы Окислительно-восстановительные реакции. Генетический ряд кальция
Окислительно-восстановительные реакции. Генетический ряд кальция Обобщение по теме Неметаллы
Обобщение по теме Неметаллы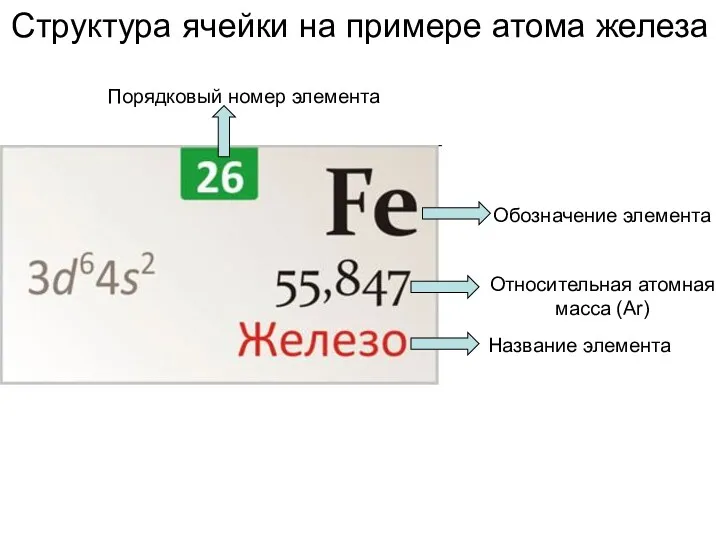 Структура ячейки на примере атома железа
Структура ячейки на примере атома железа Теория электролитической диссоциации (ТЭД), ионные уравнения
Теория электролитической диссоциации (ТЭД), ионные уравнения Строение атома
Строение атома Метод молекулярных орбиталей
Метод молекулярных орбиталей Корунд. Разновидности корунда
Корунд. Разновидности корунда Гигиена труда при работе с пестицидами и минеральными удобрениями
Гигиена труда при работе с пестицидами и минеральными удобрениями Классы неорганических веществ. Лекция №4
Классы неорганических веществ. Лекция №4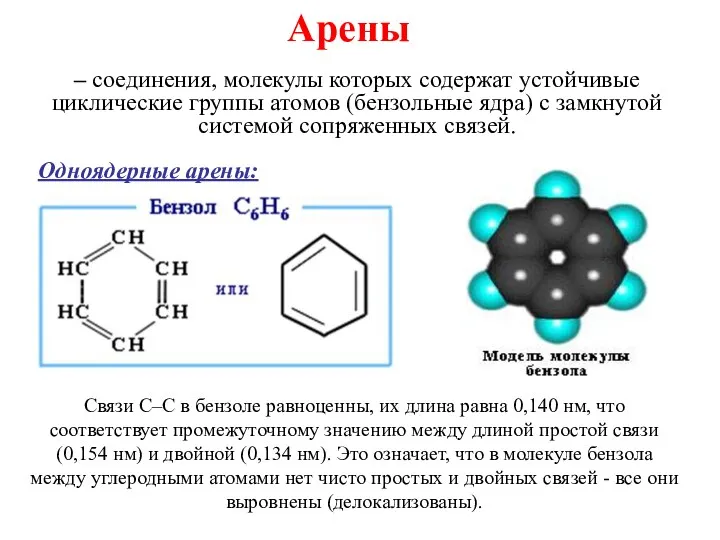 Ароматические углеводороды
Ароматические углеводороды Массообменные процессы
Массообменные процессы Основные понятия и законы химии. Тема 1
Основные понятия и законы химии. Тема 1 Фармакология. Окисление
Фармакология. Окисление Элементтер-органогендер. Көміртек – органикалық қосылыстардың негізін құраушы. Тірі және өлі табиғат арасындағы шекара
Элементтер-органогендер. Көміртек – органикалық қосылыстардың негізін құраушы. Тірі және өлі табиғат арасындағы шекара Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Titration and Acid-Base Neutralization
Titration and Acid-Base Neutralization Токсическое действие диоксинов и диоксиноподоных соединений
Токсическое действие диоксинов и диоксиноподоных соединений