Содержание
- 2. азотсодержащие органические соединения производные аммиака, в молекуле которого один, два или три атома водорода замещены на
- 3. Амины
- 4. имеет неприятный запах, малорастворим, ядовит Анилин С6Н5-NH2 Метиламин СН3-NH2 Б/ц газ, аммиачный запах, хорошо растворим в
- 5. 1.Присоединение катионов водорода (донорно-акцепторный механизм, подобно аммиаку) СН3-NH2 + Н+ СН3-NH3+ ион метиламмония С6Н5-NH2 + Н+
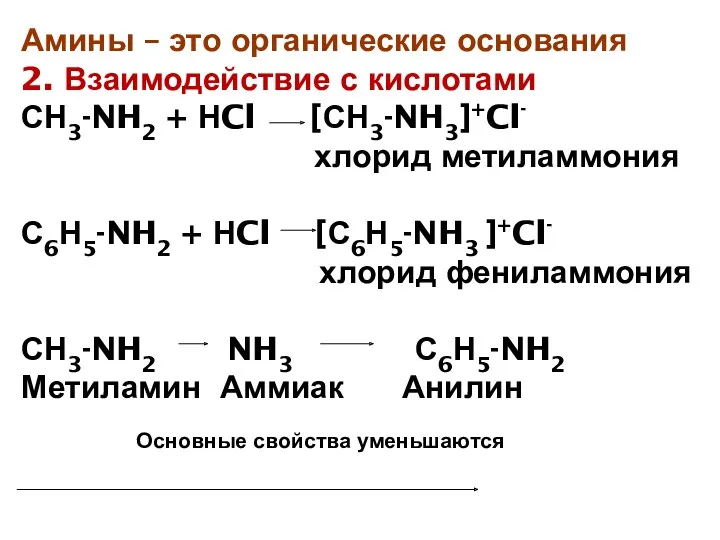
- 6. Амины – это органические основания 2. Взаимодействие с кислотами СН3-NH2 + НCl [СН3-NH3]+Cl- хлорид метиламмония С6Н5-NH2
- 7. С6Н5-NH2 анилин самое слабое основание, т.к. наблюдается взаимное влияние аминогруппы и фенилрадикала друг на друга 3.
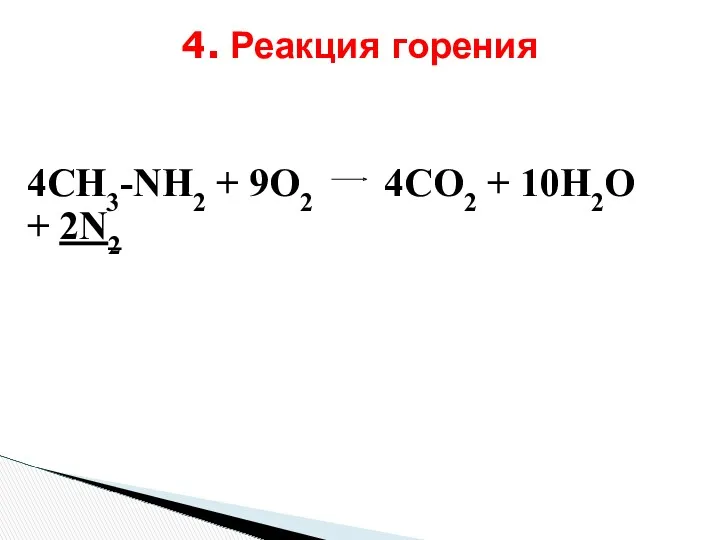
- 8. 4. Реакция горения 4СН3-NH2 + 9О2 4СО2 + 10Н2О + 2N2
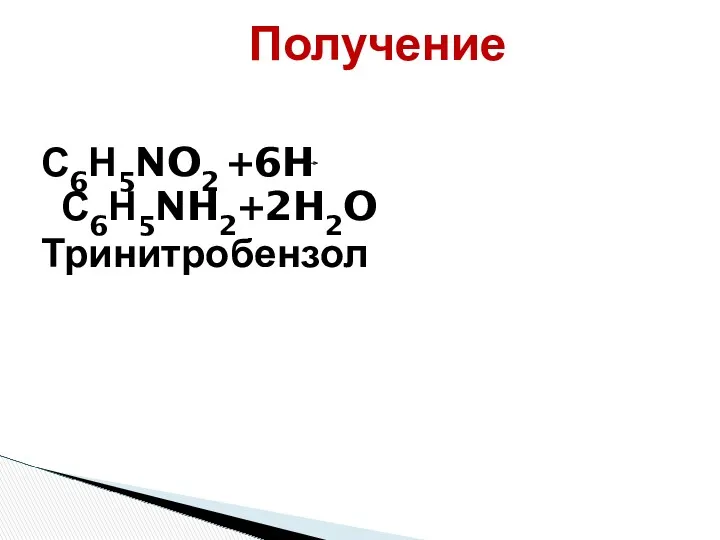
- 9. С6Н5NO2 +6H С6Н5NH2+2H2O Тринитробензол Получение
- 10. Применение Анилиновые красители Лекарства (сульфаниламиды) Полимеры Фотография
- 12. Скачать презентацию






 Металлы. Общие свойства металлов
Металлы. Общие свойства металлов Химия в организме человека
Химия в организме человека Теплота горения
Теплота горения Germaniy gruppachasining elementlarining olinishi va xossalari
Germaniy gruppachasining elementlarining olinishi va xossalari Технологическая установка Л 24-6
Технологическая установка Л 24-6 Резина и её свойства . Полимеры и их использование
Резина и её свойства . Полимеры и их использование Амінокислоти
Амінокислоти Химический состав и физические свойства продовольственных товаров
Химический состав и физические свойства продовольственных товаров Алифатические углеводороды: алканы, алкены, алкины
Алифатические углеводороды: алканы, алкены, алкины Гидролиз солей
Гидролиз солей Кислоты в свете теории электролитической диссоциации (ТЭД)
Кислоты в свете теории электролитической диссоциации (ТЭД) Оксиды. Бинарное соединение. Степень окисления у неметаллов
Оксиды. Бинарное соединение. Степень окисления у неметаллов Лекция 1. Введение в биоорганическую химию
Лекция 1. Введение в биоорганическую химию Закономірності протікання хімічних реакцій
Закономірності протікання хімічних реакцій Химический элемент кремний
Химический элемент кремний Альдегиды и кетоны
Альдегиды и кетоны Оксиды. Классификация. Номенклатура. Физические и химические свойства. Получение. Применение
Оксиды. Классификация. Номенклатура. Физические и химические свойства. Получение. Применение Гетероциклические соединения. Шестичленные гетероциклы с одним гетероатомом
Гетероциклические соединения. Шестичленные гетероциклы с одним гетероатомом Палладий. История открытия химических веществ
Палладий. История открытия химических веществ Особенности сжигания газообразного топлива и топливосжигающие устройства
Особенности сжигания газообразного топлива и топливосжигающие устройства Organic chemistry. Alcohols
Organic chemistry. Alcohols Химическая стойкость тугоплавких металлов в различных реагентах
Химическая стойкость тугоплавких металлов в различных реагентах Фазовые равновесия в системе ограниченно смешивающихся жидкостей
Фазовые равновесия в системе ограниченно смешивающихся жидкостей Гидролиз солей
Гидролиз солей Химия 8 класс. Введение в химию
Химия 8 класс. Введение в химию Органические вещества
Органические вещества Физические свойства минералов
Физические свойства минералов Определение воды по Фишеру. Кислотное число, число омыления. Определение аминного азота
Определение воды по Фишеру. Кислотное число, число омыления. Определение аминного азота