3
16.05.2016
Метод электронно-ионного баланса
K2Cr2O7 + 4H2SO4 + 3H2S = Cr2(SO4)3 + 7H2O + 3S(т) + K2SO4
Метод
электронно-ионного баланса
а) записывают формулы реагентов данной реакции и устанавливают химическую функцию каждого из них (окислитель, кислотная среда реакции, восстановитель)
б) записывают формулы реагентов в ионном виде, указывая только те ионы, молекулы и формульные единицы, которые примут участие в реакции в качестве окислителя, среды и восстановителя
в) определяют восстановленную форму окислителя и окисленную форму восстановителя, составляют электронно-ионные уравнения полуреакций восстановления и окисления
г) суммируя уравнения полуреакций, составляют ионное уравнение данной реакции,
д) на основе ионного уравнения составляют молекулярное уравнение данной реакции
е) проводят проверку подобранных коэффициентов
2e-















 Анализ проб воды
Анализ проб воды Carbohydrates and their metabolism. Digestion of carbohydrates
Carbohydrates and their metabolism. Digestion of carbohydrates Химические свойства и получение алканов
Химические свойства и получение алканов Олово и свинец
Олово и свинец Күкірт қышқылы
Күкірт қышқылы Показатели химической обстановки при авариях на химически опасных объектах
Показатели химической обстановки при авариях на химически опасных объектах Жуғыш заттар және жуғыш әсері. 2 Лекция
Жуғыш заттар және жуғыш әсері. 2 Лекция Кристаллы и минералы
Кристаллы и минералы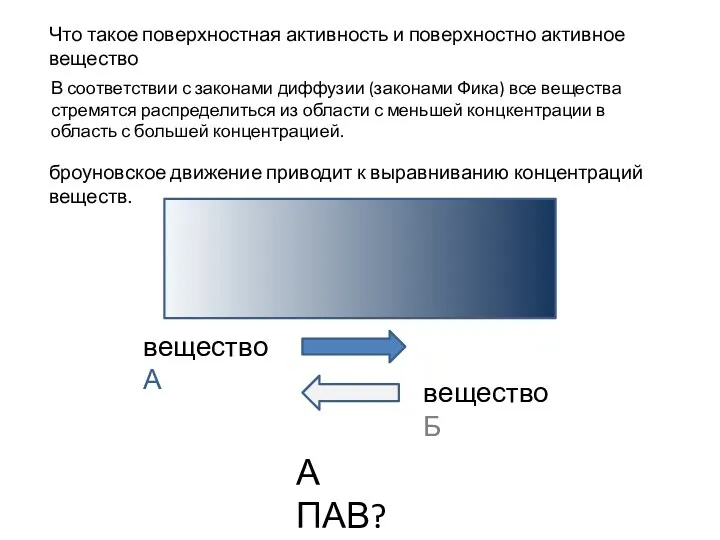 Поверхностная активность и поверхностно активное вещество
Поверхностная активность и поверхностно активное вещество Строение и свойства циклоалканов
Строение и свойства циклоалканов Химические реакции или химические явления
Химические реакции или химические явления Растворы ВМС
Растворы ВМС Констукционные и функциональные волокнистые композиты. Стекловолокно
Констукционные и функциональные волокнистые композиты. Стекловолокно Основные способы получения металлов
Основные способы получения металлов Расчет распределения пор по размерам из изотерм адсорбции
Расчет распределения пор по размерам из изотерм адсорбции Обчислення об'ємних відношень газів за хімічними рівняннями. Хімія. 9 клас
Обчислення об'ємних відношень газів за хімічними рівняннями. Хімія. 9 клас Установка гидрокрекинга
Установка гидрокрекинга Закономірності протікання хімічних реакцій
Закономірності протікання хімічних реакцій Арилалкиламины, гидроксифенилалкиламины и их производные
Арилалкиламины, гидроксифенилалкиламины и их производные Азотсодержащие органические соединения. Лекция 8
Азотсодержащие органические соединения. Лекция 8 Приёмы обращения с лабораторным оборудованием и основы техники безопасности
Приёмы обращения с лабораторным оборудованием и основы техники безопасности Особенности лантаноидов и актиноидов
Особенности лантаноидов и актиноидов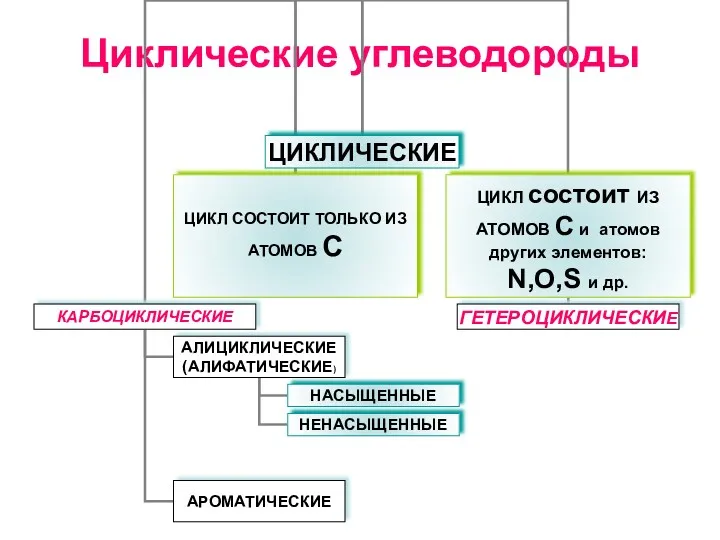 Циклические углеводороды
Циклические углеводороды Полимеры
Полимеры Кристаллические решетки
Кристаллические решетки Алкадиены: строение, номенклатура, гомологи, изомерия
Алкадиены: строение, номенклатура, гомологи, изомерия Соли, их классификация и свойства
Соли, их классификация и свойства Молярная масса вещества
Молярная масса вещества