На титрование йода было израсходовано 8,01 мл Na2S2O3. Согласно ГФ Х
1мл 0,1н. раствора тиосульфата натрия соответствует 0,01269г I, следовательно, содержание йода в 10 мл исследуемого препарата равно
1мл 0,1н. раствора тиосульфата натрия соответствует 0,01269
8,0 мл – Х г;
Х = 8,0 • 0,01269 / 1 = 0,1015.
В перерасчете на 10 мл это составляет 0,1015 * 10 / 2 = 0,5076 г, следовательно массовая доля йода в растворе равна 5,1%,что соответствует содержанию йода в 10 мл препарата согласно ГФ XIII (4,9-5,2%).
На титрование йодида натрия было израсходовано 2,5 мл AgNO3. Согласно ГФ ХIII 1мл 0,1н. раствора нитрата серебра соответствует 0,01660г йодида калия следовательно, содержание йодида калия в 10 мл исследуемого препарата равно
1мл 0,1н. раствора нитрата серебра соответствует 0,01660г
2,5 мл – Х г;
Х = 2,5 • 0,01660г / 1 = 0,0415
В перерасчете на 10 мл это составляет 0,0415 * 10 / 2 = 0,2075 г, следовательно массовая доля йодида калия в растворе равна 2,1%,что соответствует содержанию йодида калия в 10 мл препарата согласно ГФ XIII (1,9-2,1%).
Подлинность и количественный анализ
раствора йода спиртового 5%











 Реакции ионного обмена
Реакции ионного обмена Щелочноземельные металлы
Щелочноземельные металлы Общая характеристика элементов V-А-группы. Азот
Общая характеристика элементов V-А-группы. Азот Сполуки фосфору
Сполуки фосфору Диагностические свойства минералов. Занятие 3-4
Диагностические свойства минералов. Занятие 3-4 Полимерные материалы. Классификация
Полимерные материалы. Классификация Алюминий
Алюминий Алюминий и его соединения
Алюминий и его соединения Реакции ионного обмена
Реакции ионного обмена Химические свойства карбоновых кислот
Химические свойства карбоновых кислот Этилен. Углеводороды ряда этилена
Этилен. Углеводороды ряда этилена Амфотерные оксиды и гидроксиды
Амфотерные оксиды и гидроксиды Донорно-акцепторний механізм утворення ковалентного зв’язку
Донорно-акцепторний механізм утворення ковалентного зв’язку Растворы. Термодинамика процесса растворения. Способы выражения концентрации. Идеальные растворы. Законы Рауля
Растворы. Термодинамика процесса растворения. Способы выражения концентрации. Идеальные растворы. Законы Рауля XXI ғасыр көшбасшысы
XXI ғасыр көшбасшысы Химические свойства серной кислоты
Химические свойства серной кислоты Реакции щелочно-земельных металлов (Группа 2) – Mg, Ca
Реакции щелочно-земельных металлов (Группа 2) – Mg, Ca Гідроліз солей
Гідроліз солей Подгруппа азота
Подгруппа азота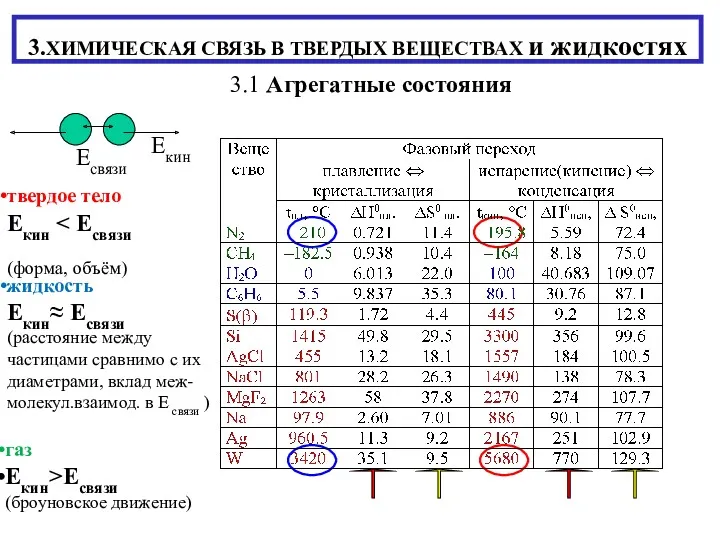 Химическая связь в твердых веществах и жидкостях
Химическая связь в твердых веществах и жидкостях Строение атома
Строение атома Алкены (олефины). Лекция 3
Алкены (олефины). Лекция 3 Пестициды. Лекция
Пестициды. Лекция Биологически важные 5-ти и 6-ти членные гетероциклические соединения. (Лекция 25)
Биологически важные 5-ти и 6-ти членные гетероциклические соединения. (Лекция 25) Кислород
Кислород Атомы и молекулы. Простые и сложные вещества. 8 класс
Атомы и молекулы. Простые и сложные вещества. 8 класс Химические явления. Химические реакции
Химические явления. Химические реакции Азотная кислота
Азотная кислота