Слайд 2

Что такое соли?
Соли–это сложные вещества, образованные атомами металлов и кислотными
остатками
Слайд 3

Номенклатура солей
Название Название Указание
Кислотного + металла (в Р.п.) + валентности
остатка (если
она переменная)
NaCl хлорид натрия
CaCO3 карбонат кальция
Са3(РО4)2 фосфат кальция
МgCI2 хлорид магния
Слайд 4

Попробуйте сами дать названия следующим солям:
KCI
CaCI2
BaCO3
Слайд 5
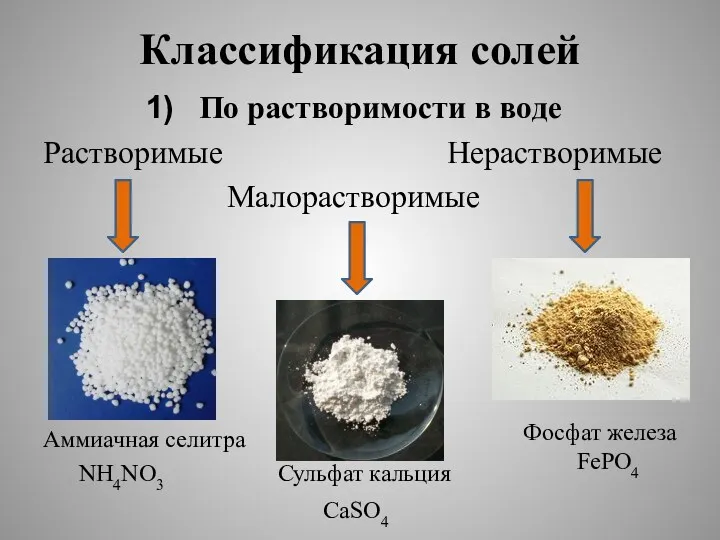
Классификация солей
По растворимости в воде
Растворимые Нерастворимые
Малорастворимые
Аммиачная селитра
NH4NO3 Сульфат кальция
Фосфат
Слайд 6
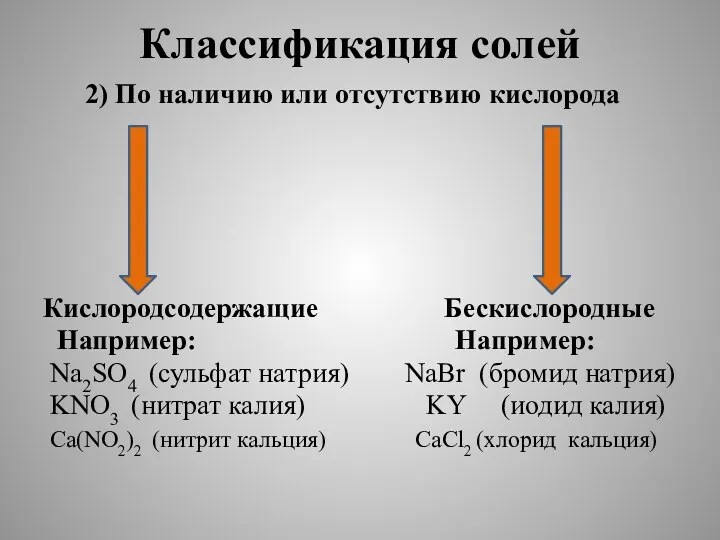
Классификация солей
2) По наличию или отсутствию кислорода
Кислородсодержащие Бескислородные
Например: Например:
Na2SO4 (сульфат натрия) NaBr (бромид натрия)
KNO3 (нитрат калия) KY (иодид калия)
Ca(NO2)2 (нитрит кальция) CaCl2 (хлорид кальция)
Слайд 7
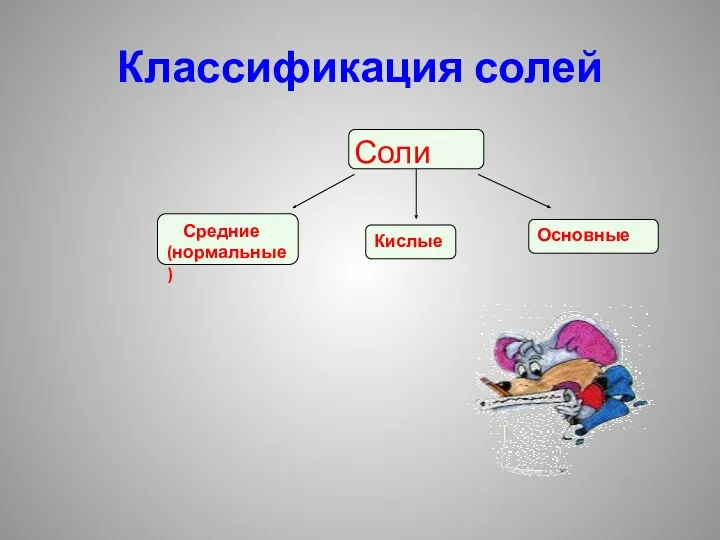
Классификация солей
Соли
Средние (нормальные)
Кислые
Основные
Слайд 8

Разновидности солей
Соли бывают:
Средние соли – это продукты полного замещения атомов водорода
в кислоте на металл.
Например: Na2CO3 (карбонат натрия)
CuSO4 (сульфат меди)
Слайд 9

Разновидности солей
2) Кислые соли – это продукты неполного замещения атомов
водорода в кислоте на металл.
Например:
NaHCO3 (гидрокарбонат натрия)
Mg(HSO4)2 (гидросульфат магния)
Слайд 10

Разновидности солей
3) Основные соли – это продукты неполного замещения гидроксогрупп
в основании на кислотный остаток.
Например:
(CuOH)2CO3 (гидроксокарбонат меди (II))
AlOHCl2 (гидроксохлорид алюминия)









 Побочная подгруппа VIII группы периодической системы
Побочная подгруппа VIII группы периодической системы Ароматические кислоты и их производные. Общая характеристика, методы получения и исследования
Ароматические кислоты и их производные. Общая характеристика, методы получения и исследования Хімічні властивості металів
Хімічні властивості металів Techniques for preparation of gaseous samples with a desired concentration of analyte
Techniques for preparation of gaseous samples with a desired concentration of analyte НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ Гидроксид магния. Mg(OH)2
Гидроксид магния. Mg(OH)2 Общие сведения о полезных ископаемых. (Лекция 2)
Общие сведения о полезных ископаемых. (Лекция 2) Вуглеводи
Вуглеводи Cromatografia ionică
Cromatografia ionică Аналитические методы
Аналитические методы Каталитический риформинг
Каталитический риформинг циклоалканы170
циклоалканы170 Современные тенденции развития химии
Современные тенденции развития химии Термодинамика
Термодинамика Комплексные соединения
Комплексные соединения Алкины. Ацетилен (Этин) – С2Н2
Алкины. Ацетилен (Этин) – С2Н2 Катализ и катализаторы
Катализ и катализаторы Тепловой эффект химической реакции. 11 класс
Тепловой эффект химической реакции. 11 класс Непредельные углеводороды ряда этилена
Непредельные углеводороды ряда этилена Предмет аналитической химии, ее структура
Предмет аналитической химии, ее структура Ионы. Проверочная работа
Ионы. Проверочная работа Применение здм к кислотно-основным равновесиям и их роль в аналитической химии
Применение здм к кислотно-основным равновесиям и их роль в аналитической химии Химическая связь
Химическая связь Аммиак
Аммиак Неметаллы. Общая характеристика
Неметаллы. Общая характеристика Алкины. 10 класс
Алкины. 10 класс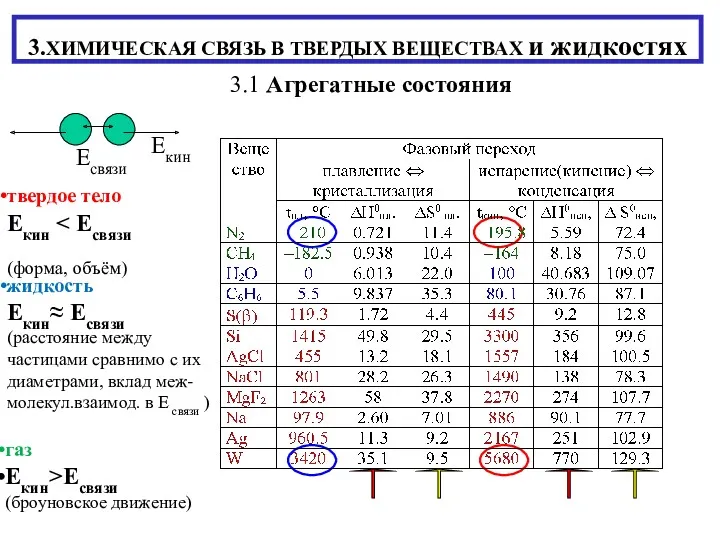 Химическая связь в твердых веществах и жидкостях
Химическая связь в твердых веществах и жидкостях ae2db93272ef42dba476a56bbc56b895
ae2db93272ef42dba476a56bbc56b895