Содержание
- 2. Литература 1. Общая химия , Глинка Н.Л. 2. Химия в центре наук, Браун, Лемей, том 1;
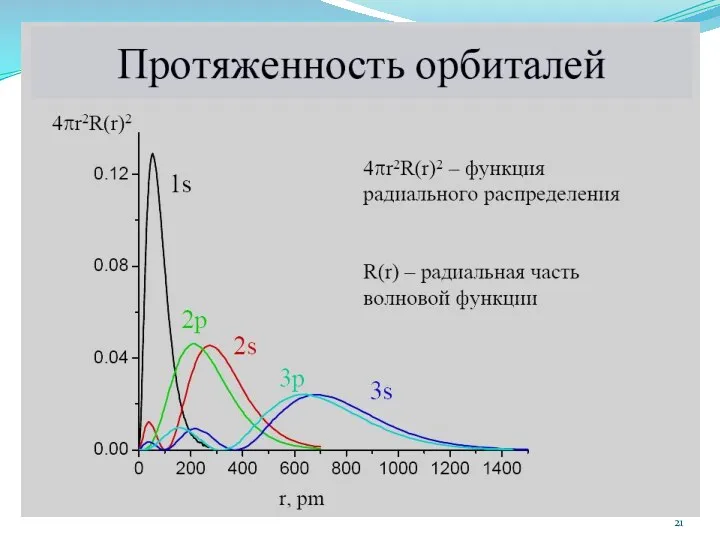
- 3. 1. Современная модель строения атома 2. Характеристика энергии электрона и пространственное распределение вероятности его нахождения в
- 4. Строение атома Атом (от греч. atomos - неделимый) - наименьшая химическая частица, состоящая из массивного положительно
- 5. Атомные частицы и их свойства Атом состоит из трёх видов частиц: 1. Электрон – (е) -
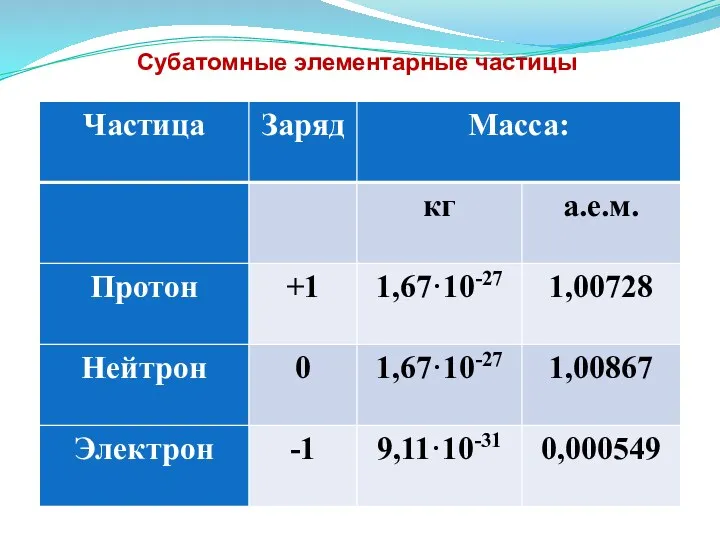
- 6. Субатомные элементарные частицы
- 8. Эрнст Резерфорд открыл α- и β-излучение короткоживущих изотопов радона и множество других изотопов. Объяснил радиоактивность тория,
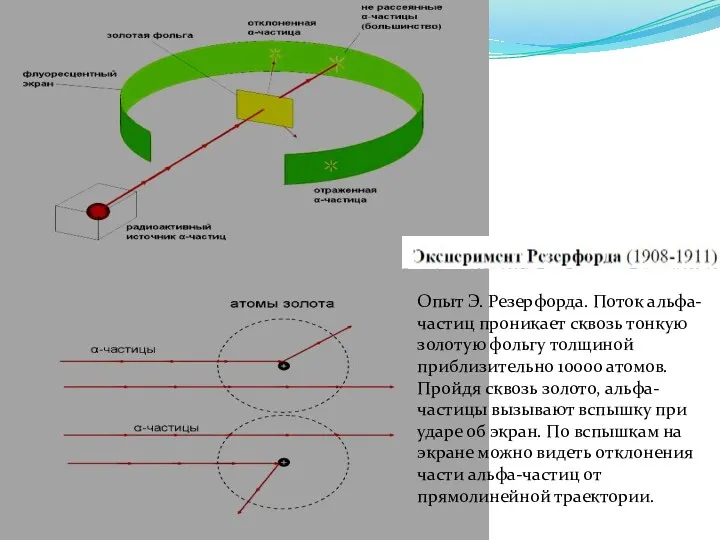
- 9. Опыт Э. Резерфорда. Поток альфа-частиц проникает сквозь тонкую золотую фольгу толщиной приблизительно 10000 атомов. Пройдя сквозь
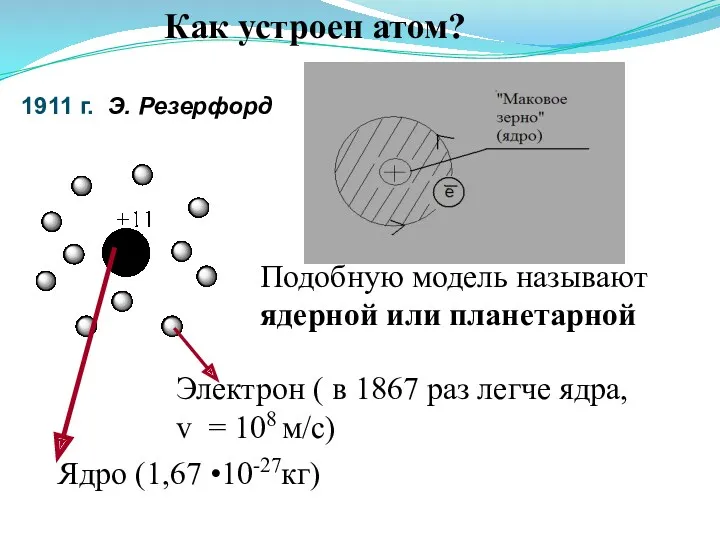
- 10. Как устроен атом? 1911 г. Э. Резерфорд Подобную модель называют ядерной или планетарной Ядро (1,67 •10-27кг)
- 11. Нильс Бор (1885-1962) В 1913 г. Нильс Бор опубликовал серию статей «О строении атомов и молекул»,
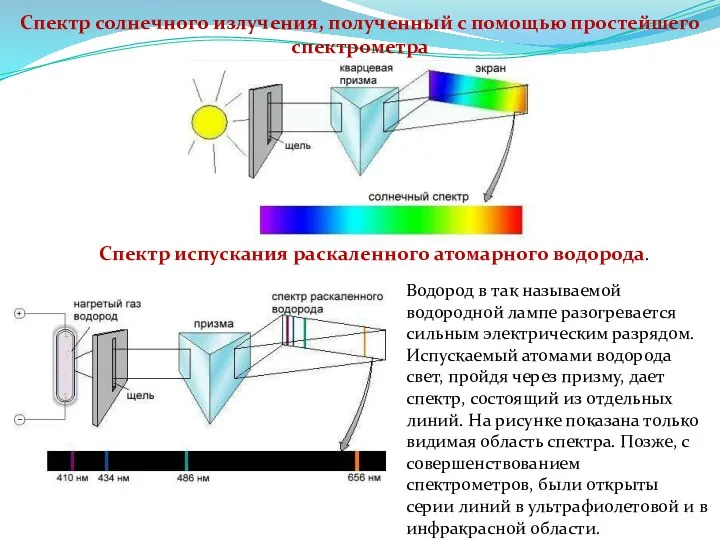
- 12. Спектр солнечного излучения, полученный с помощью простейшего спектрометра Водород в так называемой водородной лампе разогревается сильным
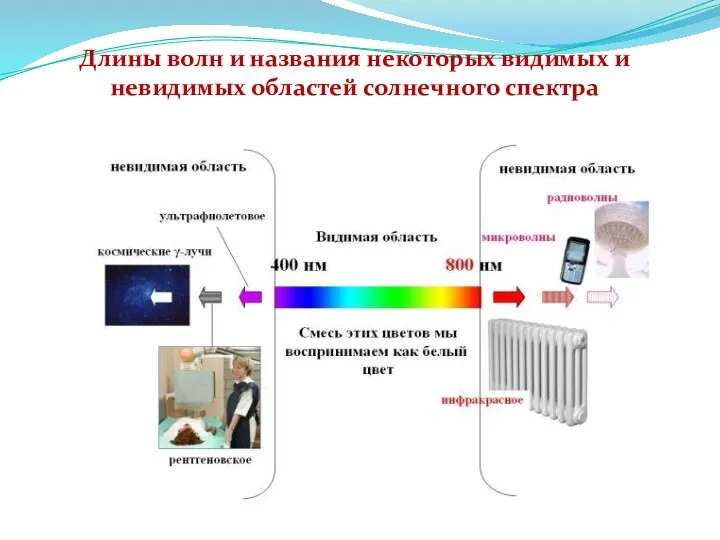
- 14. Длины волн и названия некоторых видимых и невидимых областей солнечного спектра
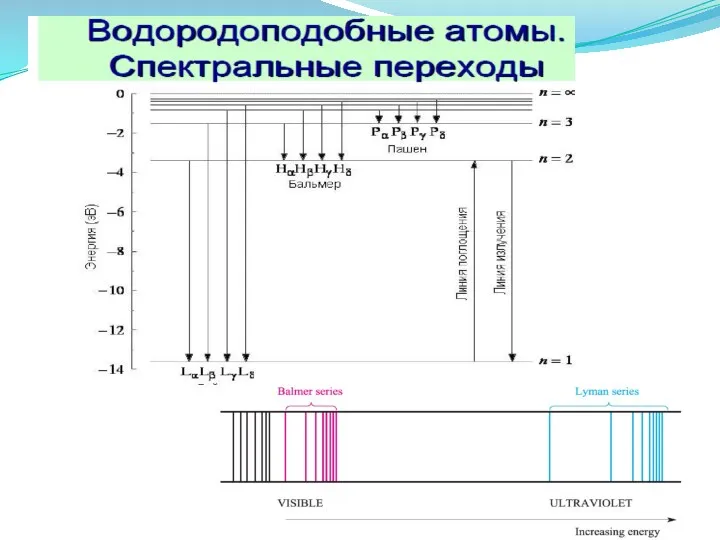
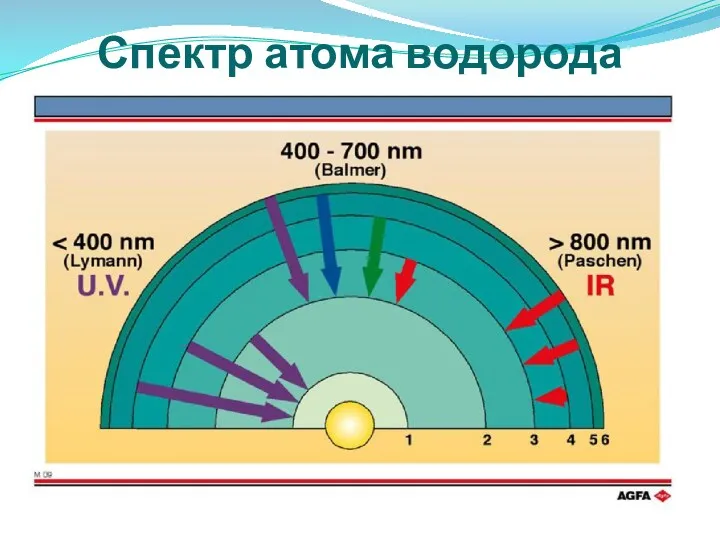
- 15. Спектр атома водорода
- 16. Создатели квантовой механики Вернер Карл Гейзенберг (1901-1976) В 1925 г. разработал матричную механику – первый вариант
- 17. 1-е Положение Квантовой Механики – Дуализм электронов Французский ученый Луи де Бройль (1892—1987), развивая представления о
- 18. 2-е Положение Квантовой Механики -Принцип неопределенности Гейзенберга 1. Невозможно с высокой степенью точности установить координаты местоположения
- 19. В 1926 году австрийский физик Э. Шредингер предложил уравнение, описывающее движение микрочастиц, проявляющих волновые свойства, которое
- 22. Главное квантовое число n – определяет… Принимает целочисленные значения от 1 до ∞ Чем > n
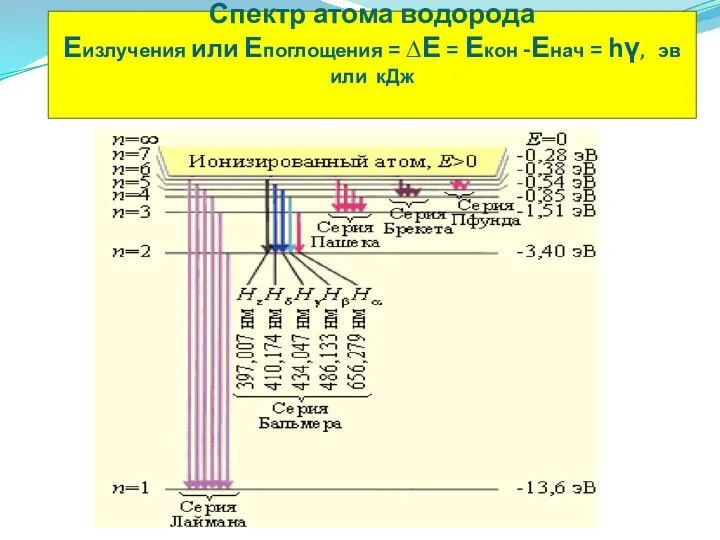
- 23. Спектр атома водорода Еизлучения или Епоглощения = ∆Е = Екон -Енач = hγ, эв или кДж
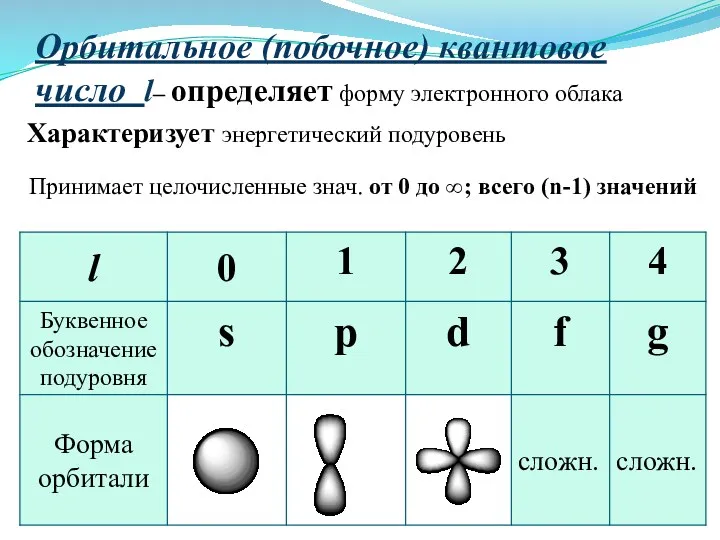
- 24. Орбитальное (побочное) квантовое число l– определяет форму электронного облака Характеризует энергетический подуровень Принимает целочисленные знач. от
- 26. Число подуровней, на которые расщепляется энергетический уровень равно номеру уровня. Например, Т.о., энергетический подуровень – это
- 27. Магнитное квантовое число ml Принимает все целочисленные значения от – l до + l Например, при
- 28. Следовательно, число значений ml это число орбиталей с данным значением l s - cостоянию соответствует одна
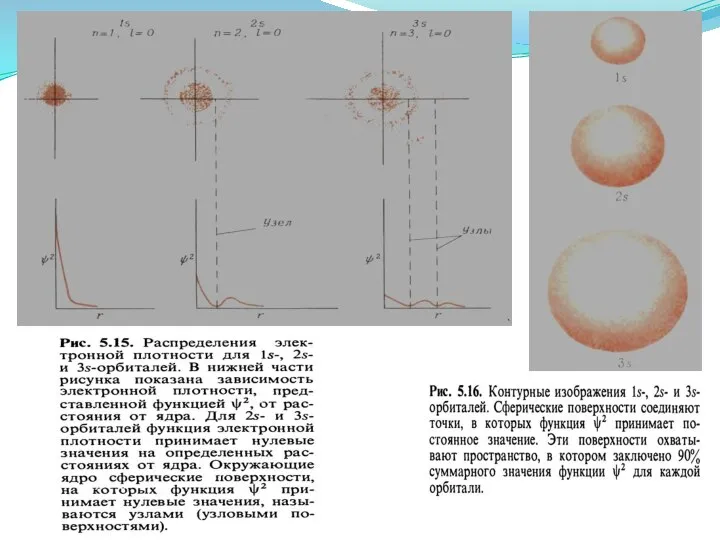
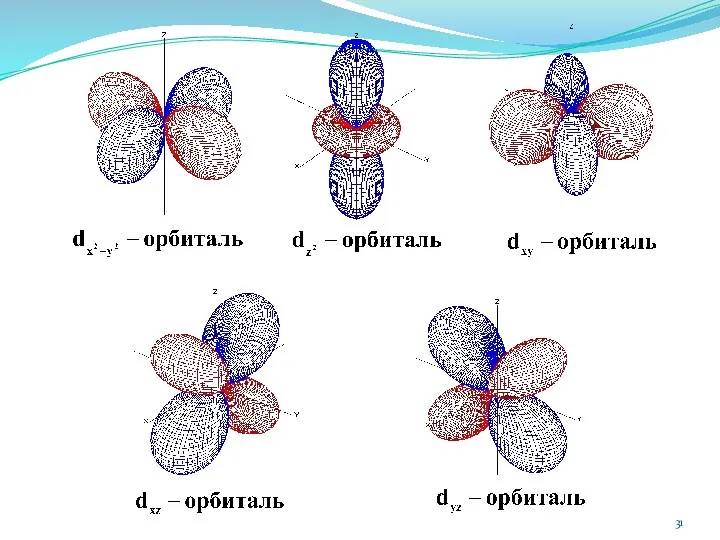
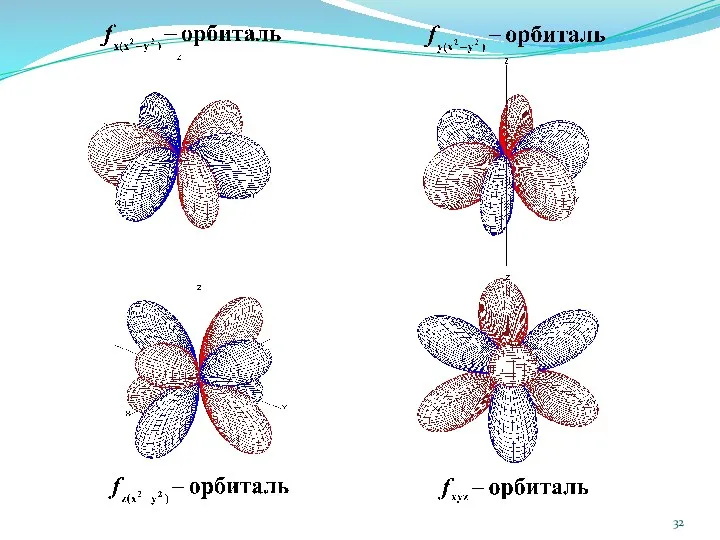
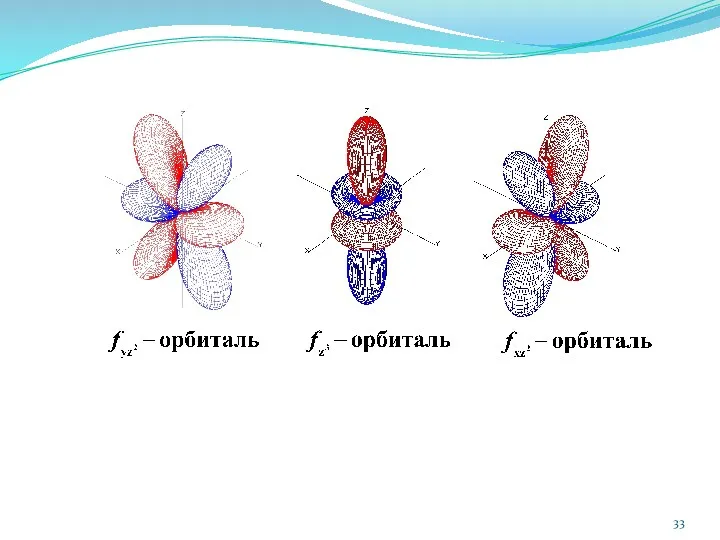
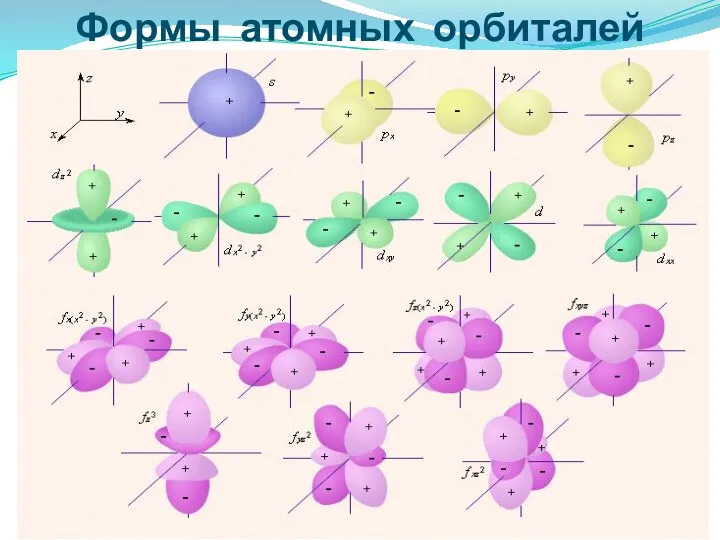
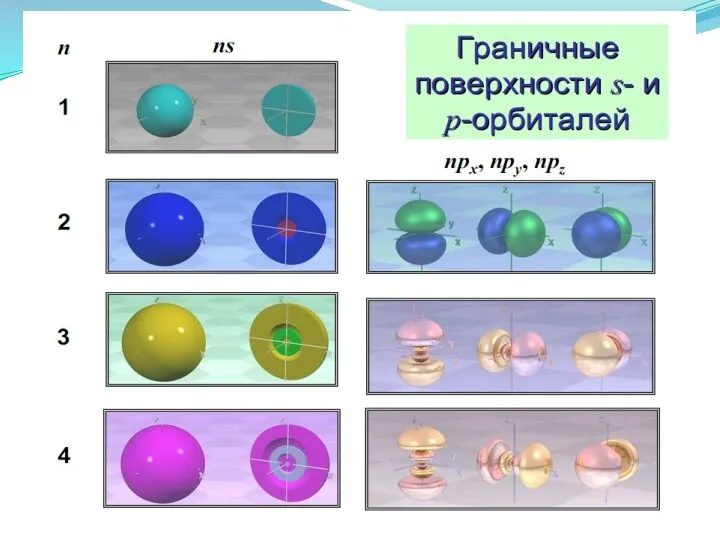
- 34. Формы атомных орбиталей
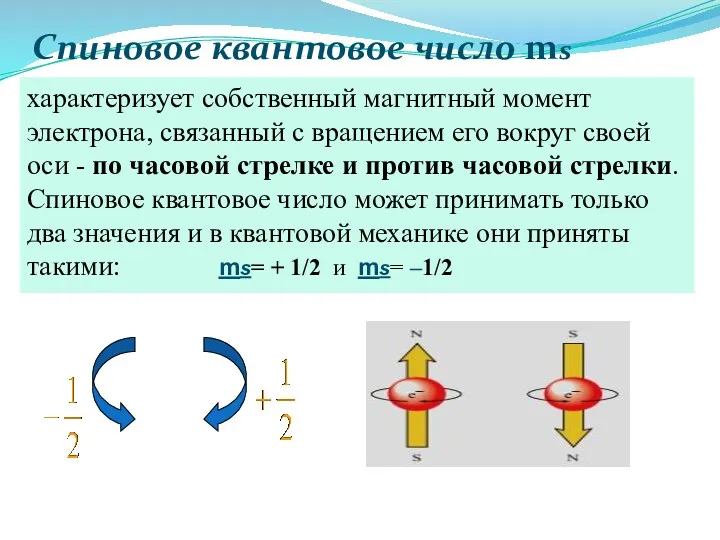
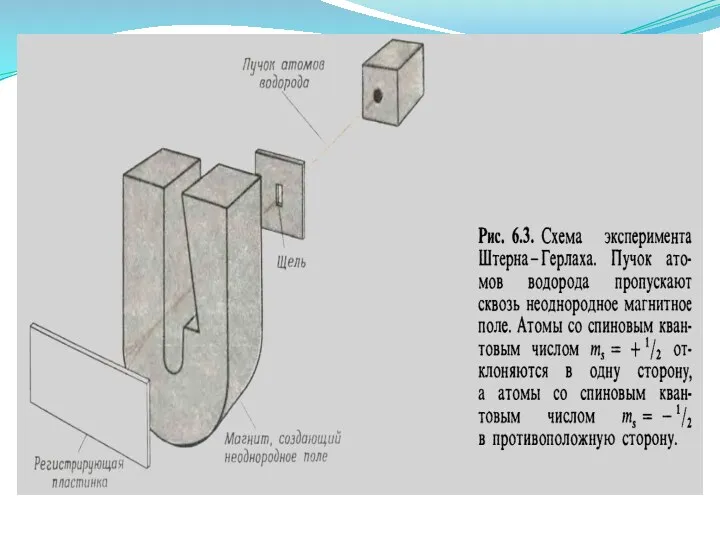
- 35. Спиновое квантовое число ms характеризует собственный магнитный момент электрона, связанный с вращением его вокруг своей оси
- 39. Скачать презентацию


















 Каучук и резина
Каучук и резина D-элементы VII-В группы. Марганец
D-элементы VII-В группы. Марганец Обмен нуклеопротеинов
Обмен нуклеопротеинов Кристаллофизика_часть_1
Кристаллофизика_часть_1 Проблемный химический эксперимент как составная часть проблемного обучения химии
Проблемный химический эксперимент как составная часть проблемного обучения химии Каталитический риформинг
Каталитический риформинг Выращивание кристаллов методом Чохральского
Выращивание кристаллов методом Чохральского AgCl негізіндегі нанокомпазиттердің фотокаталитикалық белсенділігі
AgCl негізіндегі нанокомпазиттердің фотокаталитикалық белсенділігі Катенаны. Ротаксаны (лекция 6)
Катенаны. Ротаксаны (лекция 6) Высокоэффективная жидкостная хроматография 1
Высокоэффективная жидкостная хроматография 1 Окислительно-восстановительные реакции в органической химии
Окислительно-восстановительные реакции в органической химии Crystallography. Part 4: Crystal Forms Twinning
Crystallography. Part 4: Crystal Forms Twinning Электрохимия. Часть 1
Электрохимия. Часть 1 Общие химические свойства металлов. Химия. 11 класс
Общие химические свойства металлов. Химия. 11 класс Металлы II группы главной подгруппы
Металлы II группы главной подгруппы Щелочные металлы. 9 класс
Щелочные металлы. 9 класс Сладкая жизнь. Проектно-исследовательская работа
Сладкая жизнь. Проектно-исследовательская работа Особенности строения соединений органической химии. 10 класс
Особенности строения соединений органической химии. 10 класс Распространенность химических элементов на земле и в космосе
Распространенность химических элементов на земле и в космосе Обобщение по теме Неметаллы
Обобщение по теме Неметаллы Изомерия
Изомерия Летучие яды. Токсичные газы
Летучие яды. Токсичные газы Химическое равновесие и способы его смещения
Химическое равновесие и способы его смещения Amino acid and protein metabolism II
Amino acid and protein metabolism II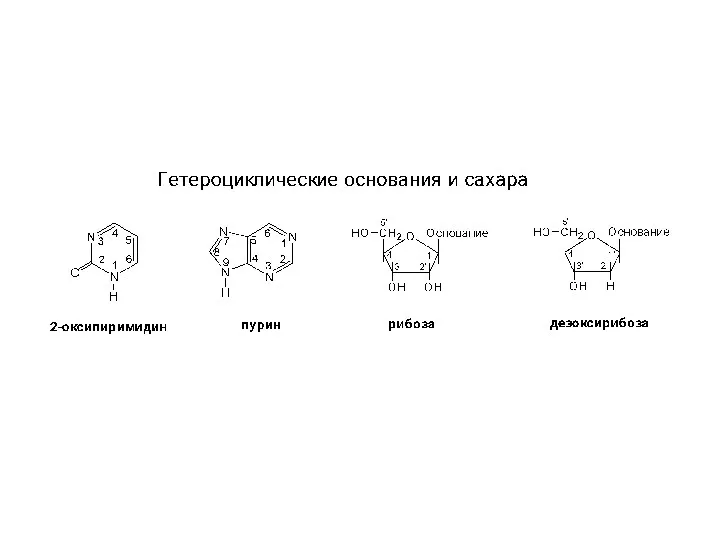 Структура гетероциклов, нуклеозидов и нуклеотидов
Структура гетероциклов, нуклеозидов и нуклеотидов Признаки и условия протекания химических реакций
Признаки и условия протекания химических реакций Молекулярно-массовые характеристики высокомолекулярных соединений
Молекулярно-массовые характеристики высокомолекулярных соединений Классификация веществ в зависимости от типа химической связи
Классификация веществ в зависимости от типа химической связи