Содержание
- 2. Поняття про дисперсні системи
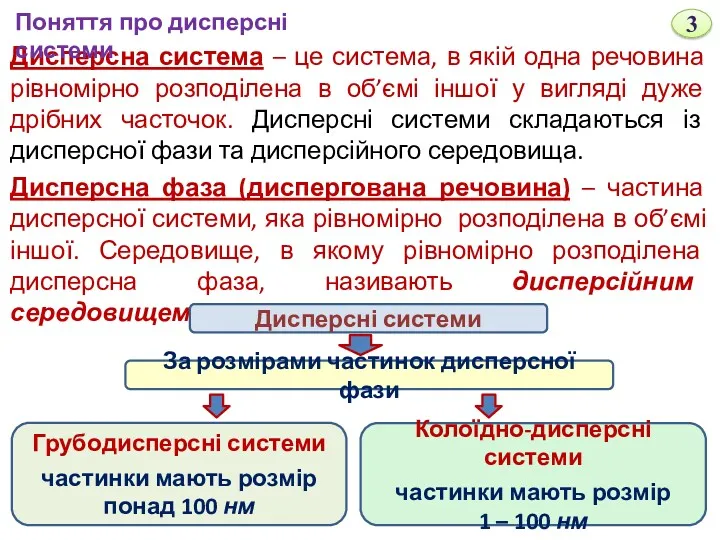
- 3. Дисперсна система – це система, в якій одна речовина рівномірно розподілена в об’ємі іншої у вигляді
- 4. До грубодисперсних відносяться такі системи: Суспензія – це система, в якій дисперсною фазою є тверда речовина,
- 5. Колоїдний розчин – це гетерогенна система, в якій частинки дисперсної фази рівномірно розподілені в рідкому дисперсійному
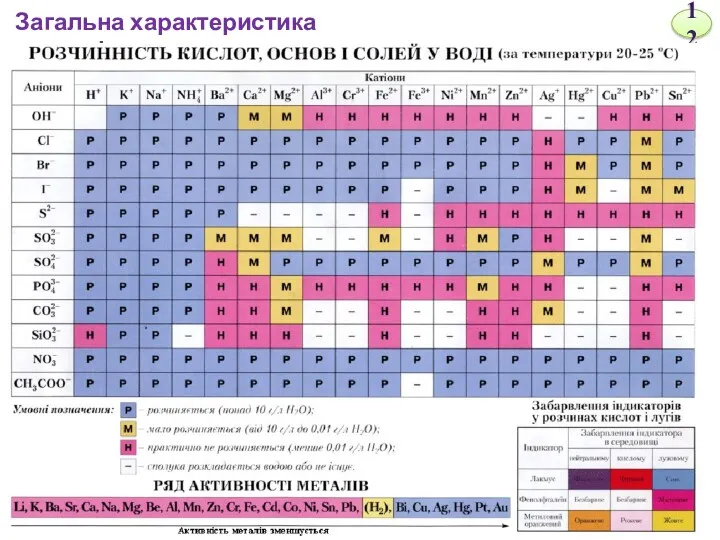
- 6. Загальна характеристика розчинів
- 7. Якщо речовина диспергована до розмірів молекул або йонів (менше ніж 1 нм), утворюється гомогенна система –
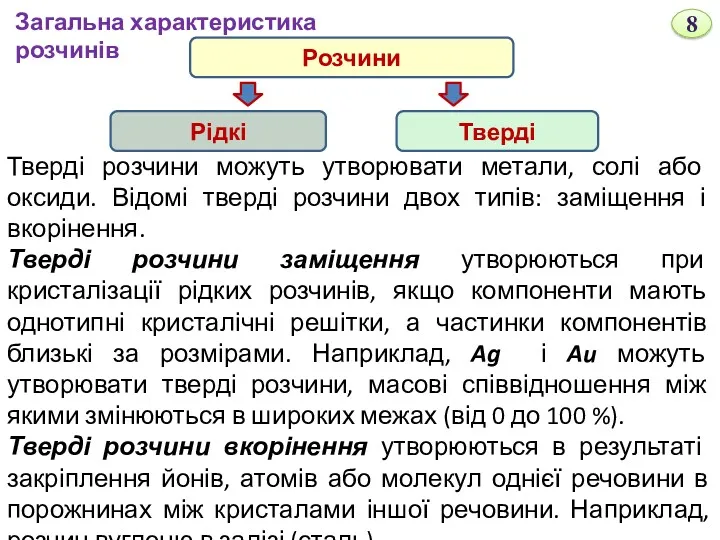
- 8. Тверді розчини можуть утворювати метали, солі або оксиди. Відомі тверді розчини двох типів: заміщення і вкорінення.
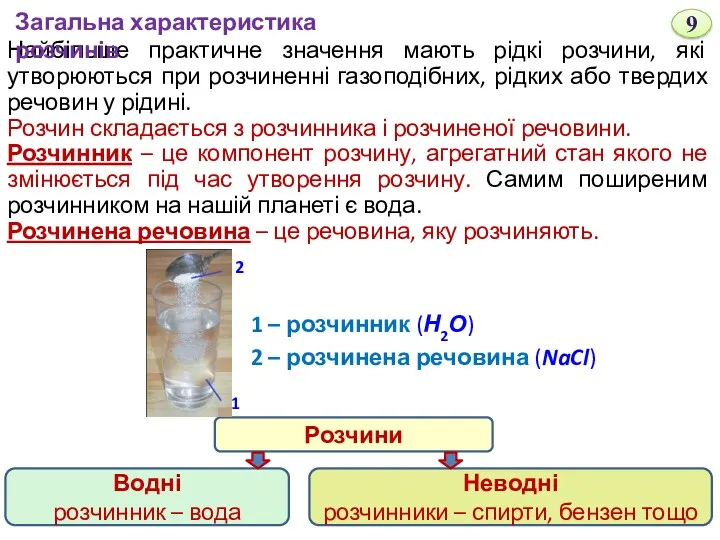
- 9. Найбільше практичне значення мають рідкі розчини, які утворюються при розчиненні газоподібних, рідких або твердих речовин у
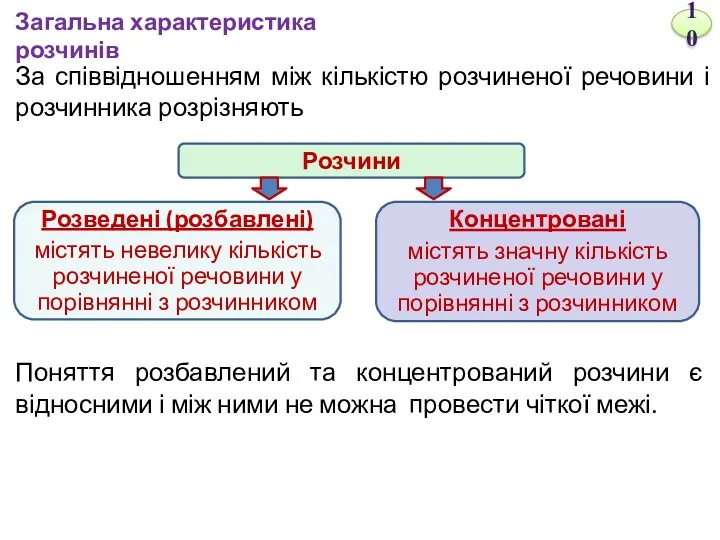
- 10. За співвідношенням між кількістю розчиненої речовини і розчинника розрізняють Поняття розбавлений та концентрований розчини є відносними
- 11. Наприклад, насичений розчин кухонної солі при 20 °С містить 36 г NaCl в 100 г води.
- 12. Загальна характеристика розчинів
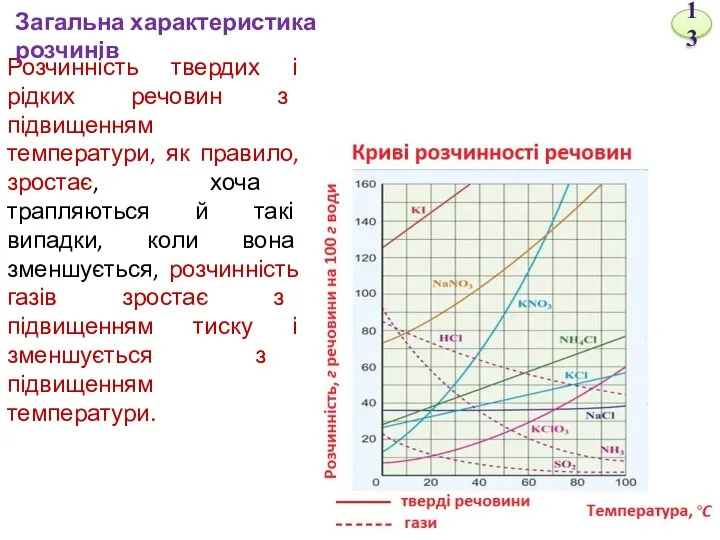
- 13. Розчинність твердих і рідких речовин з підвищенням температури, як правило, зростає, хоча трапляються й такі випадки,
- 14. Сучасна теорія розчинів розглядає розчинення як сукупність таких процесів: взаємодія розчинника з частинками розчиненої речовини —
- 15. Тепловий ефект розчинення складається з двох теплових ефектів, протилежних за знаком: ΔНрозчинення = ΔНсольв. + ΔНрозриву
- 16. Концентрація розчину і способи її вираження
- 17. Концентрація розчину – це вміст розчиненої речовини в одиниці маси або об’єму розчину. Масова частка розчиненої
- 18. Мольну частку обчислюють за формулою: де N1 – мольна частка одного з компонентів розчину; ν –
- 19. Молярна концентрація показує, скільки молів розчиненої речовини міститься в 1 л розчину. Молярну концентрацію розчину обчислюють
- 20. Молярна концентрація еквівалента (стара назва – нормальна концентрація) показує, скільки молів еквівалента розчиненої речовини міститься в
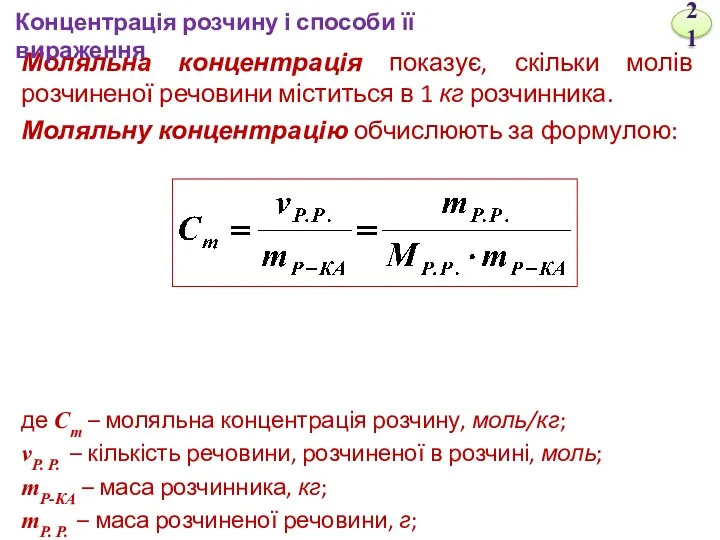
- 21. Моляльна концентрація показує, скільки молів розчиненої речовини міститься в 1 кг розчинника. Моляльну концентрацію обчислюють за
- 22. Колігативні властивості розчинів
- 23. Колігативні властивості розчинів – це властивості розчинів, які залежать лише від їхньої концентрації і не залежать
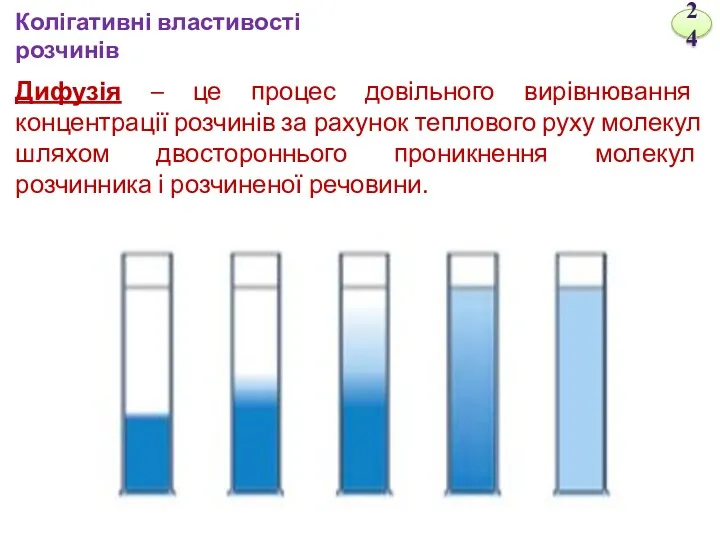
- 24. Дифузія – це процес довільного вирівнювання концентрації розчинів за рахунок теплового руху молекул шляхом двостороннього проникнення
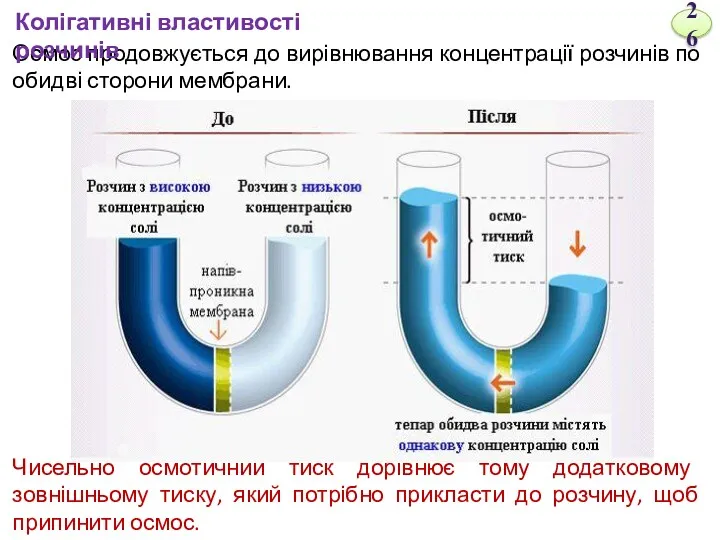
- 25. Осмос – це процес односторонньої дифузії молекул розчинника через напівпроникну мембрану з менш концентрованого у більш
- 26. Осмос продовжується до вирівнювання концентрації розчинів по обидві сторони мембрани. Чисельно осмотичний тиск дорівнює тому додатковому
- 27. Закон осмотичного тиску Вант-Гоффа: осмотичний тиск чисельно дорівнює тиску, який мала б розчинена речовина, якби вона
- 28. Осмос відіграє дуже велику роль у життєдіяльності живих організмів, оскільки стінки клітин біологічних тканин мають властивості
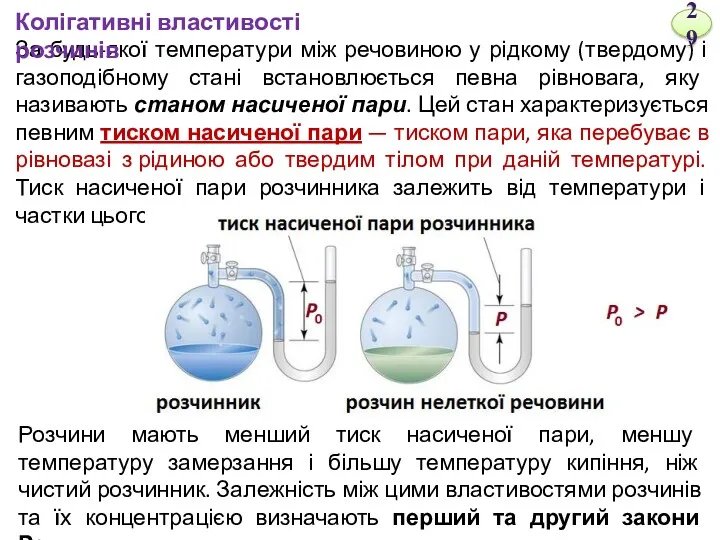
- 29. За будь-якої температури між речовиною у рідкому (твердому) і газоподібному стані встановлюється певна рівновага, яку називають
- 30. Перший закон Рауля: відносне пониження тиску насиченої пари над розчином порівняно з чистим розчинником дорівнює мольній
- 31. Тиск насиченої пари над розчином визначає їхню температуру кипіння і замерзання. Рідина закипає за температури, при
- 32. Другий закон Рауля: зменшення температури замерзання розчину і збільшення його температури кипіння порівняно з чистим розчинником
- 34. Скачать презентацию





















 Карбонові кислоти
Карбонові кислоти Молярна маса речовини
Молярна маса речовини Растворы. Общая характеристика растворов
Растворы. Общая характеристика растворов Скорость химической реакции
Скорость химической реакции Некоторые закономерности протекания химических реакций: тепловой эффект реакции, скорость реакции, химическое равновесие
Некоторые закономерности протекания химических реакций: тепловой эффект реакции, скорость реакции, химическое равновесие Степень окисления
Степень окисления Мыло. Мылящие вещества в природе
Мыло. Мылящие вещества в природе Виды и свойства текстильных материалов из химических волокон. 6 класс
Виды и свойства текстильных материалов из химических волокон. 6 класс Химико-аналитический контроль. Основы химико-аналитического контроля товаров
Химико-аналитический контроль. Основы химико-аналитического контроля товаров Қоспаларды бөлу әдістері
Қоспаларды бөлу әдістері Предельные углеводороды
Предельные углеводороды От кулинарии — к кулинохимии
От кулинарии — к кулинохимии Метали VI групи побічної підгрупи (Cr, Mo, W)
Метали VI групи побічної підгрупи (Cr, Mo, W) Классы неорганических соединений: Оксиды (8 класс)
Классы неорганических соединений: Оксиды (8 класс) Азот. Элемент V группы главной подгруппы
Азот. Элемент V группы главной подгруппы Номенклатура оснований. Классификация и примеры. Получение оснований. Химические свойства
Номенклатура оснований. Классификация и примеры. Получение оснований. Химические свойства Получение хлортетрациклина
Получение хлортетрациклина Реакции ионного обмена
Реакции ионного обмена Минеральные воды
Минеральные воды Химическое равновесие
Химическое равновесие Тепловой эффект химических реакций
Тепловой эффект химических реакций Химические элементы. Типы связей
Химические элементы. Типы связей Электротехнический фарфор – разновидность твердого фарфора
Электротехнический фарфор – разновидность твердого фарфора Химическая картина мира
Химическая картина мира Химические свойства кислот
Химические свойства кислот Производство метанола. Физико-химические основы синтеза метанола. Современные катализаторы
Производство метанола. Физико-химические основы синтеза метанола. Современные катализаторы Химическая организация клетки
Химическая организация клетки Формулы веществ. Относительная атомная масса. Относительная молекулярная масса. Массовая доля элементов в сложных веществах
Формулы веществ. Относительная атомная масса. Относительная молекулярная масса. Массовая доля элементов в сложных веществах