Содержание
- 2. По данной теме - минералогии выполняются лабораторные работы: «Физико-диагностические свойства минералов» «Важнейшие породообразующие минералы» Ход этих
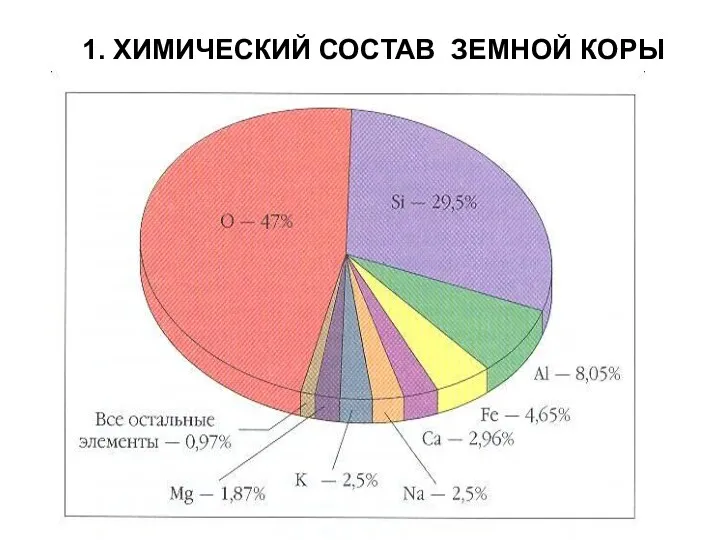
- 3. 1. ХИМИЧЕСКИЙ СОСТАВ ЗЕМНОЙ КОРЫ
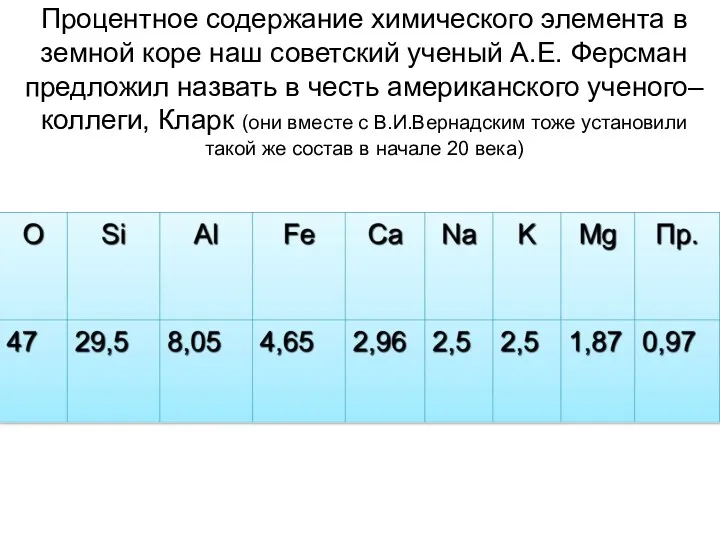
- 4. Процентное содержание химического элемента в земной коре наш советский ученый А.Е. Ферсман предложил назвать в честь
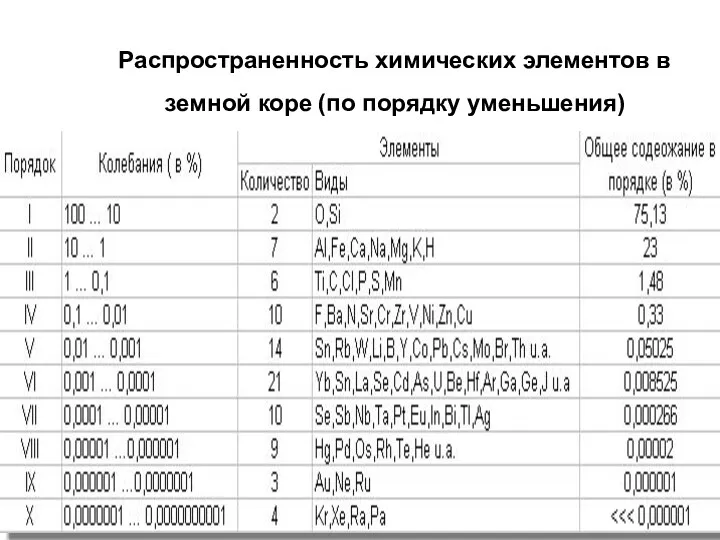
- 6. Распространенность химических элементов в земной коре (по порядку уменьшения)
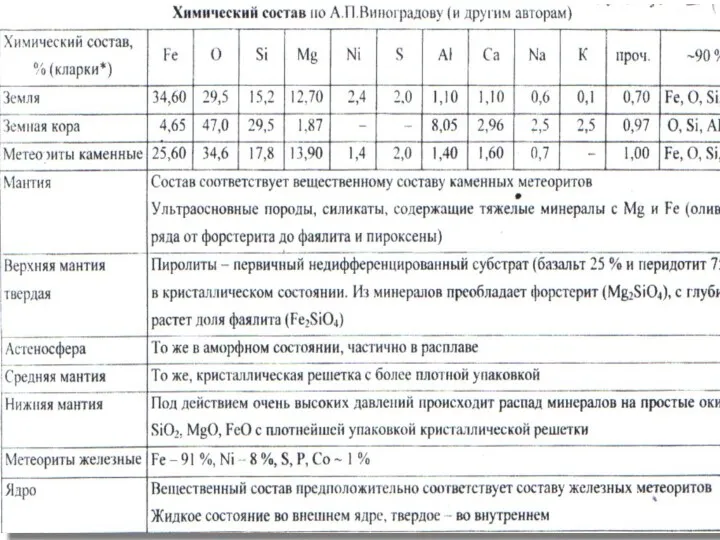
- 7. В целом, мы видим: В земной коре установлено около 85 химических элементов таблицы Менделеева. Химические элементы
- 8. Химические элементы Встречаются в земной коре и недрах Земли в виде природных химических соединения: SiO2, FeS2
- 9. 2. Основы минералогии Минералы - составные части горных пород в виде твердых - природных индивидов (кристаллов
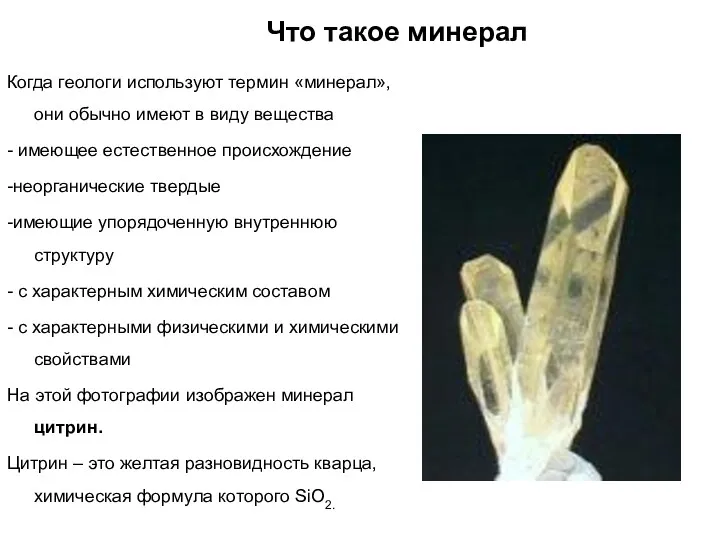
- 10. Что такое минерал Когда геологи используют термин «минерал», они обычно имеют в виду вещества - имеющее
- 11. Кристаллы граната в форме ромбододекаэдров Альмандин. Мама, Вост. Сибирь, Россия. Кристаллы до 2,5 см. Образцы: Мин.
- 12. Что такое минерал Голубой минерал на этой фотографии – кианит – Al2SiO5
- 13. 1. Кристалл пирита, 4,5 см. Навахун, Испания. 2. «Пиритовый доллар» - дисковый сферолит пирита. Диаметр 8
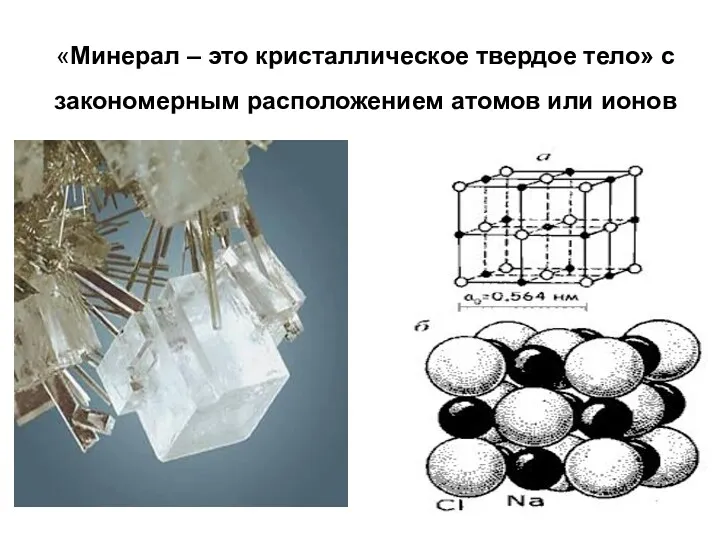
- 14. «Минерал – это кристаллическое твердое тело» с закономерным расположением атомов или ионов
- 15. Образование любого минерала Можно представить как присоединение химических элементов друг ко другу на минимальное расстояние, которое
- 16. Внутренняя структура минералов Мы можем условно рассматривать ионы в структуре минералов как сферы различного размера. Ионы
- 17. Периодическая система Периодическая система включает все известные химические элементы. Атомный номер химического элемента соответствует числу протонов
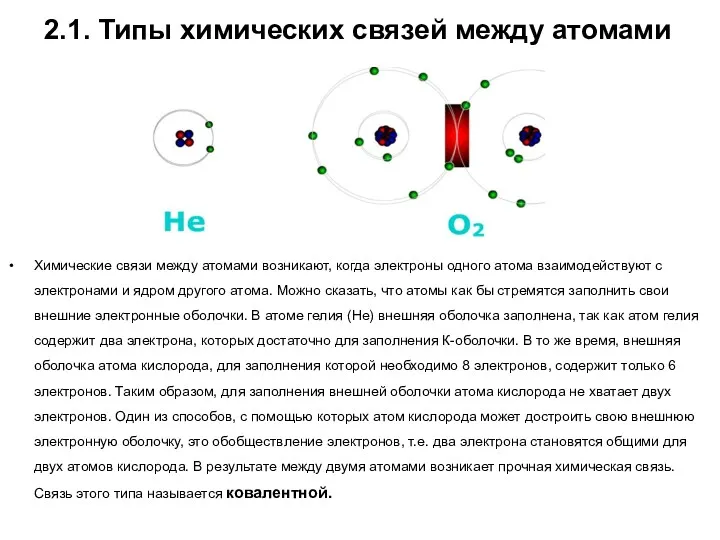
- 18. 2.1. Типы химических связей между атомами Химические связи между атомами возникают, когда электроны одного атома взаимодействуют
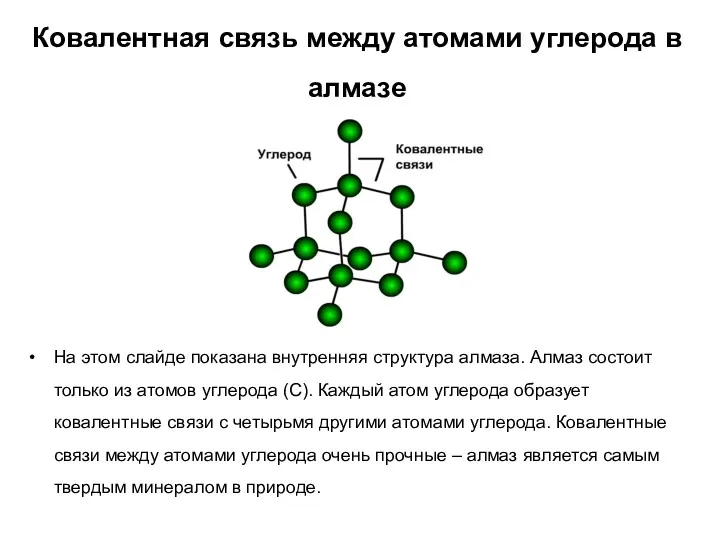
- 19. Ковалентная связь между атомами углерода в алмазе На этом слайде показана внутренняя структура алмаза. Алмаз состоит
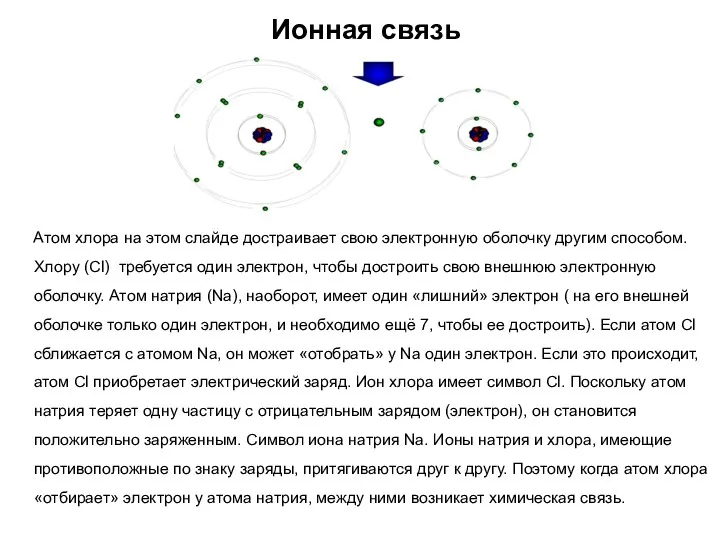
- 20. Ионная связь Атом хлора на этом слайде достраивает свою электронную оболочку другим способом. Хлору (Cl) требуется
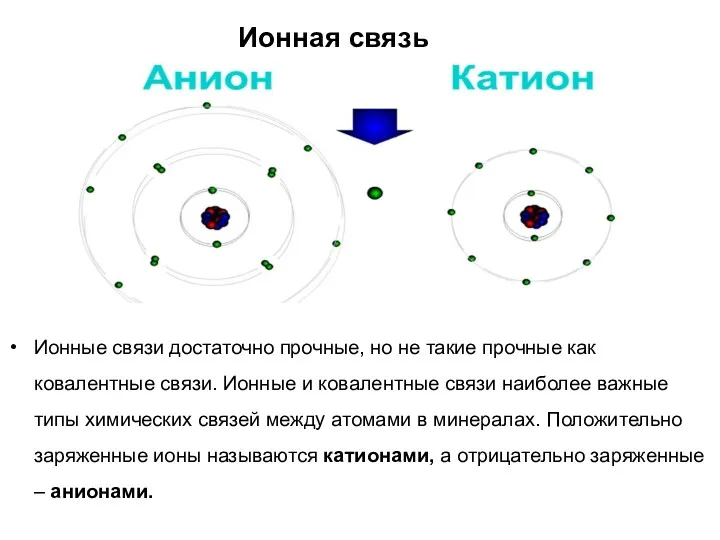
- 21. Ионная связь Ионные связи достаточно прочные, но не такие прочные как ковалентные связи. Ионные и ковалентные
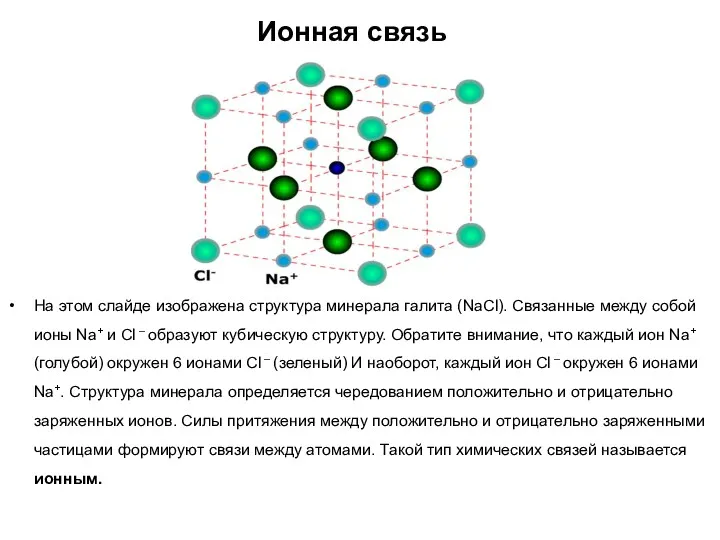
- 22. Ионная связь На этом слайде изображена структура минерала галита (NaCl). Связанные между собой ионы Na+ и
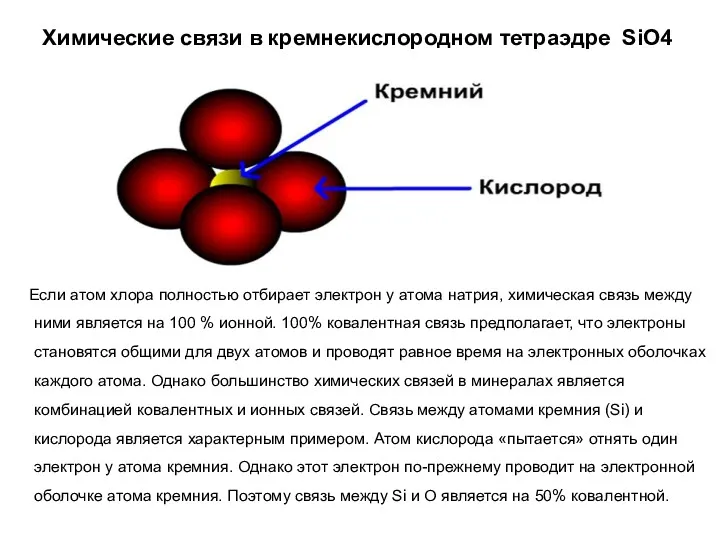
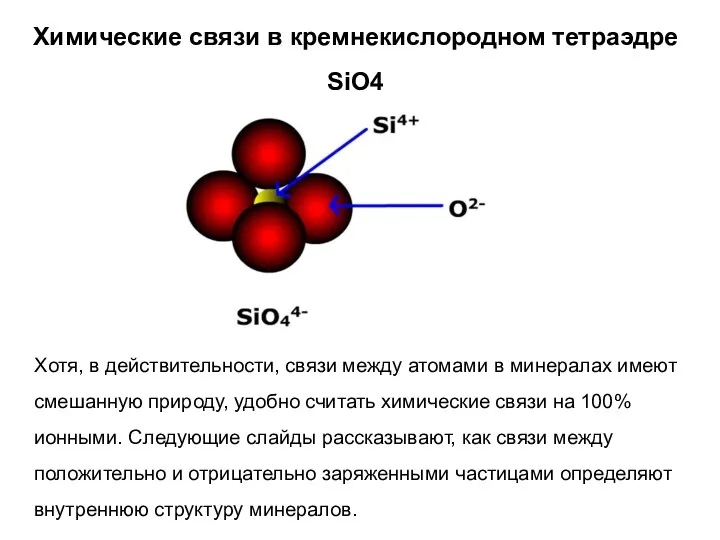
- 23. Химические связи в кремнекислородном тетраэдре SiO4 Если атом хлора полностью отбирает электрон у атома натрия, химическая
- 24. Химические связи в кремнекислородном тетраэдре SiO4 Хотя, в действительности, связи между атомами в минералах имеют смешанную
- 25. Другие типы химических связей Металлическая связь характерна для атомов металлов, которые имеют тенденцию легко расставаться с
- 26. Другие типы химических связей Ван дер Ваальсовы связи это слабые химические связи, которые возникают между электрически
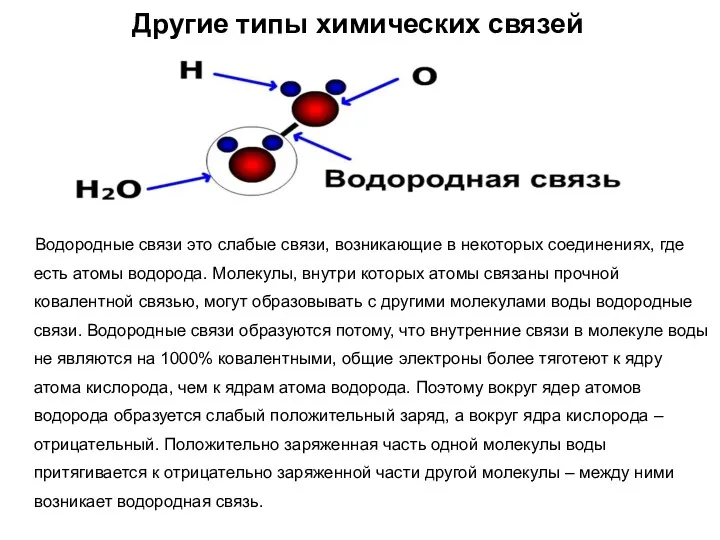
- 27. Другие типы химических связей Водородные связи это слабые связи, возникающие в некоторых соединениях, где есть атомы
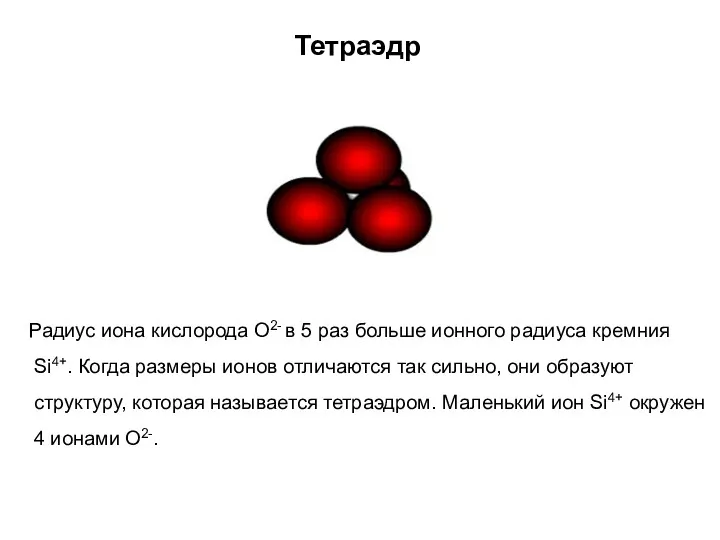
- 28. Тетраэдр Радиус иона кислорода О2- в 5 раз больше ионного радиуса кремния Si4+. Когда размеры ионов
- 29. Октаэдр Ионный радиус Na+ равен 0.99 и сильно отличается от ионного радиуса Cl- равного 1.81 Ангстрёма.
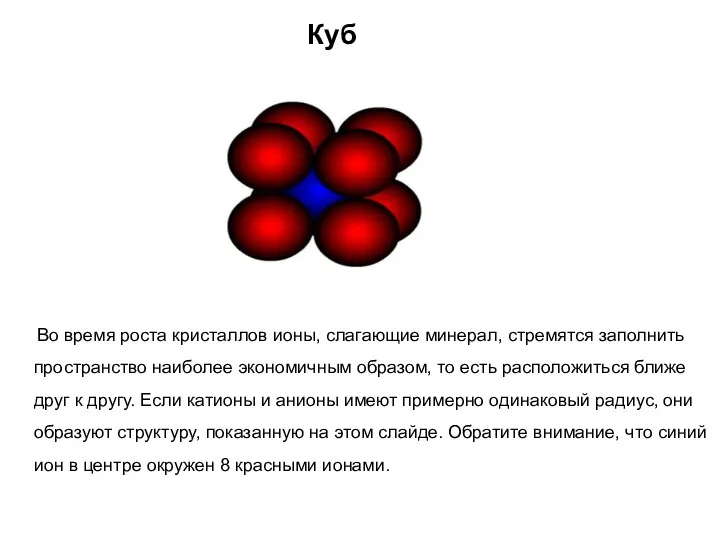
- 30. Куб Во время роста кристаллов ионы, слагающие минерал, стремятся заполнить пространство наиболее экономичным образом, то есть
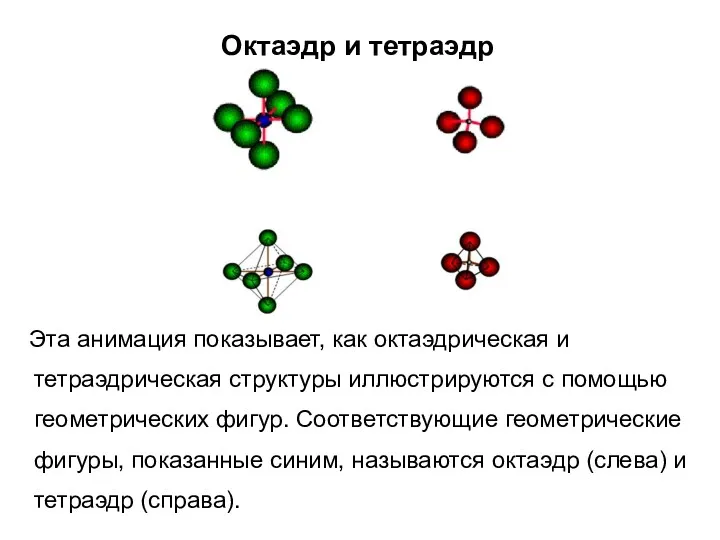
- 31. Октаэдр и тетраэдр Эта анимация показывает, как октаэдрическая и тетраэдрическая структуры иллюстрируются с помощью геометрических фигур.
- 32. 2.2. Внутренняя структура и форма кристаллов Форма кристаллов минерала зависит от его внутренней структурой. При формировании
- 33. Внутренняя структура и форма кристаллов Минералы пирит (FeS2) и галенит (PbS) также имеют кубическую структуру.
- 34. Внутренняя структура и форма кристаллов В основе структуры минерала кварца лежат кремнекислородные тетраэдры SiO4. В структуре
- 35. Внутренняя структура минералов На этих фотографиях кристаллы некоторых других минералов. Форма кристаллов минерала зависит от его
- 36. Морфология индивидов : алмаз, пирит гранат (куб.), турмалин (триг.)
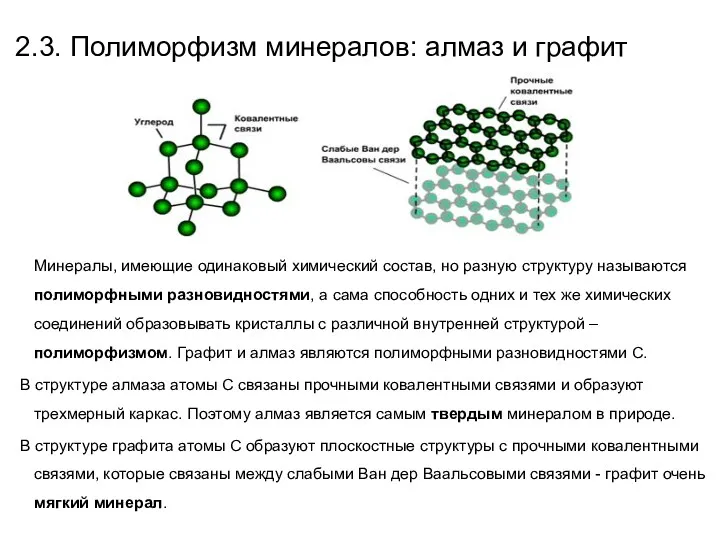
- 37. 2.3. Полиморфизм минералов: алмаз и графит Минералы, имеющие одинаковый химический состав, но разную структуру называются полиморфными
- 38. Полиморфизм - это явление кристаллизации химических соединений одного состава с образованием различных кристаллических структур и морфологий.
- 39. Полиморфизм минералов Графит, плотность которого 2,1 г/см3, стабилен до глубин порядка 50-60 км. Если кристалл графита
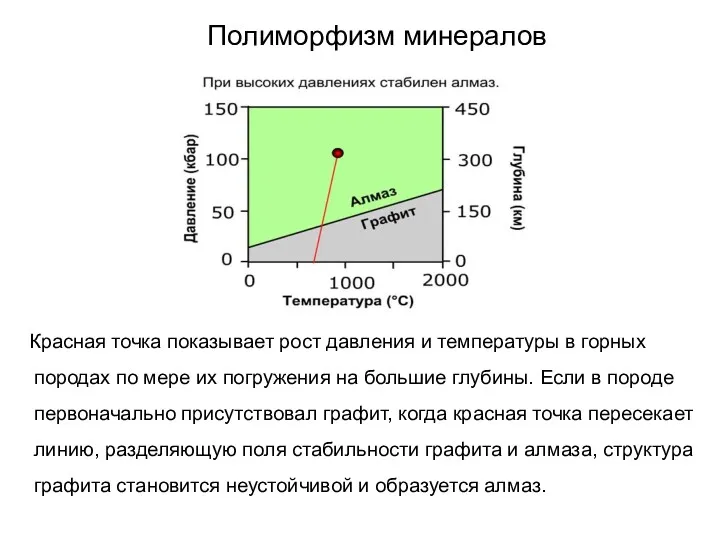
- 40. Полиморфизм минералов Красная точка показывает рост давления и температуры в горных породах по мере их погружения
- 41. 2.4. Изоморфизм - это способность химических элементов одиноковой валентности и близких ионных радиусов замещать друг друга
- 42. Изоморфизм На этом рисунке показаны размеры ионов, которые слагают наиболее распространенные породообразующие минералы. Цифрами обозначен радиус
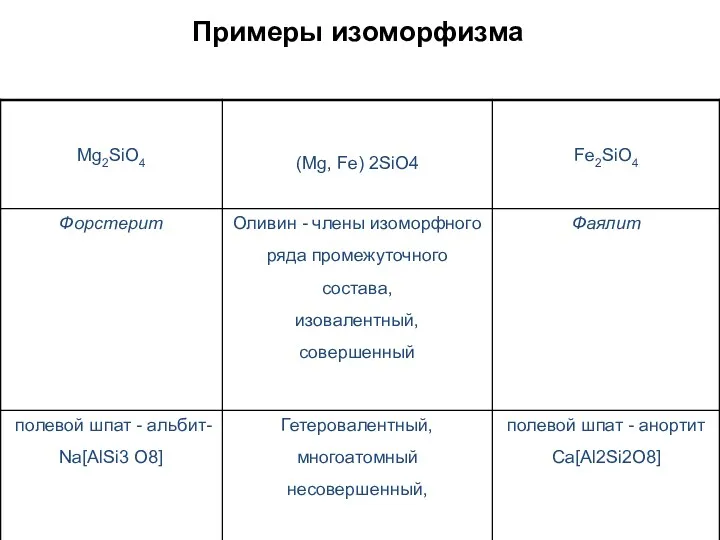
- 43. Примеры изоморфизма
- 44. Изоморфизм Na+ и К+ имеют одинаковый заряд (+1) и относительно крупные размеры. Na+ и К+ могут
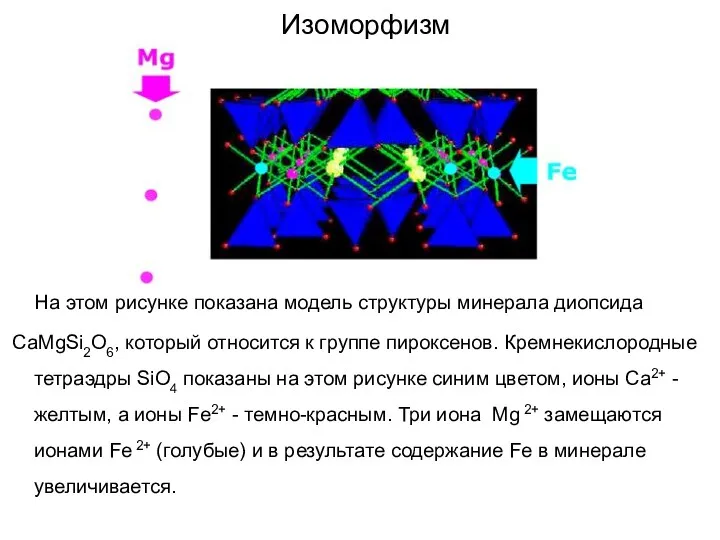
- 45. Изоморфизм Ионы Fe2+ и Mg2+ имеют одинаковый заряд и близкие размеры, поэтому они могут замещать друг
- 46. Изоморфизм На этом рисунке показана модель структуры минерала диопсида CaMgSi2O6, который относится к группе пироксенов. Кремнекислородные
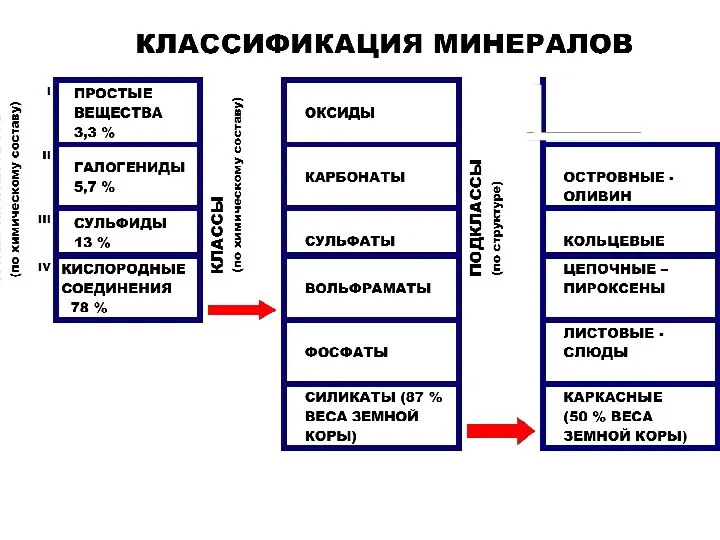
- 47. 3. Классификация минералов В природе зарегистрировано около 4000 (около 5000) минеральных видов. Часто минералы одного и
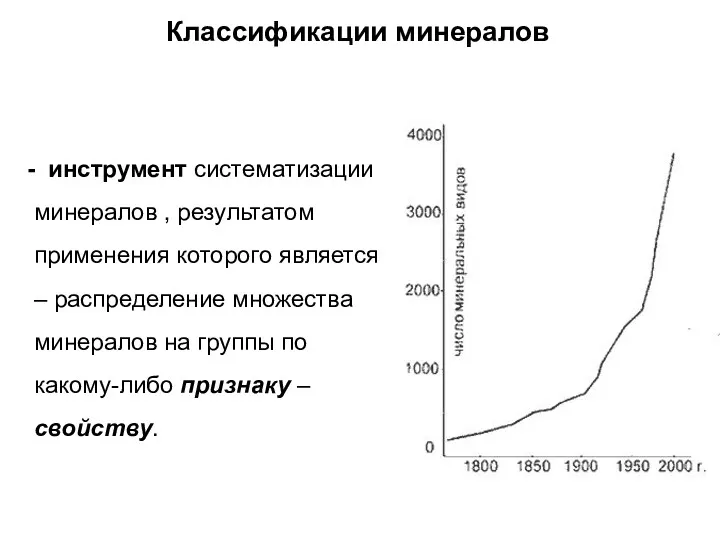
- 48. Классификации минералов - инструмент систематизации минералов , результатом применения которого является – распределение множества минералов на
- 49. Первые классификации минералов(18 век): по цвету по форме кристаллов по твердости (шкала Мооса, которую до сих
- 50. Классификации минералов (19 век): По химическому составу – по преобладающему элементу (минералы вольфрама, минералы бериллия, др.)
- 51. Современная кристаллохимическая классификация минералов опирается на 2 принципа: сходство химического состава – ведущий признак (№1), по
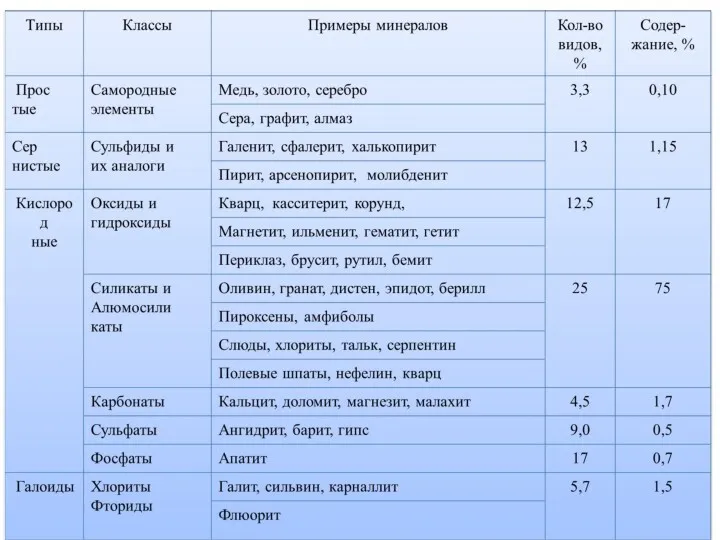
- 54. Учитывая ХС земной коры, мы видим, что среди минералов преобладают - класса силикаты, которые составляют примерно
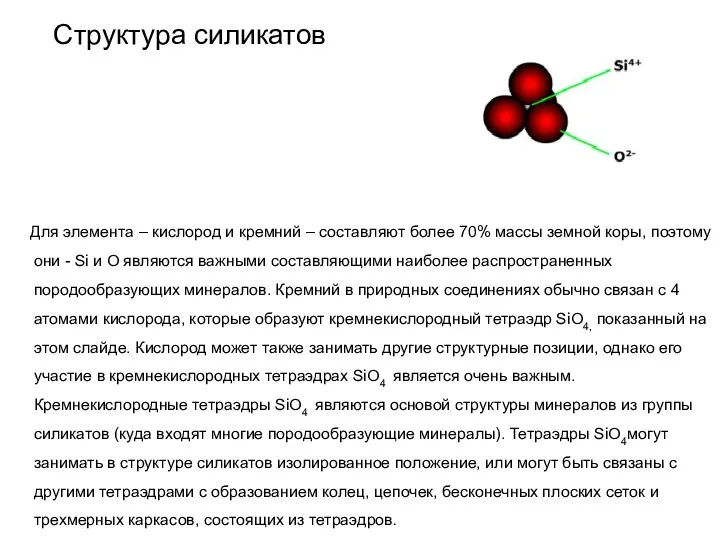
- 55. Структура силикатов Для элемента – кислород и кремний – составляют более 70% массы земной коры, поэтому
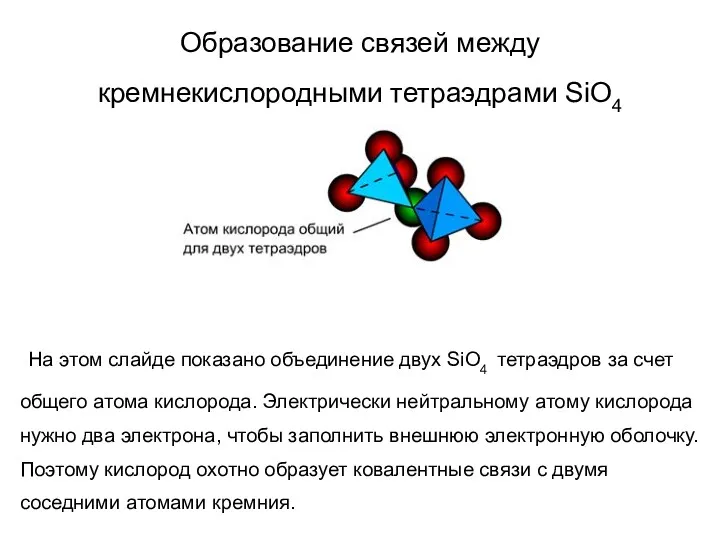
- 56. Образование связей между кремнекислородными тетраэдрами SiO4 На этом слайде показано объединение двух SiO4 тетраэдров за счет
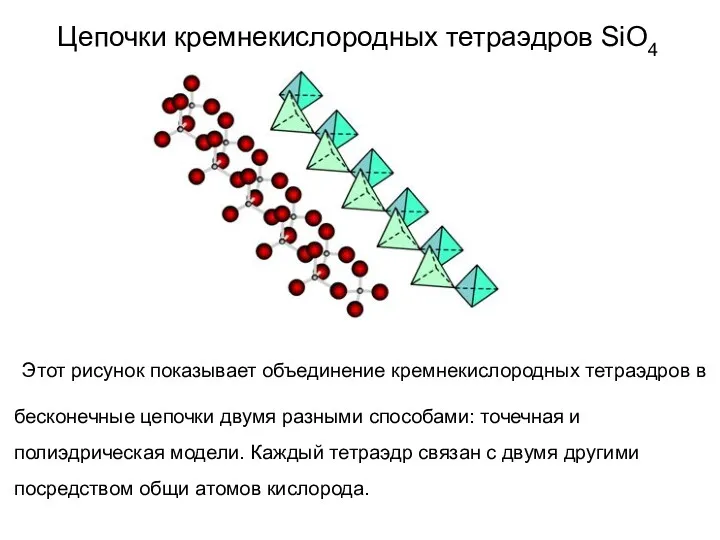
- 57. Цепочки кремнекислородных тетраэдров SiO4 Этот рисунок показывает объединение кремнекислородных тетраэдров в бесконечные цепочки двумя разными способами:
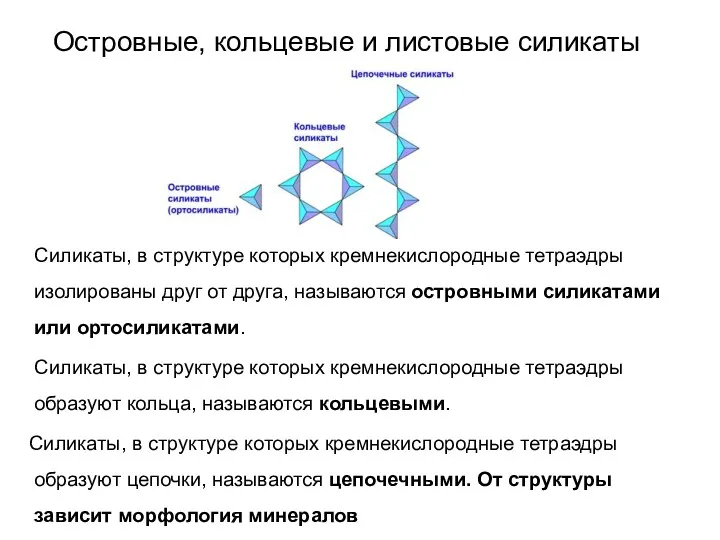
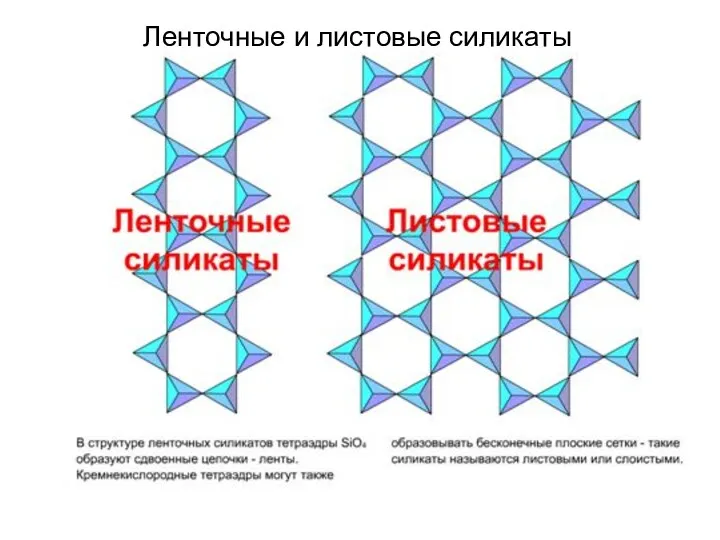
- 58. Островные, кольцевые и листовые силикаты Силикаты, в структуре которых кремнекислородные тетраэдры изолированы друг от друга, называются
- 59. Гроссуляр и циркон К островным или ортосиликатам относятся несколько минералов и минеральных групп. В структуре островных
- 60. Оливин и кианит Оливин и кианит также относятся к ортосиликатам. Формула оливина (Mg, Fe)2SiO4, а формула
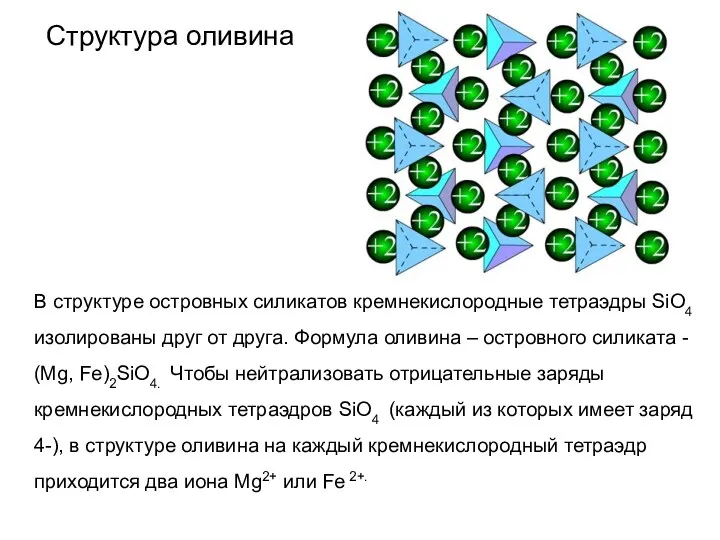
- 61. Структура оливина В структуре островных силикатов кремнекислородные тетраэдры SiO4 изолированы друг от друга. Формула оливина –
- 62. Излом оливина В структуре оливина между ионами Mg2+ и Fe 2+ и кремнекислородными тетраэдрами возникают ионные
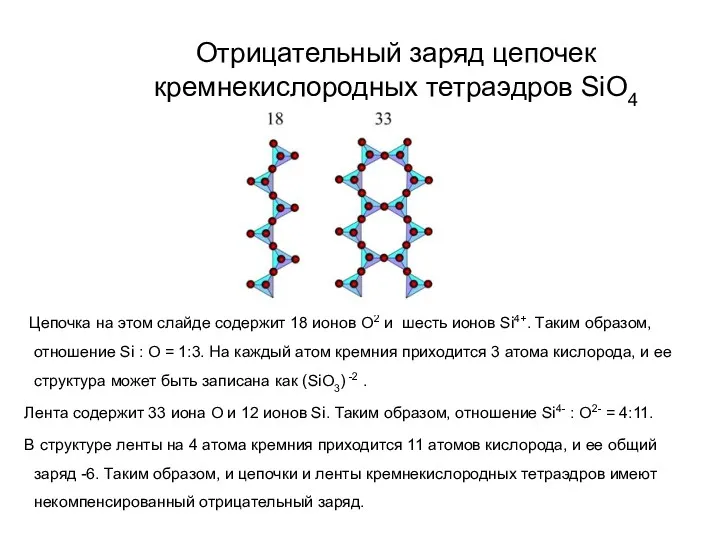
- 63. Отрицательный заряд цепочек кремнекислородных тетраэдров SiO4 Цепочка на этом слайде содержит 18 ионов О2 и шесть
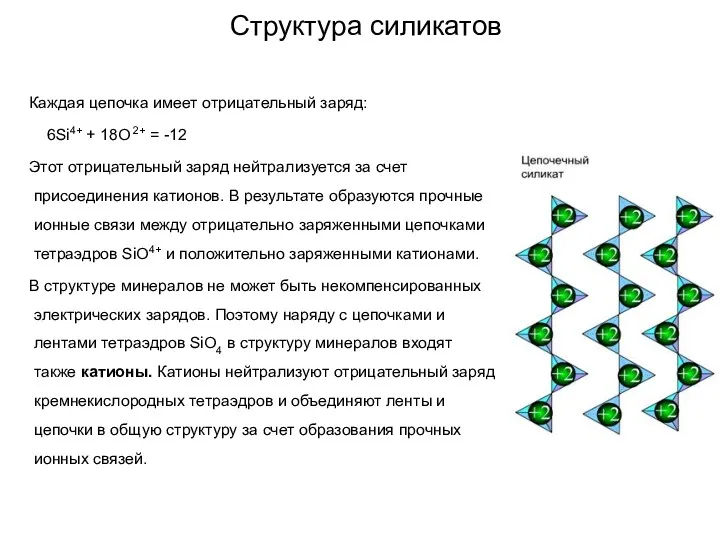
- 64. Структура силикатов Каждая цепочка имеет отрицательный заряд: 6Si4+ + 18O 2+ = -12 Этот отрицательный заряд
- 65. Пироксены Минералы из группы пироксенов являются наиболее распространенными цепочечными силикатами. Авгит – минерал из группы пироксенов.
- 66. Пироксены Другой минерал из группы пироксенов – диопсид. Формула диопсида CaMgSi2O6. В структуре диопсида нет атомов
- 67. Пироксены Геденбергит, который также относится к пироксенам, темно-зеленого цвета из-за присутствия железа. Формула геденбергита: CaFeSi2O6
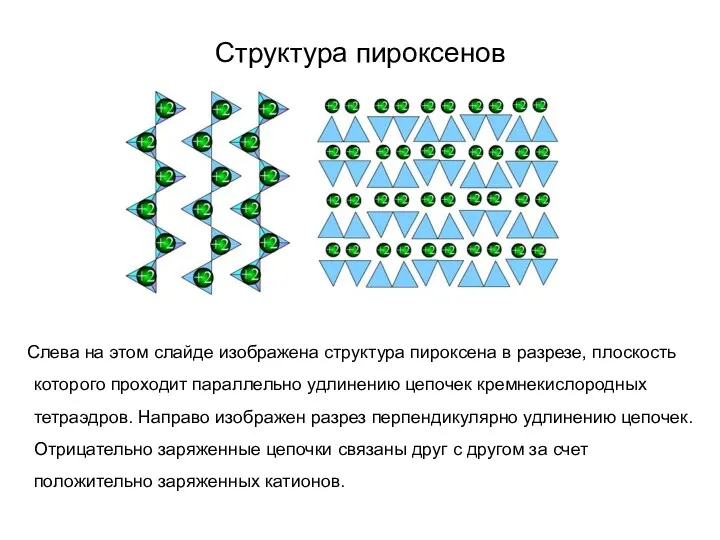
- 68. Структура пироксенов Слева на этом слайде изображена структура пироксена в разрезе, плоскость которого проходит параллельно удлинению
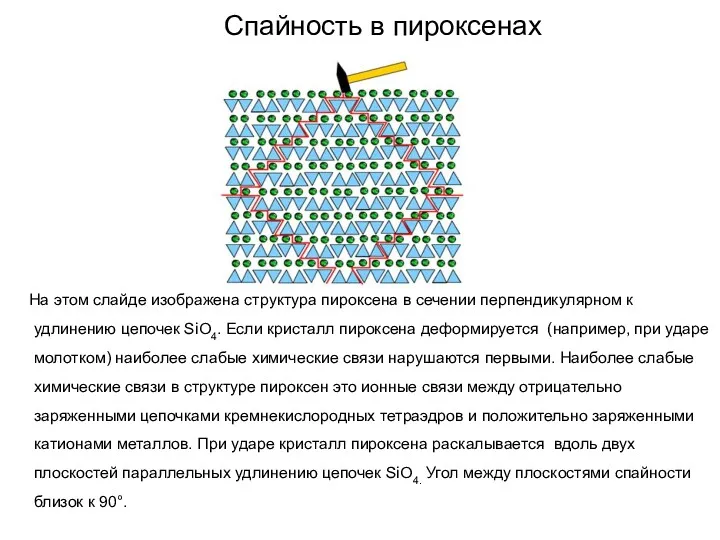
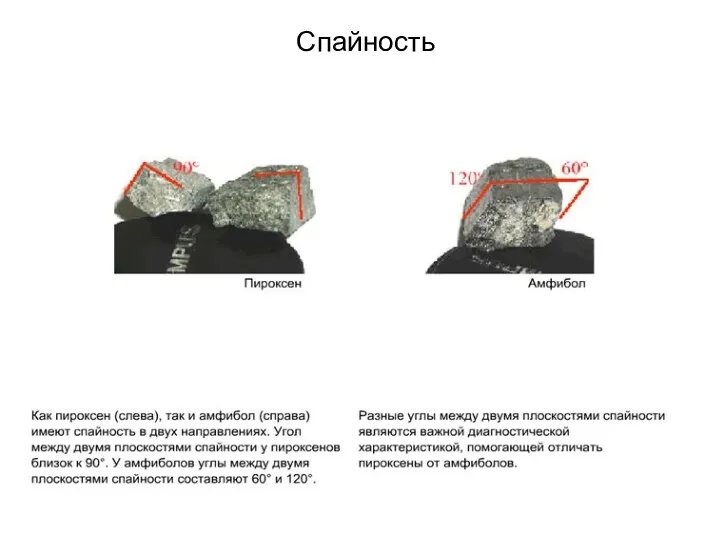
- 69. Спайность в пироксенах На этом слайде изображена структура пироксена в сечении перпендикулярном к удлинению цепочек SiО4.
- 70. Спайность в пироксенах Способность кристаллов минералов раскалываться по определенным направлениям называется спайностью. Спайность это важное свойство,
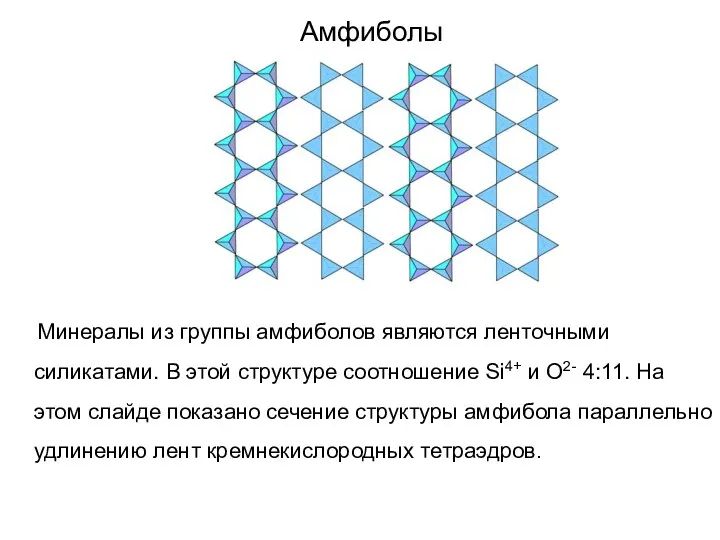
- 71. Амфиболы Минералы из группы амфиболов являются ленточными силикатами. В этой структуре соотношение Si4+ и O2- 4:11.
- 72. Амфиболы Тремолит и актинолит относятся к группе амфиболов. Формула тремолита: Ca2Mg5Si8O22(OH) 2. Актинолит имеет сходную формулу,
- 73. Амфиболы Слева кристалл из группы амфиболов - роговая обманка - Ca2 (Mg, Fe, Al)5Si8O22(OH) 2. Справа
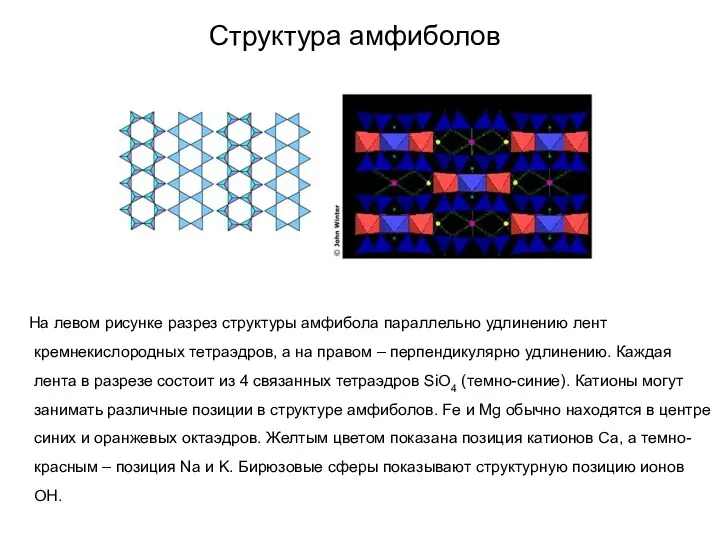
- 74. Структура амфиболов На левом рисунке разрез структуры амфибола параллельно удлинению лент кремнекислородных тетраэдров, а на правом
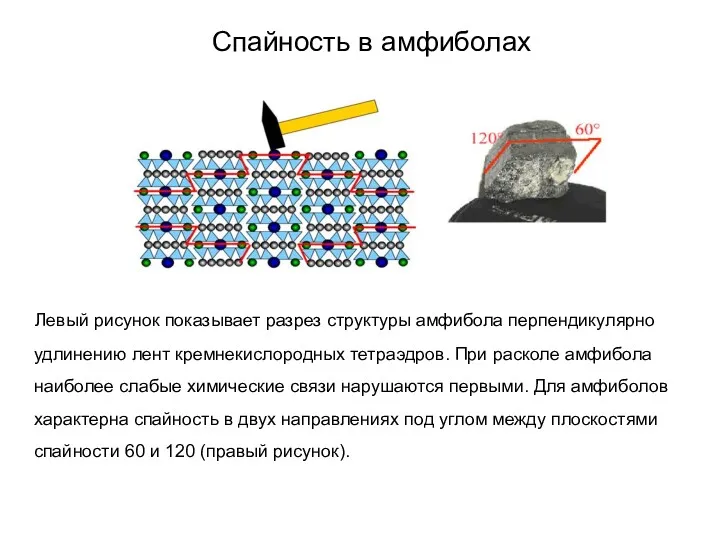
- 75. Спайность в амфиболах Левый рисунок показывает разрез структуры амфибола перпендикулярно удлинению лент кремнекислородных тетраэдров. При расколе
- 76. Асбест
- 77. Ленточные и листовые силикаты
- 78. Слюды
- 79. Другие листовые силикаты
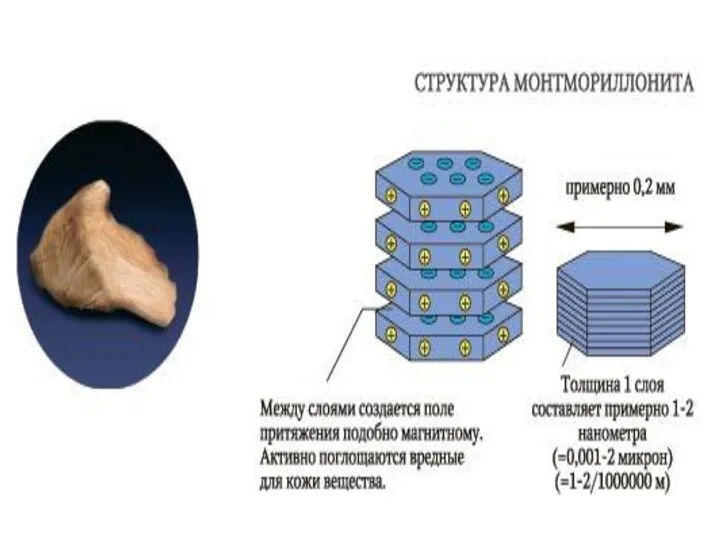
- 80. Другие листовые силикаты
- 81. Структура листовых силикатов
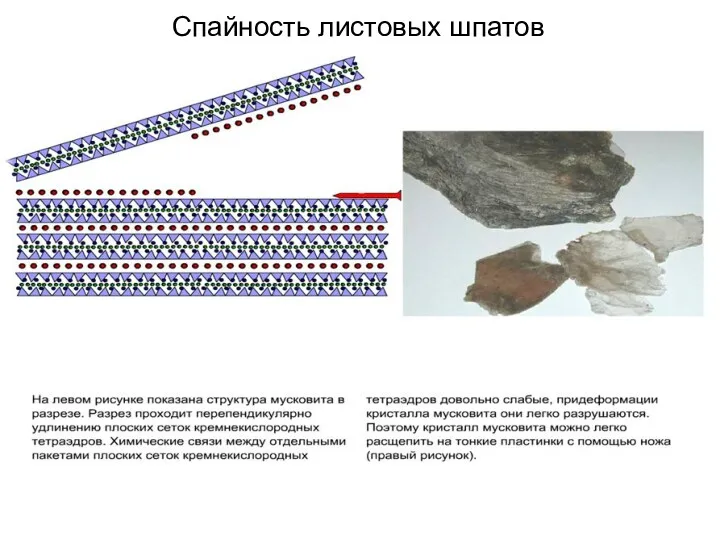
- 82. Спайность листовых шпатов
- 84. Каркасные силикаты
- 85. Щелочной полевой шпат
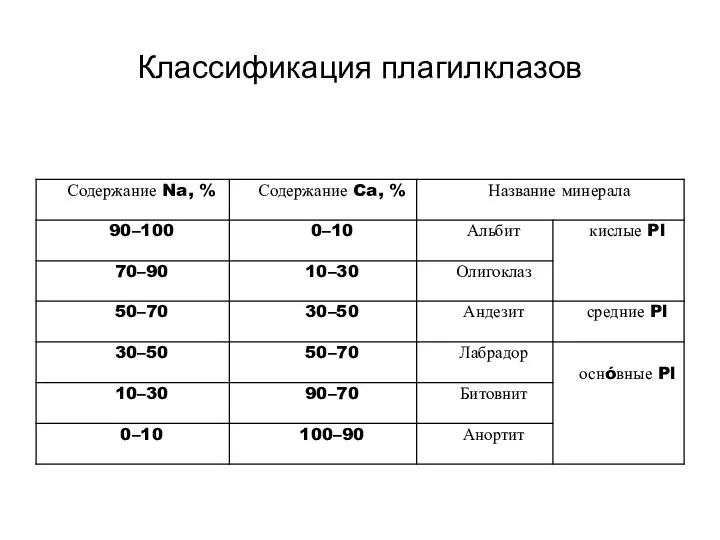
- 86. Плагиоклазы
- 87. Амазонит
- 88. Структура полевой шпатов
- 89. Спайность в полевых шпатах
- 90. Классификация плагилклазов
- 91. Все породообразующие силикаты делятся: Лейкократовые (светлые): - кварц - нефелин - гр. полевые шпаты: - K-Na-ортоклаз
- 92. Оксиды
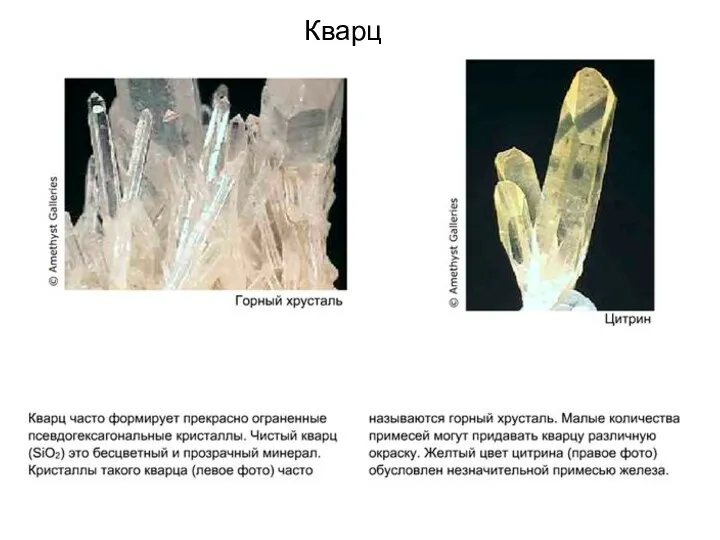
- 93. Кварц
- 94. Кварц
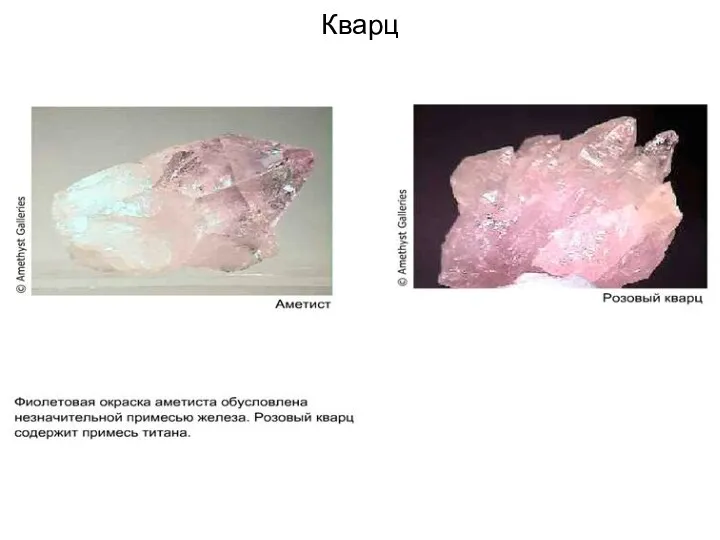
- 95. Кварц
- 96. Кварц
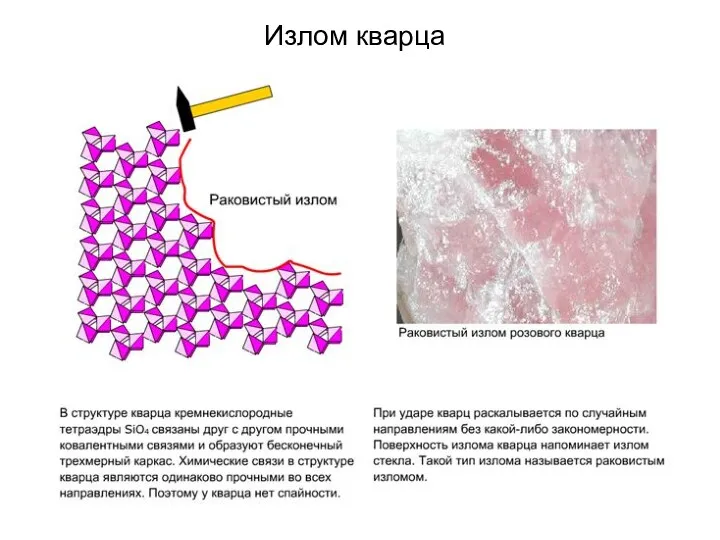
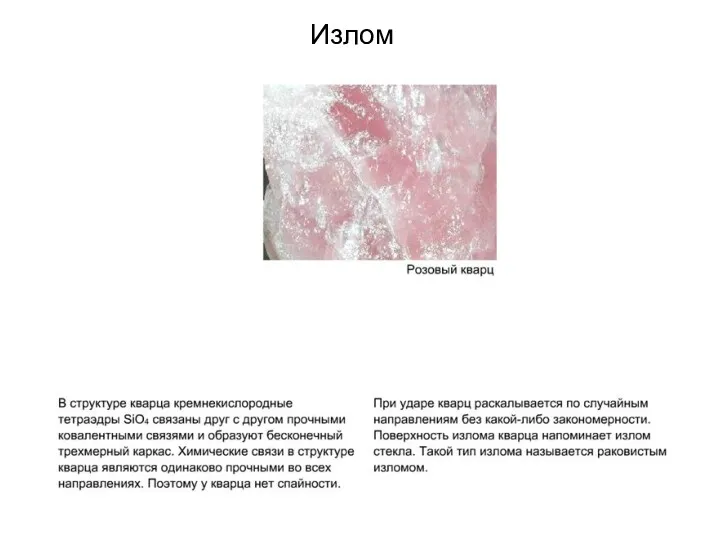
- 97. Излом кварца
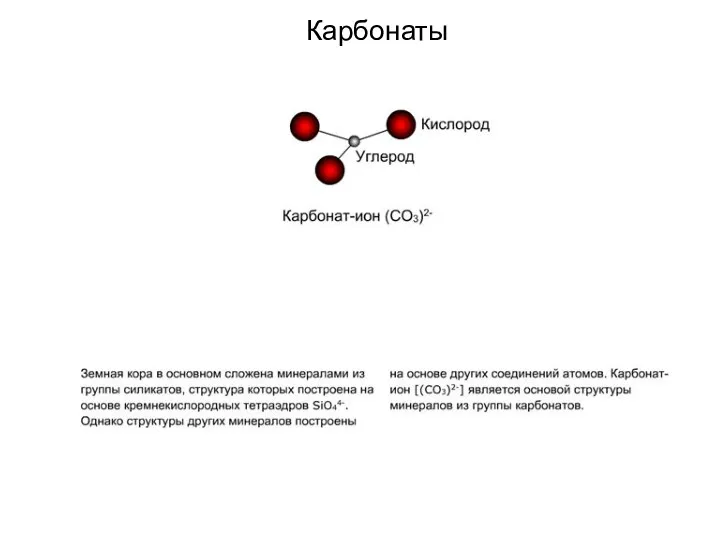
- 98. Карбонаты
- 99. Карбонаты
- 100. Кристаллы кальцита, до 3,5 см – агрегат – сростки, Ущ. Лухумисцкали, Грузия
- 101. Сульфаты
- 102. Сульфиды
- 103. Фосфаты
- 104. Современная минералогия Твердые природные соединения (вещества) аморфного, т.е. не упорядоченного строения - без кристаллической решетки, относит
- 105. 4. Физические свойства минералов
- 106. Твердость по шкале Мооса
- 107. Твердость по шкале Мооса
- 108. Спайность
- 109. Спайность
- 110. Спайность
- 111. Излом
- 112. Цвет
- 113. Цвет
- 114. Цвет черты
- 115. Габитус кристаллов
- 116. Магнитность
- 117. Растворимость
- 118. Плотность
- 119. Плотность
- 120. Поляризационный микроскоп
- 121. Гранат и амфибол под микроскопом
- 122. Эклогит под микроскопом
- 124. Скачать презентацию











































































 Кислоты. Растворы всех кислот
Кислоты. Растворы всех кислот Хімія та їжа
Хімія та їжа Химическая связь
Химическая связь Литий
Литий Классификация органических соединений
Классификация органических соединений Гидролиз солей
Гидролиз солей Аминокислоты. Пептиды. Белки
Аминокислоты. Пептиды. Белки Кремний и его соединения
Кремний и его соединения Гідроліз солей
Гідроліз солей Периодический закон Менделеева
Периодический закон Менделеева Изучение строения и свойств глюкозы
Изучение строения и свойств глюкозы Минералы. Принципы классификации минералов
Минералы. Принципы классификации минералов Лекция 6. Электрофильное присоединение к кратным связям
Лекция 6. Электрофильное присоединение к кратным связям Прикладные аспекты химии поверхностно-активных веществ
Прикладные аспекты химии поверхностно-активных веществ Фенолы
Фенолы Физико-химические процессы в системе свинец - сталь - кислород, для энергетических ядерных реакторов
Физико-химические процессы в системе свинец - сталь - кислород, для энергетических ядерных реакторов Теория строения органических соединений А.М. Бутлерова
Теория строения органических соединений А.М. Бутлерова Катионная полимеризация (Лекция 6)
Катионная полимеризация (Лекция 6) Теорія сильних і слабких електролітів. Рівновага в розчинах малорозчинних електролітів
Теорія сильних і слабких електролітів. Рівновага в розчинах малорозчинних електролітів Алюминий. Строение и свойство атомов
Алюминий. Строение и свойство атомов Методы исследования гидрохимического режима водоемов
Методы исследования гидрохимического режима водоемов Алкадиены
Алкадиены Кремний и его соединения. Простое вещество - кристаллический кремний Si
Кремний и его соединения. Простое вещество - кристаллический кремний Si Аналитическая химия. Предмет и задачи
Аналитическая химия. Предмет и задачи Вода. Практическая работа
Вода. Практическая работа Спирти
Спирти Электролитическая диссоциация. Вещества в растворах
Электролитическая диссоциация. Вещества в растворах Твердое состояние вещества. Плавление
Твердое состояние вещества. Плавление